-
2025-12-25 14:52
控病率80%+生存率84.6%!FDA批准通用型CART细胞疗法MT027的Ⅱ期临床试验,打破脑瘤、胃癌、肝癌等治疗桎梏

2025年12月21日,T-MAXIMUM制药公司宣布,其自主研发的同种异体B7-H3靶向CAR-T疗法MT027,已获美国FDA的IND批准,即将启动复发性胶质母细胞瘤(rGBM)II期临床试验。
-
2025-12-24 16:10白血病
CAR-T临床试验,pCAR-19B临床试验现正在急招白血病患者pCAR-19B细胞自体回输制剂是一款CAR-T细胞疗法,现正在开展在CD19阳性R/R B-ALL的安全性和耐受性的研究。 -
2025-12-24 15:36
2025年12月18日FDA批准阿米万他单抗(Rybrevant Faspro)用于治疗携带EGFR突变的非小细胞肺癌


2025年12月18日,皮下注射阿米万他单抗(阿米万他单抗和透明质酸酶-IPUJ,Rybrevant Faspro®)获美国食品药品监督管理局(FDA)批准,用于治疗携带EGFR突变的非小细胞肺癌(NSCLC)患者,其适应症与阿米万他单抗-VMJW(Rybrevant)相同。
-
2025-12-24 15:00
Neo-P DC疫苗治疗胰腺癌,81.3%诱导率+61个月零死亡
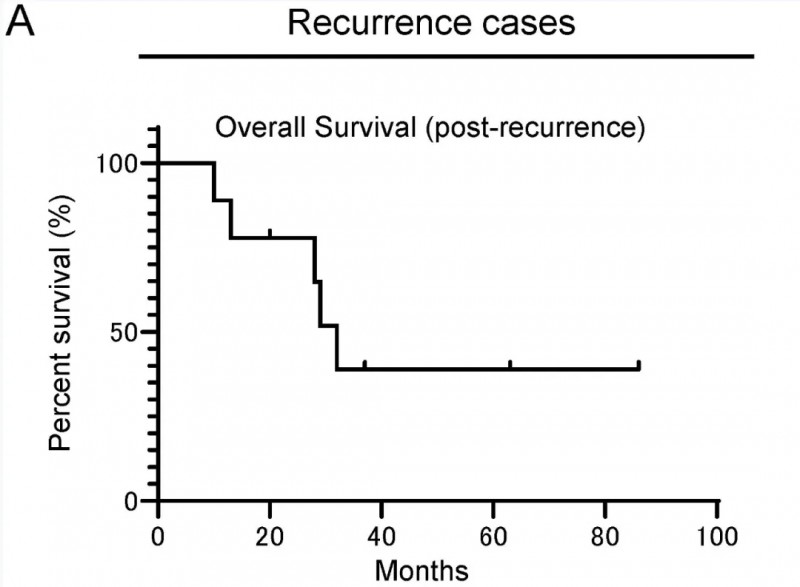
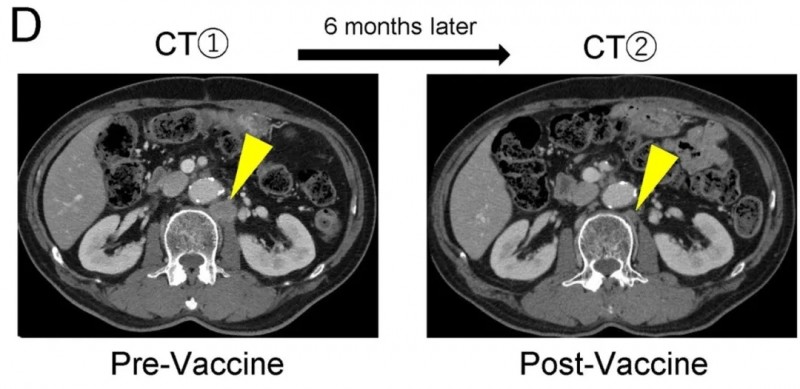
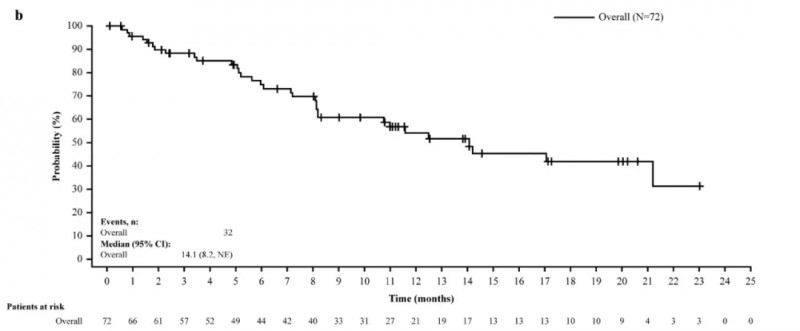
2025年4月,《癌症免疫与免疫疗法》发表的一项回顾性研究,评估了胰腺癌患者术后接受新抗原肽脉冲树突状细胞(Neo-P DC)疫苗疗法的安全性与有效性。
-
2025-12-24 11:57
硬核抗癌!美国MD安德森癌症中心六项“救命研究”齐发,重塑白血病/肺癌/肠癌/卵巢癌等预后
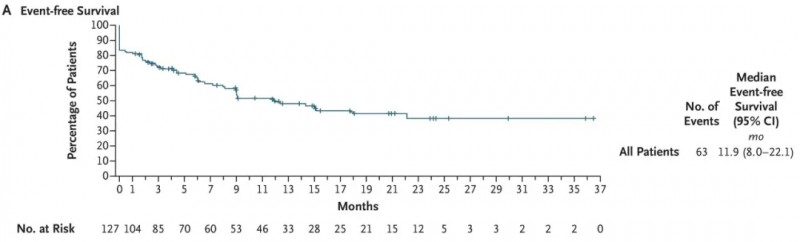
作为全球癌症研究的引领者,MD安德森癌症中心的研究团队在过去一年持续突破医学边界——从推动临床试验成果加速获得美国食品药品监督管理局(FDA)批准,到开展为癌症治疗突破筑牢基础的探索性研究。
-
2025-12-23 16:21肿瘤临床试验
HDAC抑制剂注射用甲磺酸普依司他临床试验现正招募实体瘤患者甲磺酸普依司他是一种组蛋白去乙酰化酶(HDAC)抑制剂,通过调节基因表达和抑制肿瘤细胞增殖发挥作用。 -
2025-12-23 14:13
双靶点CAR-T治疗胶质母细胞瘤,62%患者肿瘤消退
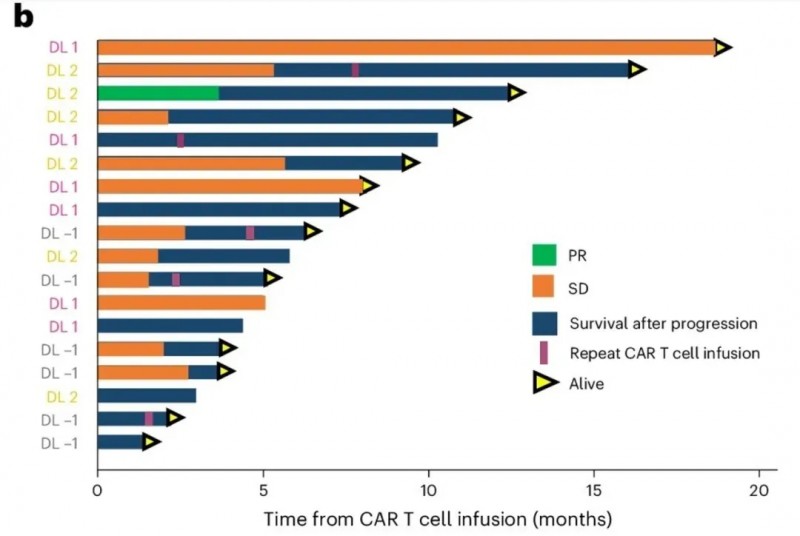
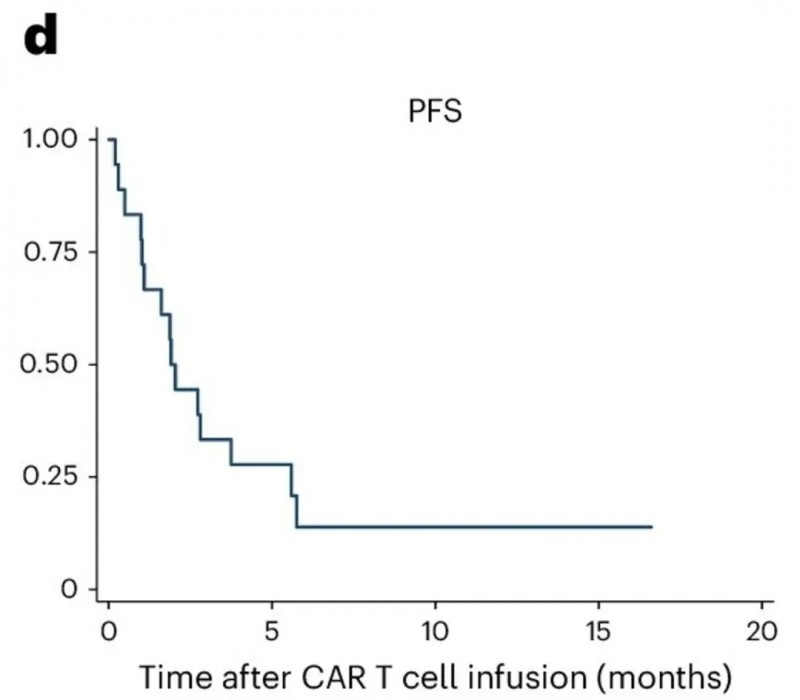
2025年6月1日,宾夕法尼亚大学佩雷尔曼医学院的研究团队在全球权威期刊《Nature Medicine》上,公布了一项I期临床试验(NCT05168423)的振奋数据。
-
2025-12-23 11:58
全球首创Vx001疫苗治疗晚期肺癌帮患者中位总生存超21个月


Vx-001是全球首个采用“优化隐蔽肽”策略的创新疫苗,靶向通用肿瘤抗原端粒酶逆转录酶(TERT),可精准诱导产生特异性Vx-001/TERT572 CD8⁺细胞毒性T细胞,且这一核心免疫反应与晚期/转移性非小细胞肺癌(NSCLC)患者的总生存期(OS)改善密切相关。
-
2025-12-23 10:56
2025压轴惊喜!四大国产细胞与基因治疗(CGT疗法)临床试验扎堆获批,横扫胰腺癌、肺癌、胃癌等,ORR超88%


2025年11月24日~12月14日期间,根据中国国家药监局药品审评中心(CDE)官网及公开资料统计,超65款1类创新药迎来关键进展,包括拟纳入突破性治疗品种、IND获批临床默示许可及IND申请获受理等情形,覆盖免疫细胞疗法(含CAR-T、TIL)、基因疗法、mRNA疫苗、DC疫苗及双抗类药物等前沿热门疗法。
-
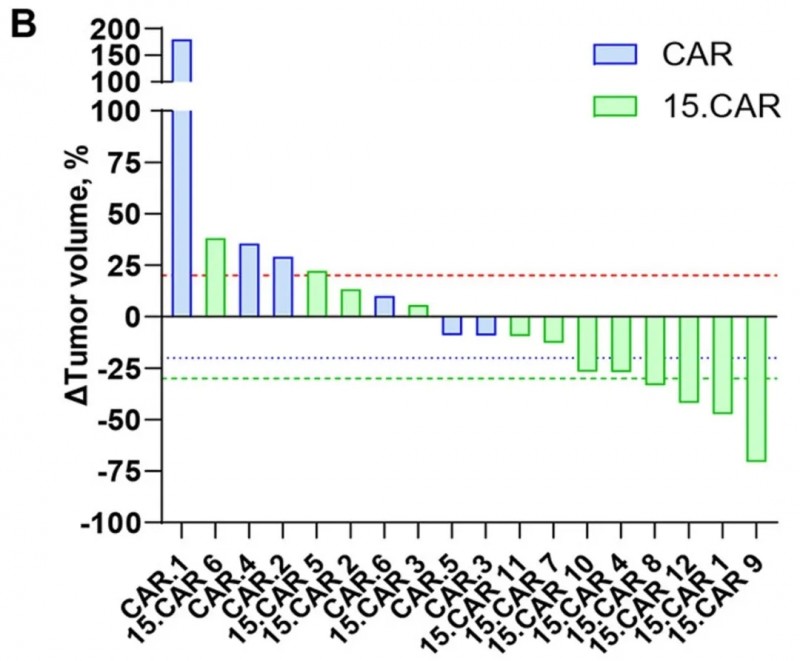
2025-12-19 11:54结直肠癌细胞治疗
抗复发添重磅方案,DC疫苗治疗结肠癌肝转移,帮患者中位无病生存提升超2倍不仅复发率显著更低、复发时间明显推迟,充分证实了该DC疫苗在降低结肠癌肝转移复发风险中的积极作用。