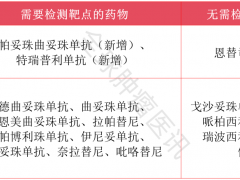
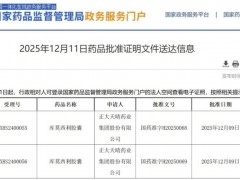
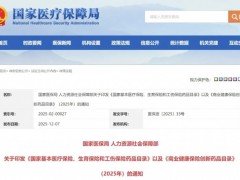
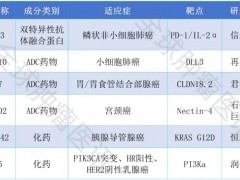
由Jung-Mo Ahn设计的化合物ERX-11, 能够显着地选择性地破坏许多共同调节因子与乳腺癌细胞(包括抗癌细胞)中雌激素受体的相互作用。结果就是阻止了癌症增殖和增加癌细胞死亡。
信誉:达拉斯德克萨斯大学的化学与生物化学副教授Jung-Mo Ahn博士设计了一种小分子, 帮助那些因为治疗而不能再工作的乳腺癌患者。
在最近发表在《eLife》杂志上的一篇论文中,Jung-Mo Ahn和他的同事们描述了他们设计这种分子的方法,以及实验证明了他们在治疗乳腺癌细胞的隔离性和动物模型中进展的有效性。
根据国家癌症研究所的资料,约80%女性的乳腺癌是基于雌激素的增长。这些患者乳腺癌细胞会含有称为雌激素受体(ER)的蛋白质,会与激素结合并促进癌症的生长。
对于这些ER阳性患者,治疗方案通常两选其一:抑制人体雌激素产生的药物方案,或与雌激素受体结合并阻断激素附着的药物。
然而,在一些患者中,乳腺癌对雌激素阻断疗法有抗药性。当乳腺癌细胞中的雌激素受体发生突变并改变形状时,这种情况就发生了,没有留下任何药物附着的地方。不管有没有基因突变,受体仍然需要在细胞中吸收其他的蛋白质,称为联合调控器,促进肿瘤生长。
Ahn说:“在雌激素结合后,雌激素受体与其他蛋白质如共同调节因子相互作用以刺激癌细胞生长。 “阻止这些共同监管者(雌激素受体与其他蛋白质如共同调节因子的相互作用)是一种新的行为模式,能突破治疗的屏障。”
Putting the Brakes on Cancer
把刹车器放在癌症身上
由Ahn研发的ERX-11化合物在乳腺癌细胞(包括治疗抗性癌细胞)中能显著性并选择性地破坏了许多共同调节因子与雌激素受体的相互作用。最后结果是明确阻止了癌症增殖和增加癌细胞死亡。
Ahn近十年来一直在研究靶向蛋白质 - 蛋白质相互作用的小分子,他们使用基于结构的合理设计方法开发了ERX-11。 他的研究小组详细研究了与雌激素受体相关的表面上关键的共同调节因子的化学结构。 然后,他们设计了一个小分子“模板”,这个模板就像一个绷带一样覆盖在共同调节器所在的受体区域。
“基本上,我们正在寻找一个特定的点,让这些蛋白质和受体握手,”Ahn说。 “我们不是试图重现整个大的共同调节蛋白,只是与受体相互作用的小表面,即使受体发生变异,这些小表面仍然具有活性。
合理的药物设计:简化的方法
为了达到ERX-11的设计,Ahn的研究小组进行了计算机模拟,将该领域缩小到他们预测可以工作的少数分子。 Ahn说在他的实验室里包括研究科学家Tae-Kyung Lee博士和化学研究生Bikash Manandhar,在他们发现“一击之前”只合成了一些候选化合物。
Ahn说:“合理设计方法的优势在于,我们不是从数以千计的化合物开始,而是为了更有效性筛选它们。 “生物学和化学都涉及药物发现,而我们的化学专业知识是精简这一过程的关键。”Ahn的研究小组之前使用了合理的药物设计方法来开发一种治疗前列腺癌药物。
为了测试ERX-11分子,Ahn会与合作者一起研究,包括综合癌症中心的泌尿学Ganesh Raj博士UT西南医学中心的药理学教授Harold C. Simmons, 以及在圣安东尼奥的UT健康科学中心的产科学教授Ratna Vadlamudi博士
Ahn说:“由于其独特的设计,ERX-11与目前在临床试验中使用的其他化合物相比,操作方式非常不同,为治疗乳腺癌提供了一种潜在的替代方法。 “最终我们也许能够开发类似于ERX-11的分子来治疗其他类型的癌症。”
Ahn和他的同事们继续改进ERX-11并正在评估,而Ahn希望下一代化合物更加有效果。他说:“这种分子的另一个优点是合成起来并不困难,因此将其作为大量用于临床试验的药物可行的