9年无瘤+99%癌标大降,PRAME TCR-T细胞疗法申报临床,现可惠及肝癌、肠癌、宫颈癌等
据“BioSpace”2025年11月18日报道,新一代靶向PRAME的增强型TCR-T疗法TK-6302已提交临床试验申请(CTA),拟启动I期ATLAS试验,用于治疗鳞状非小细胞肺癌、卵巢癌等存在高度未满足医疗需求的实体瘤。
PRAME作为已验证的肿瘤特异性靶点,在上述实体瘤中均有表达,此次CTA提交意义重大——其临床前数据证实,TK-6302不仅具备同类最佳抗肿瘤疗效,更能增强T细胞活性与持久性、有效突破肿瘤免疫屏障。据悉,CTA获批后,该试验计划于2026年正式启动,有望为相关患者带来深度且持久的治疗反应。此外,多款TCR-T疗法已在肝癌、肉瘤等实体瘤领域斩获突破性进展,共同为实体瘤免疫治疗开辟全新赛道,点亮更多患者的希望!
▲截图源自“BioSpace”
靶向PRAME再添猛将:TK-6302凭差异化优势,打破实体瘤治疗桎梏
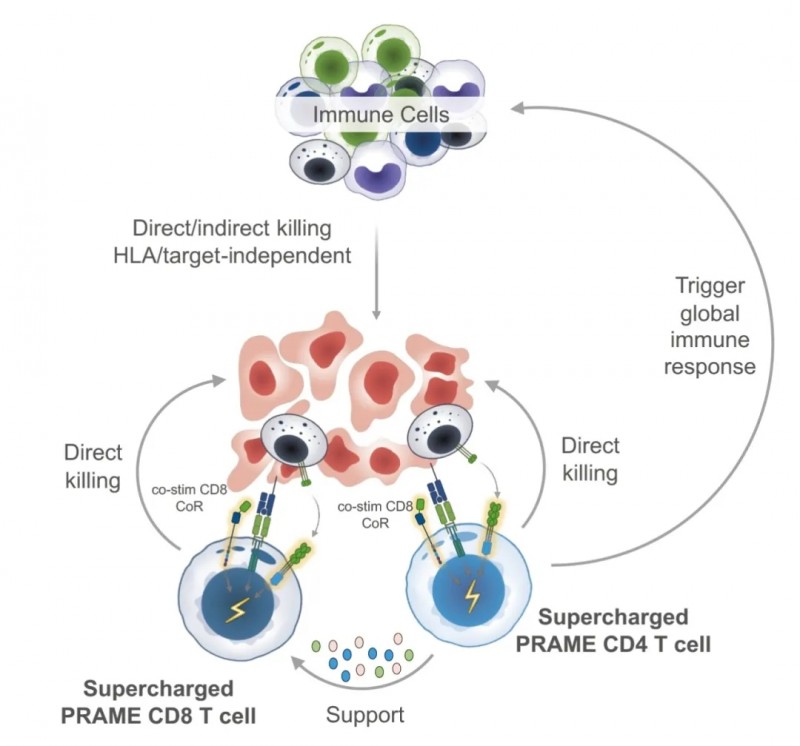
TK-6302是一款靶向PRAME的增强型TCR-T疗法,2025年癌症免疫治疗学会(SITC)年会上,摘要329海报通过临床前研究证实其抗肿瘤活性、多功能性、T细胞适应性及安全性,凭借三大核心创新技术形成差异化优势:①高亲和力TCR强化T细胞毒性;②嵌合CD8共受体(共刺激CD8CoR)结合CD4T细胞并提供共刺激信号,提升T细胞活性与持久性;③FAS-TNFR检查点转换器在淋巴结激活,增强T细胞植入能力并抵御肿瘤微环境中FAS-L诱导的凋亡,提高存活率。
临床前数据显示,TK-6302相较于同类疗法展现一流抗肿瘤疗效与T细胞活性,性能稳定。其采用非病毒基因编辑工艺提升TCR表达,已实现临床级大规模生产,为后续试验奠定坚实基础,我们对ATLASI期临床试验充满信心。下图为三维球体肿瘤模型示意图,展示TK-6302在多细胞肿瘤球体连续挑战下的强大持久抗肿瘤活性。
▲图源“T-knife”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
关于TCR-T疗法:
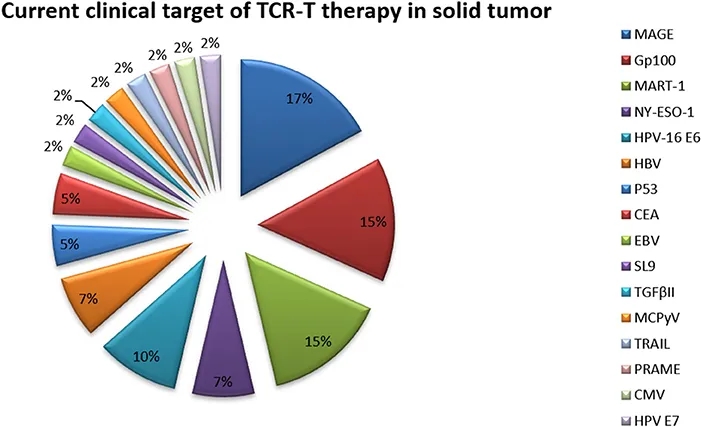
TCR-T细胞疗法(T细胞受体工程化T细胞疗法)通过基因工程技术,将抗原特异性TCR基因序列(α和β链)导入T细胞,使其可精准识别肿瘤抗原(涵盖细胞膜表面及细胞内来源的肿瘤特异性抗原)并杀伤癌细胞。得益于TCR能靶向大多数肿瘤特异性抗原(尤其是胞内抗原),目前已有多项TCR-T技术进入实体瘤临床试验阶段,实体瘤中TCR-T疗法的当前临床靶点(ClinicalTrials.gov)(详见下图)。
▲图源“frontiers”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
做了基因检测的病友可以拿出报告看看,一旦存在EGFR突变,可联系医学部,初步评估是否有机会接受国内新药治疗,看不懂的病友也可致电医学部解读报告。
超2年无进展+66.7%疾病控制率,SCG101让乙肝相关肝癌患者告别"无药可选"
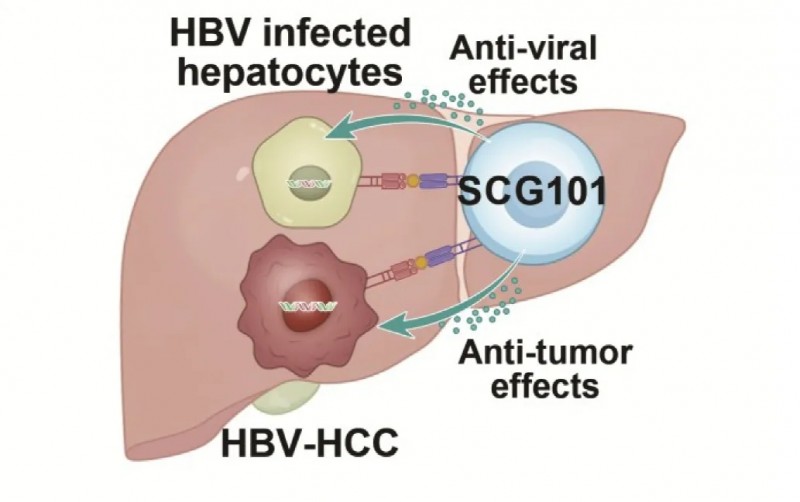
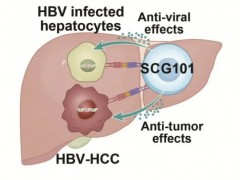
肝细胞癌(HCC)约占所有原发性肝癌的75%-85%,SCG101是一款自体T细胞疗法,通过稳定表达天然高亲和力T细胞受体,专门靶向乙型肝炎病毒(HBV)。《肝病学》杂志报道了一项针对HBV相关HCC的临床研究(NCT05339321)。
▲图源“BMJ”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
该研究共纳入6例HLA-A*02:01阳性、肝功能稳定(Child-PughA级)、慢性乙型肝炎(CHB)处于非活动期的晚期HBV相关HCC成人患者。受试者中位年龄46.0岁,平均确诊HCC为3.1年(范围1.2-5.7年),其中4例合并肝硬化;入组前均接受过酪氨酸激酶抑制剂(TKI)治疗,4例曾接受免疫检查点抑制剂(ICI)治疗,且均经1-3线全身治疗失败。患者在淋巴清除3天后,接受SCG101 TCR-T细胞单药输注治疗。
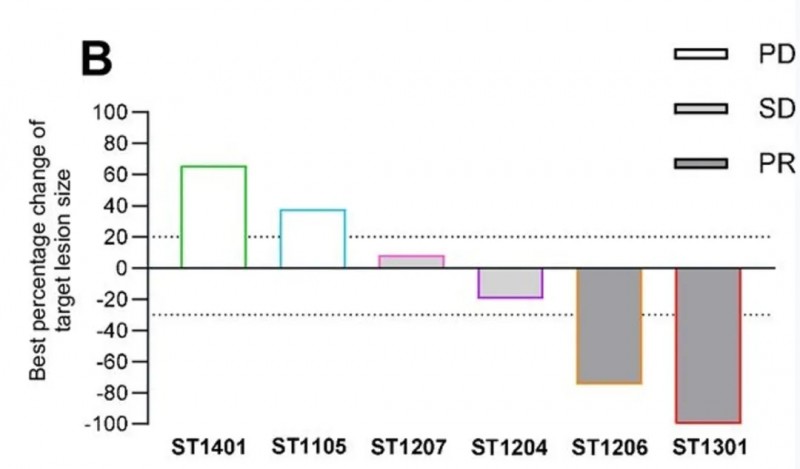
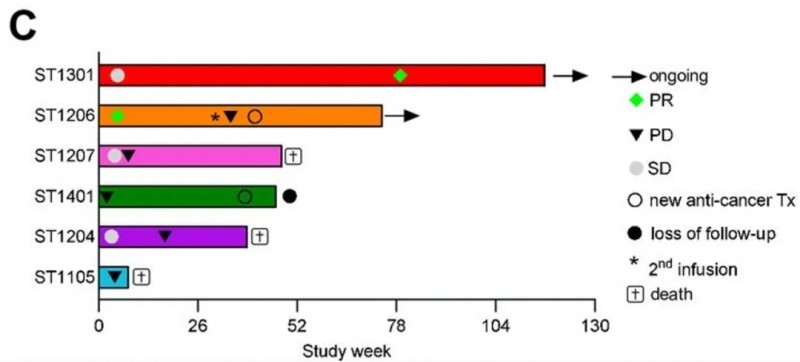
结果显示:根据改良实体瘤疗效评价标准(mRECIST),6例患者中有3例实现肿瘤缩小,靶病灶最佳缩小百分比分别为-19.5%、-74.6%、-100%:其中1例达完全缓解(CR),无进展生存期(PFS)长达27个月;2例达部分缓解(PR),缓解持续时间分别为8.0个月和≥9.5个月(详见下图C),另有2例患者病情稳定(详见下图B),研究客观缓解率(ORR)为33.3%,疾病控制率(DCR)为66.7%。
▲图源“BMJ”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
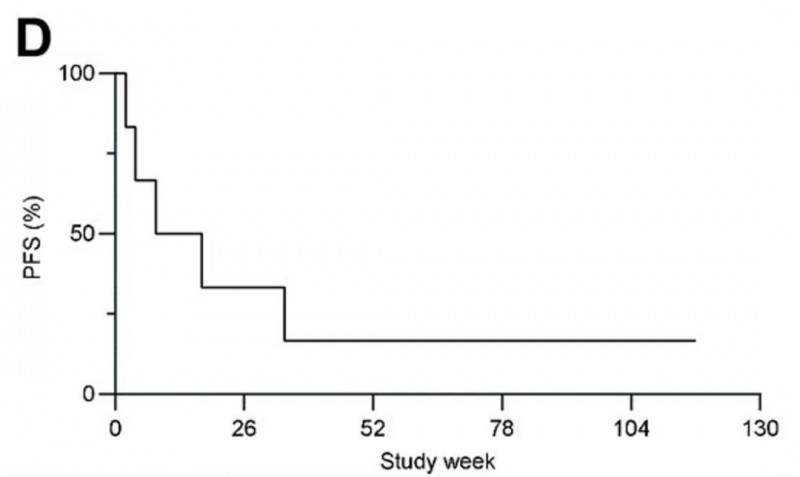
全组中位无进展生存期(PFS)为12.8周,其中1例患者在数据截止前超2年仍保持无进展状态(含非靶病灶,详见下图D);中位随访10.9个月时,2例患者输注SCG101后存活超2年。值得关注的是,ST1301患者的靶病灶位于肺部(靶肽存在情况不明),输注后18个月,该病灶在初期轻微缩小后显著退缩,同时检测到SCG 101T细胞重新出现。
▲图源“BMJ”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
综上,SCG101单药治疗HBV相关HCC患者,既展现出显著的抗肿瘤活性(可延缓应答者疾病进展),又具备明确的抗病毒效果(降低HBsAg水平),且安全性良好,不良反应可通过支持治疗有效控制,为经多线治疗失败的HBV相关HCC患者提供了全新治疗选择。
CEA靶向TCR-T疗法让多线失败结直肠癌绝境逢生,病灶缩小49%+癌标CEA暴跌74%–99%
癌胚抗原(CEA)是一种180kDa的糖蛋白,隶属于免疫球蛋白超家族,作为肿瘤相关蛋白,其在结直肠腺癌等多种上皮癌中存在过度表达,同时也可见于胃肠道多种正常上皮细胞(以结肠隐窝上三分之一处的高度分化上皮细胞表达最为显著)。目前,靶向CEA的疫苗与抗体已成为癌症免疫治疗的重要探索方向。
基于这一靶点,研究人员开发了针对转移性结直肠癌的自体T细胞疗法——通过基因工程改造T细胞,使其表达可特异性识别CEA的高亲和力T细胞受体(TCR)。
《Molecular Therapy》首次报道了该过继性T细胞疗法在转移性结直肠癌中的客观缓解案例,验证了HLA转基因小鼠来源的人肿瘤相关抗原特异性TCR的临床应用价值,同时也揭示了少量高亲和力T细胞的强效杀伤作用,以及CEA作为免疫治疗靶点的局限性。值得关注的是,这是该类细胞转移疗法首次应用于对所有标准治疗无效的常见上皮癌(如转移性结直肠癌)。该研究共纳入3例对标准治疗无效的转移性结直肠癌患者,接受了经逆转录病毒转导、表达上述TCR的自体T细胞输注。
结果显示:所有患者血清CEA水平均显著下降74%–99%(治疗前CEA水平为226–865µg/L)。
其中,两例典型患者的情况值得广泛关注:患者1治疗后2个月肺转移瘤缩小17%。
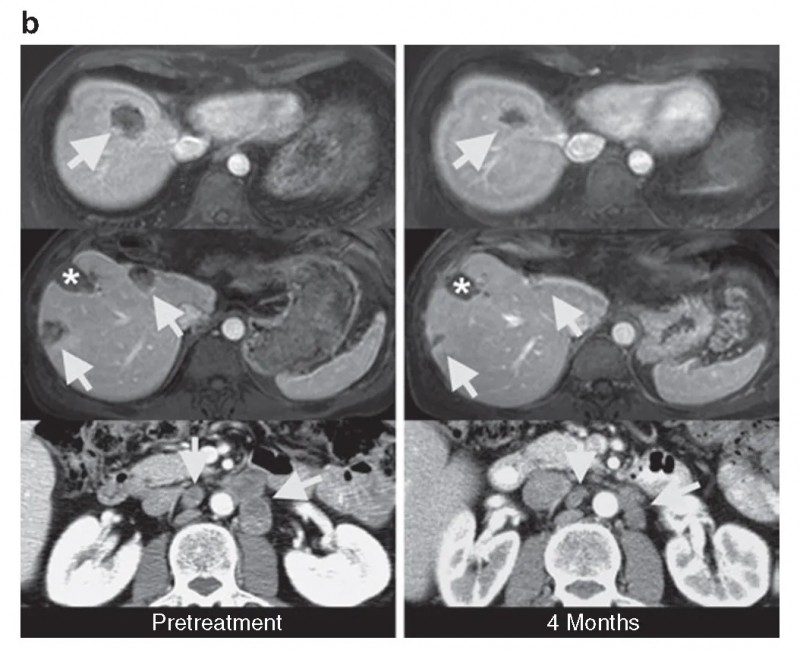
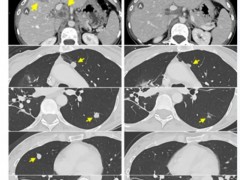
患者3在治疗3个月时,肝、肺及腹主动脉旁淋巴结转移瘤按实体瘤疗效评价标准(RECIST)缩小34%,4个月时缩小幅度达49%(详见下图),达到RECIST确认的部分缓解(PR)。
▼患者3在治疗前、治疗后4个月的计算机断层扫描(CT)图像
▲图源“Mol Ther”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:
①箭头表示:结直肠癌转移灶的位置;
②星号表示:先前接受过射频消融(RFA)治疗的肝转移灶部位的肝脏缺损。
CEA CAR-T疗法暴击CEA阳性结直肠癌,70%实现病情稳定,一例病灶显著缩小
除TCR-T疗法外,中国科学家针对CEA靶点研发的CEA CAR-T疗法,已用于治疗CEA阳性结直肠癌、肺癌等实体瘤。其治疗CEA阳性结直肠癌(CRC)的I期临床试验(NCT02349724)数据同样振奋:10例既往治疗进展的患者中,70%(7/10)在治疗后达病情稳定(SD),肿瘤直径仅轻微变化,其中2例稳定状态持续超30周(7.5个月)。
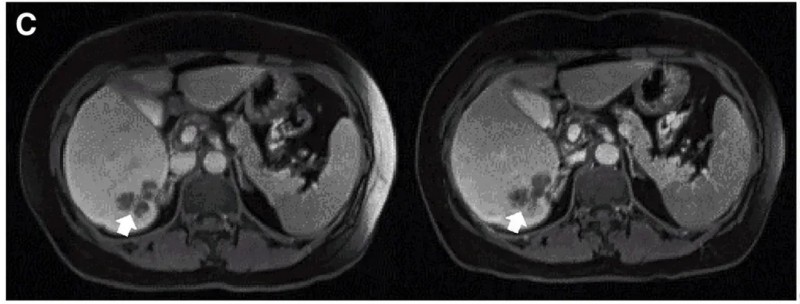
值得一提的是,典型病例P10在接受DL4剂量CEA CAR-T治疗后,MRI检查证实肝内一处病灶明显缩小(详见下图)。
▼P10患者在CAR-T治疗前(左图)、治疗4周后(右图)的MRI对比
▲图源“Molecular Therapy”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
MASCT疗法让晚期宫颈癌患者重掌生命主动权,实现超9年无癌生存
世界权威期刊《Nature》子刊曾报道一则振奋人心的案例:一名人乳头瘤病毒(HPV)阳性转移性宫颈鳞状细胞癌患者,经MASCT(多抗原刺激细胞疗法)治疗后,实现无瘤生存超9年!
该患者诊断为人乳头瘤病毒(HPV)阳性转移性宫颈鳞状细胞癌,确诊时已伴随右侧骶髂关节转移病灶,此前虽接受过根治性切除术及辅助化放疗,但病情仍持续进展。随后患者入组接受多次MASCT治疗——这是一种融合自体T细胞与树突状细胞的免疫疗法。
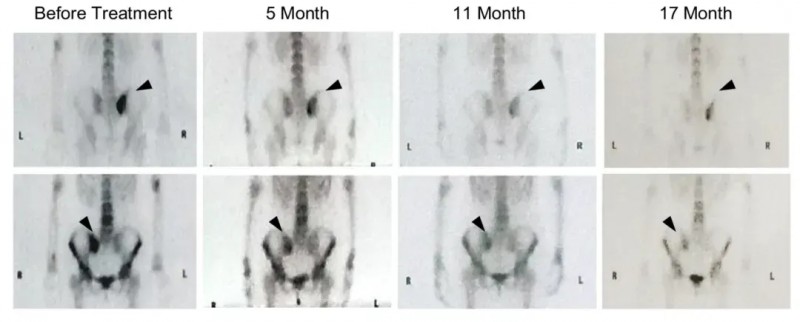
治疗结果十分亮眼:患者对该疗法产生强烈免疫应答,不仅转移性骨肿瘤得到有效抑制(详见下图),更达成了超9年的无瘤生存,为晚期宫颈癌治疗带来重磅希望!
▼该患者治疗前后发射计算机断层扫描(ECT)图像对比
▲图源“nature communications”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
小编寄语
TCR-T疗法开创了一种抗癌和抗病毒“双杀”的新型治疗模式,近年来,研究人员也在尝试将TCR-T疗法,用于治疗与病毒感染相关的实体瘤上,比如乙肝病毒相关肝细胞癌、人乳头瘤病毒(HPV)感染相关的宫颈癌等方面。小编也期望未来可以迎来更多抗癌新疗法获批上市的好消息,让更多的实体瘤患者实现长期带瘤生存的美好愿景!
目前TCR-T疗法的正在招募鼻咽癌、乙型肝炎病毒相关肝细胞癌、晚期葡萄膜黑色素瘤、妇科恶性肿瘤(卵巢癌、子宫内膜癌)、血液系统恶性肿瘤等,如果您也想寻求TCR-T、CAR-T、TILs等新兴抗癌疗法的帮助,可以将近期病理检查结果、治疗经历等资料,提交至医学部,进行初步评估!
参考资料
[1]Zhao L,et al.Engineered T cell therapy for cancer in the clinic[J]. Frontiers in immunology, 2019, 10: 2250.
https://www.frontiersin.org/journals/immunology/articles/10.3389/fimmu.2019.02250/full
[2]Wu X,et al.Clinical results of an HBV-specific T-cell receptor-T-cell therapy (SCG101) in patients with HBV-related hepatocellular carcinoma treated in an investigator-initiated, interventional trial[J]. Gut, 2025.
https://gut.bmj.com/content/early/2025/08/21/gutjnl-2025-335456
[3]Parkhurst MR,et al.T cells targeting carcinoembryonic antigen can mediate regression of metastatic colorectal cancer but induce severe transient colitis. Mol Ther. 2011 Mar;19(3):620-6.
https://www.cell.com/molecular-therapy-family/molecular-therapy/fulltext/S1525-0016(16)30411-7?_returnURL=https%3A%2F%2Flinkinghub.elsevier.com%2Fretrieve%2Fpii%2FS1525001616304117%3Fshowall%3Dtrue
[4]Long J,et al.HLA-class II restricted TCR targeting human papillomavirus type 18 E7 induces solid tumor remission in mice[J]. Nature Communications,2024,15(1):1-13.
https://www.nature.com/articles/s41467-024-46558-4
[5]https://www.biospace.com/press-releases/t-knife-therapeutics-files-clinical-trial-application-for-phase-1-atlas-trial-for-tk-6302-a-supercharged-prame-targeted-t-cell-receptor-therapy