国研首款BCMA CAR-T伊基奥仑赛(福可苏)出海韩国,有效率达96%,2年生存率逼近80%
据驯鹿生物官网报道,2025年7月9日,韩国食品药品安全部(MFDS)授予我国驯鹿生物自主研发的靶向BCMA CAR-T产品伊基奥仑赛注射液(Fucaso)孤儿药资格(ODD),适用于经至少三线治疗进展的复发/难治性多发性骨髓瘤成人患者(需用过蛋白酶体抑制剂及免疫调节剂)。
韩国鼓励“境外有药、境内无药”孤儿药进口,此次认定将加速该药在韩注册审批,助力当地患者早日用上创新疗法。这是其继5月获沙特ODD后又一国际监管突破,标志着我国自主研发的CAR-T疗法临床价值获国际认可。国研CAR-T正以“多国并行、区域协同”战略推进全球获批,用创新力量跨越国界,为全球患者点亮生命希望!
不止国内!全球首款全人源BCMA CAR-T伊基奥仑赛注射液三国获批/受理:从中国首发到全球开花
伊基奥仑赛注射液(Equecabtagene Autoleucel Injection,eque-cel,福可苏®,Fucaso)由驯鹿生物与信达生物联合研发,是全球首款全人源B细胞成熟抗原(BCMA)靶向CAR-T细胞疗法。其核心优势在于通过全人源抗体设计降低免疫原性,为复发/难治性多发性骨髓瘤(R/RMM)患者提供精准治疗选择。
2023年6月30日,该药获中国国家药品监督管理局(NMPA)批准用于R/RMM治疗,成为中国首款获批的BCMACAR-T疗法,也是全球首款全人源BCMA靶向CAR-T疗法,填补了该领域临床空白。
2025年1月29日,新加坡卫生科学局(HSA)受理其新药上市申请,适用于接受过≥3种既往治疗的R/RMM患者,标志着“出海”首站落地。同年5月,沙特阿拉伯食品药品监督管理局(SFDA)授予其孤儿药资格,用于经至少三线治疗(含蛋白酶体抑制剂及免疫调节剂)失败的成人R/RMM患者,加速中东地区临床可及性。2025年7月9日,该药再获韩国食品药品安全部(MFDS)孤儿药资格,我国自研CAR-T国际化进程再下一城!
伊基奥仑赛长期数据震撼公布:96%多发性骨髓瘤有效,CR患者2年生存率高达78.9%
2025年5月16日,《转化医学杂志》发表了伊基奥仑赛的长期临床疗效数据,该研究纳入65例复发/难治性多发性骨髓瘤(r/r MM)患者,中位年龄为56岁,范围:51-61岁),中位随访39.6个月(范围:1.0-69.3个月),所有患者均曾接受过蛋白酶体抑制剂(PI)和/或免疫调节药物(IMiD)治疗。
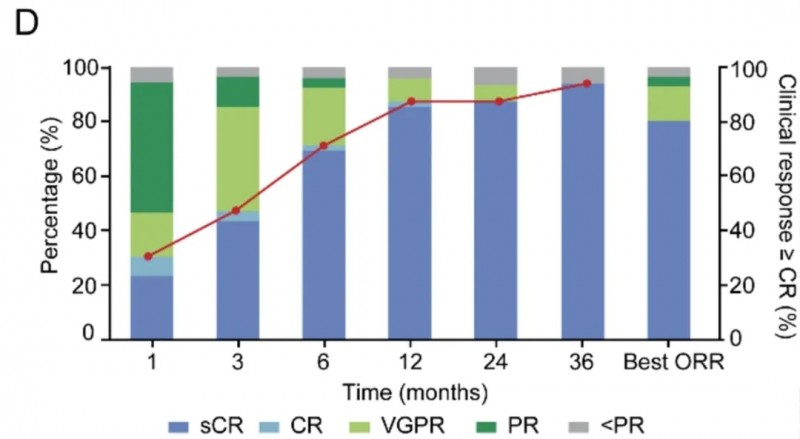
结果显示:总有效率(ORR)达96.4%,其中80.4%(45例)患者达到完全缓解(CR)或严格完全缓解(sCR)(详见下图D),96.4%(54/56例)的患者实现微小残留病阴性(MRD-)。
▲图源“JTM”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
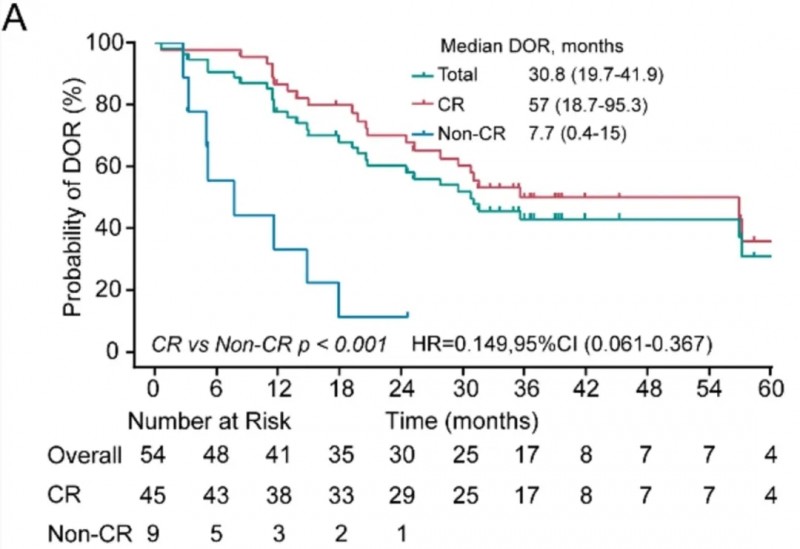
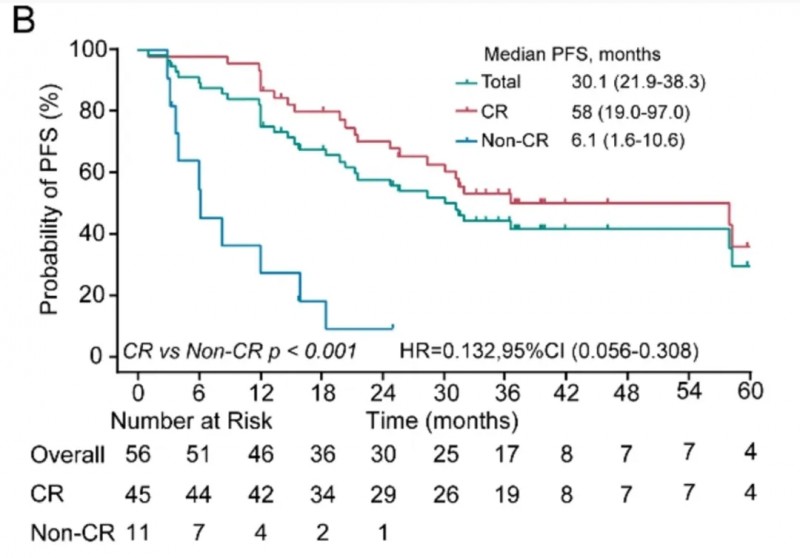
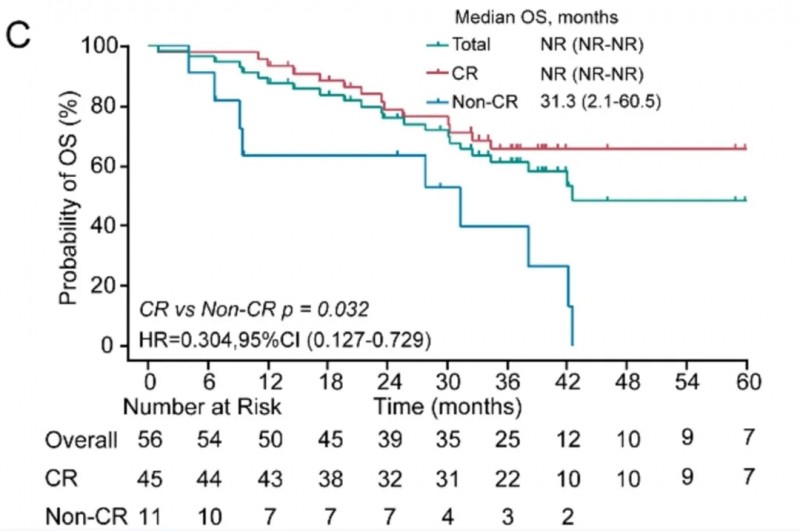
此外,中位缓解持续时间(DOR)为30.8个月(详见下图A),中位无进展生存期(PFS)长达30.1个月(详见下图B),总生存期(OS)未达到(NR)(详见下图C)。
▲图源“JTM”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
值得关注的是,CAR-T细胞持续存在≥6个月且MRD-的患者预后更佳,维持MRD阴性达12、24、36个月者,中位PFS分别为58个月、64个月、未达到(NR)。此外,45名达到CR或严格完全缓解(sCR)的患者,其2年无进展生存(PFS)率为70.0%、总生存(OS)率为78.9%,显著高于未达到CR的患者(p <0.05),提示早期干预促进深度缓解可显著改善生存结局。
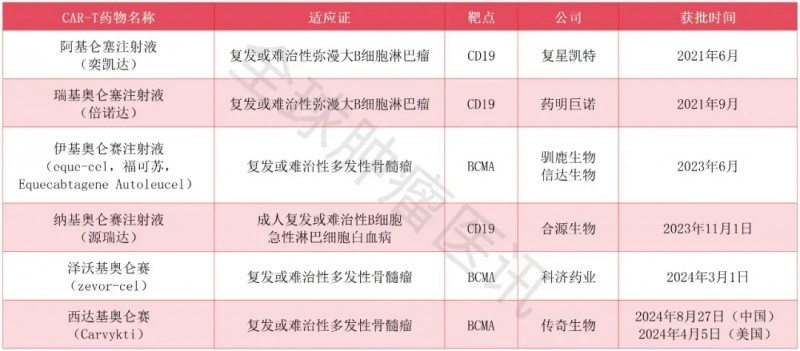
中国已获批上市的六大CAR-T产品
小编寄语
近年来,随着多款CAR-T疗法相继获批上市,我国CAR-T的研发领域也迎来了属于自己的高光时刻!目前我国已有20多家制药巨头,如驯鹿医疗、传奇生物、复星凯特、科济生物等纷纷布局CAR-T的研发,力争在精确调控、新靶点设计、通用CAR-T细胞等方面,取得突破性进展。这两年,更是有多款CAR-T产品登上国际舞台。全球肿瘤医学部小编也期望随着越来越多明星靶点的涌现、技术的不断革新,CAR-T疗法可以早日突破价格和癌症治疗的瓶颈,造福更多的癌症晚期患者,实现长期带瘤生存、降低复发风险的美好愿景!
如果您对目前的治疗方案不满意,或想寻求CAR-T、CAR-NK、TCR-T、TIL疗法等国内外抗癌新技术的帮助,可将治疗经历、近期影像学检查、病理检查报告等资料汇总后,提交至医学部,进行初步评估,或申请国内外抗癌专家会诊。
参考资料
[1]An N, et al. Key predictors of long-term outcomes in BCMA-targeted CAR-T therapy for relapsed/refractory multiple myeloma[J]. Journal of Translational Medicine, 2025, 23(1): 552.
https://translational medicine.biomedcentral.com/articles/10.1186/s12967-025-06543-x