全球首创门控CAR-NK细胞疗法SENTI-202获孤儿药认证!为白血病、肠癌、胰腺癌、脑瘤等筑起免疫防线
2025年6月18日,美国食品药品监督管理局(FDA)授予新型CAR-NK疗法SENTI-202孤儿药资格,用于治疗包括急性髓系白血病(AML)在内的复发/难治性血液系统恶性肿瘤。
复发/难治性AML存在显著未满足的治疗需求,患者平均生存期仅5.3个月,迫切需要新的治疗方法。SENTI-202作为全球首创的“现成型”逻辑门控CAR-NK细胞疗法,通过靶向CD33和/或FLT3双标志物,可选择性清除表达上述抗原的AML及骨髓增生异常综合征(MDS)细胞,同时保护健康骨髓组织。目前该疗法正在开展Ⅰ期临床试验(NCT06325748),其孤儿药资格的获得,验证了“克服肿瘤异质性+保护正常细胞”的创新机制,也凸显了临床对高效AML疗法的迫切期待。
值得关注的是,除SENTI-202外,国内外多家机构正围绕肺癌、结直肠癌、淋巴瘤、胰腺癌等多癌种开展CAR-NK疗法研发,全球范围内的临床研究已呈燎原之势。随着这类创新疗法从实验室走向临床的步伐加快,CAR-NK技术将为更多癌症患者点燃生命的希望!
▲截图源自“BioSpace”
从"无法切除"到"肿瘤停滞生长5个月":Robo1 CAR-NK细胞首现胰腺癌肝转移长期控制奇迹
胰腺导管腺癌(PDAC)是胰腺癌中最常见的类型,恶性程度极高,5年生存率极低。尽管转移性PDAC的全身化疗进展已提升缓解率与疗效,但多数患者因肿瘤无法手术切除,中位总生存期仍不足1年,临床治疗面临严峻挑战。
自然杀伤(NK)细胞作为人体免疫防御的重要效应细胞,在临床中被视为CAR-T细胞疗法安全有效的替代策略。而CAR-NK细胞(CAR-NK)是利用基因工程技术,给NK细胞安装一个名为“CAR”(一种人工修饰的融合蛋白)的“弹头”,使其不仅能保留抗癌斗士NK细胞的原有功能,同时还可将打击目标精准锁定在特定的抗原蛋白上,让狡猾的癌细胞“无处躲藏”。
《癌症研究与治疗学杂志》曾报道一则经典案例:一名46岁男性确诊PDAC肝转移(T4N1M1,IV期),肿瘤组织穿刺活检证实Robo1阳性。因肿瘤无法手术切除且患者拒绝化疗,遂入组接受Robo1特异性CAR-NK细胞治疗,该疗法已在胰腺癌的临床前研究中展现出显著协同抗肿瘤作用。
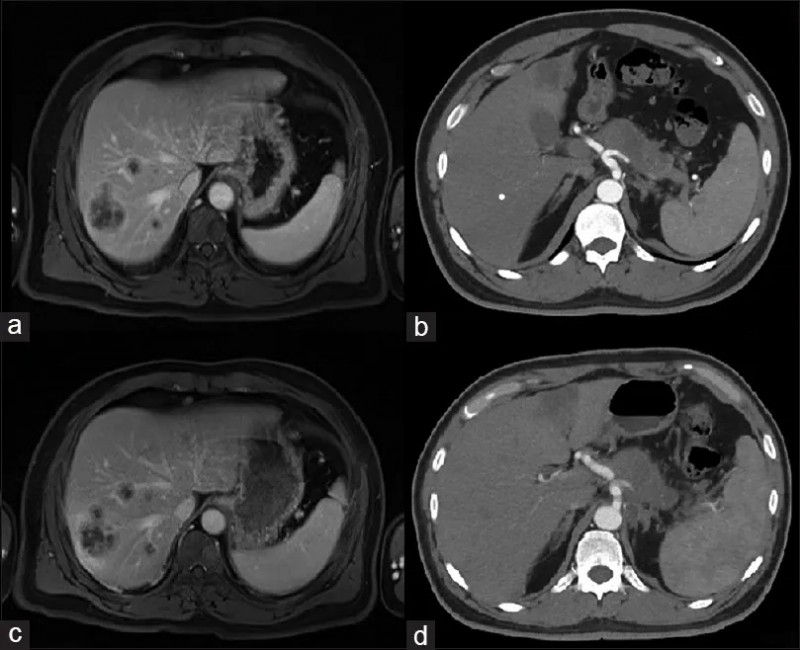
结果显示:治疗前,影像学检查显示胰腺存在6cm×2.5cm×3cm占位伴淋巴结浸润,肝脏多发高代谢转移灶(最大直径3.5cm,详见下图a、b)。Robo1 CAR-NK细胞治疗5个月内,胰腺原发病灶及肝转移灶得到有效控制[详见下图c、d]。维持治疗期间,患者卡氏功能评分稳定,Child-Pugh肝功能分级无明显变化,总生存期(OS)达8个月。该案例证实,Robo1 CAR-NK细胞疗法为PDAC肝转移患者提供了新的治疗思路,其精准靶向Robo1抗原的特性或成为突破PDAC治疗瓶颈的关键方向。
▲图源“J Cancer Res Ther”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
HER2靶向CAR-NK疗法首次在胶质母细胞瘤中实现超2年长期生存
在一项针对复发性HER2阳性胶质母细胞瘤(GB)患者的I期首次人体临床试验中,研究人员探索了一种CAR-NK细胞疗法——该疗法采用永久性人类NK细胞系NK-92,转导第二代靶向HER2的CAR-NK细胞。
研究共纳入9例复发性GB患者,在肿瘤复发手术期间,将剂量递增的CAR-NK细胞注射至术腔边缘。
结果显示:整个队列的中位总生存期(OS)为31周(近8个月),其中接受最高剂量治疗的2例患者分别存活至116周(29个月)、97周(≈24个月)。
▲截图源自“BTRT”
总之,该研究证实,局部应用靶向HER2的CAR-NK细胞疗法对复发性胶质母细胞瘤(GB)患者具有安全性和可行性,为这类难治性肿瘤的免疫治疗提供了新的临床证据。
3例临床实证!CAR-NK细胞逆转肠癌恶性腹水,肝转移灶代谢活性近乎清零,一例达完全缓解
《Molecular Therapy》发表的一项先导临床试验显示,针对3例化疗难治性转移性结直肠癌患者,mRNA修饰的NKG2D CAR-NK细胞疗法展现出安全有效的局部抗肿瘤潜力。
该研究采用电穿孔技术制备NKG2Dp CAR-NK细胞:患者1001接受2次自体NK细胞来源的CAR-NK输注,患者1002接受4次同种异体半相合CAR-NK细胞腹腔注射,患者1003则接受6次同种异体CAR-NK细胞肝区注射。结果显示如下:
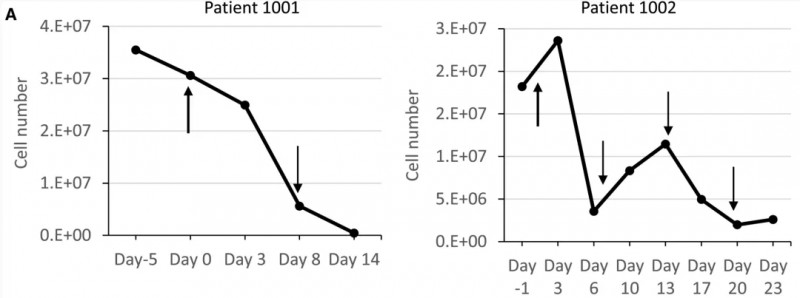
1、恶性腹水控制:患者1001与患者1002治疗后,腹水中上皮细胞粘附分子(EpCAM)阳性癌细胞数量显著减少(详见下图A),治疗结束时几乎检测不到。腹水量经CT成像证实显著减少。
▲图源“Molecular Therapy”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
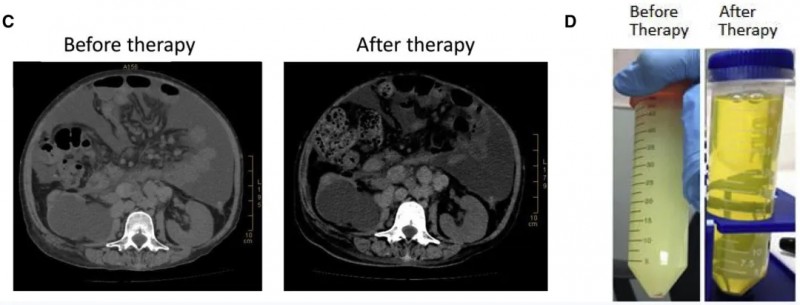
其中患者1002虽然治疗前CT扫描可见大量腹水,但在CAR-NK细胞注射后,腹水量显著减少(详见下图C)。腹水从乳白色转为澄清,腹腔病灶维持稳定(详见下图D)。
▲图源“Molecular Therapy”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
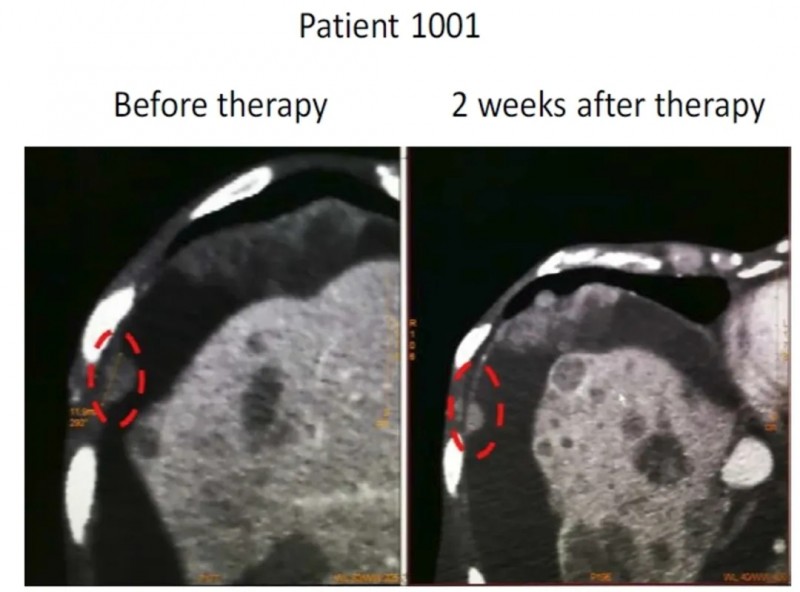
2、腹膜靶病灶控制:CT扫描结果显示,患者1001与患者1002治疗后,腹膜靶病灶均病情稳定(详见下图)。
▲图源“Molecular Therapy”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
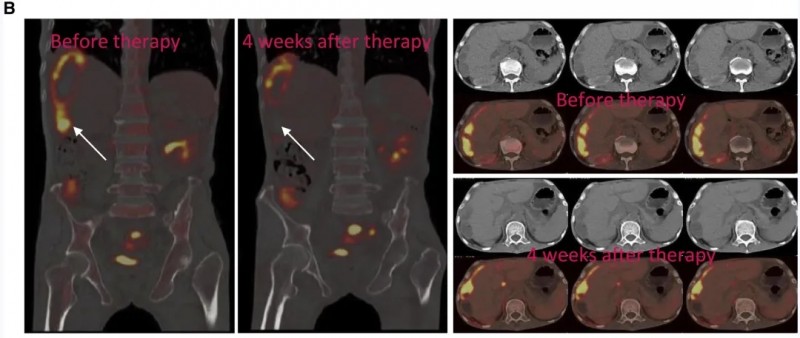
3、肝转移灶消退:患者1003接受肝区注射后,多普勒超声显示肝区肿瘤快速消退,肝肿瘤面积从66.0mm×28.5mm缩小至46.9mm×24.0mm;PET/CT扫描显示肝段VI的FDG摄取SUVmax从8.2降至0.14(详见下图),达到完全代谢缓解;组织活检证实注射部位肿瘤坏死,非注射区域仍有癌组织残留。
▲图源“Molecular Therapy”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
综上,影像引导下经皮注射CAR-NK细胞(微创可重复操作)能在体内诱导强大的局部抗肿瘤效应,为化疗难治性结直肠癌转移患者提供了新的治疗策略。
CAR-NK细胞为淋巴瘤/白血病患者筑起安全免疫防线,客观缓解率高达73%
《新英格兰医学杂志》发表的临床研究(NCT03056339)证实,源自脐带血的HLA错配抗CD19CAR-NK细胞疗法在复发/难治性CD19阳性肿瘤中展现出高效低毒的治疗潜力。
该研究纳入11例经多线治疗(中位4种疗法)的CD19阳性患者,包括5例慢性淋巴细胞白血病(CLL)、6例非霍奇金淋巴瘤(NHL),含2例弥漫大B细胞淋巴瘤、4例滤泡性淋巴瘤,中位年龄60岁,入组接受CAR-NK细胞回输治疗。
结果显示:治疗后,疗效快速显现,所有应答患者在输注后30天内即见缓解,其中73%(8/11)达到客观缓解(ORR),7例(4例淋巴瘤、3例CLL)达完全缓解(CR),1例Richter转化患者部分缓解但残留CLL病灶。且CAR-NK细胞持续扩增并在体内低水平存续至少12个月。
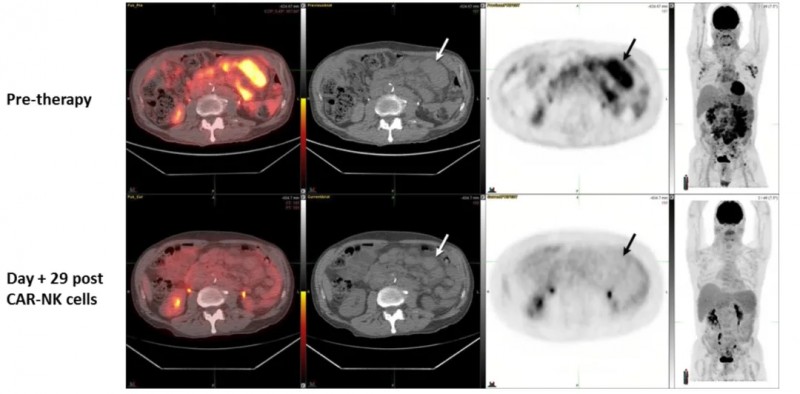
值得关注的是,1例发生Richter转化的慢性淋巴细胞白血病(CLL)患者(患者5)在输注后29天PET-CT显示,肠系膜淋巴结FDG摄取完全消失,虽伴发血细胞减少及CLL骨髓浸润,但后续经缓解后治疗实现完全缓解(CR)。影像学检查显示,治疗前可见肠系膜肿大淋巴结异常FDG摄取,治疗后病灶代谢活性消失(详见下图),证实CAR-NK细胞的精准杀伤效应。
▲图源“N Engl J Med”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
CAR-NK疗法上市在即!国内多中心启动临床
相信看了上面的数据,胰腺癌、脑瘤、血液肿瘤或其他实体瘤患者,一定燃起了新的希望!好消息是,目前我国正在开展针对CAR-NK疗法的临床研究,现已有大量患者通过抗癌新药招募中心,成功入组接受这款抗癌黑科技的治疗!
CGC729
新药简介
①药品名称:CAR-NKT 细胞注射(CGC729)。
②靶点:CD70。
③适应症:复发或转移晚期透明细胞型肾细胞癌。
招募信息
1)18-75 岁男性或女性受试者。
2)经影像学和组织学或细胞学证实至少二线及以上治疗复发或转移晚期透明细胞型肾细胞癌受试者。
3)按照 RECIST1.1 标准至少存在一个可测量病灶。
抗BCMA-CD19CAR-NK细胞
新药简介
①药品名称:抗BCMA-CD19CAR-NK细胞。
②靶点:CD19。
③适应症:复发难治性多发性骨髓瘤患者。
招募信息
1)年龄≥18岁,≤70岁的中线诊断年龄。
2)至少一种治疗疾病(PI)和一种治疗方法,至少未获得部分缓解或改善后的改善状态,或缓解症状一次治疗难治或无缓解。
3)筛选时需满足以下可测量指标的标准:血糖水平(0g/dL/M)≥21.0g/dL/M水平≥20000mg/24小时;或尿液中测量测量的多发性骨髓瘤。
申请流程
想申请抗癌新药临床试验的患者,需将近期病理报告、基因检测报告等资料汇总后,提交至网医学部,进行初步评估。
我们的专家将为您全面分析解读检测报告,预计一个工作日内电话联系推荐用药方案,并匹配适合患者入组的临床试验项目。注:我们作为国内权威的肿瘤患者服务平台,我们承诺对所有受试者的个人信息保密,并保证在整个过程中,遵循国家临床研究相关的法律法规。
小编寄语
当前,CAR-NK的研究证据有力地表明,NK细胞在攻克目标癌症方面,兼具安全性与高效性,这无疑是肿瘤治疗领域的一抹曙光!令人振奋的是,这些正在开展的新临床试验,可能取得的重大进展,将为创新型CAR-NK疗法带来颠覆性的变革。
值得欣慰的是,目前我国也有多款关于CAR-NK细胞疗法的临床研究,正在进行中。小编也希望以NK细胞强大的抗肿瘤能力为基石的CAR-NK细胞疗法,能够早日获批上市,为血液肿瘤及实体瘤的治疗带来前所未有的突破性进展,让更多被癌症折磨的患者重燃希望!如果您对目前的治疗方案存疑,或想寻求CAR-NK细胞、NK细胞、CAR-T细胞获国内外其他抗癌新技术的帮助,可将治疗经历、近期病理及影像学检查结果等,提交至医学部,进行初步评估或了解详细的入排标准。
参考资料
[1]Li C,et al.Robo1-specific chimeric antigen receptor natural killer cell therapy for pancreatic ductal adenocarcinoma with liver linkstasis. J Cancer Res Ther. 2020;16(2):393-396.
https://journals.lww.com/cancerjournal/fulltext/2020/16020/robo1_specific_chimeric_antigen_receptor_natural.29.aspx
[2]Burger M C,et al.A phase I first-in-human trial with local application of CAR-NK cells targeting HER2 in patients with recurrent glioblastoma (CAR2BRAIN): results of the dose-escalation cohort[J]. Brain Tumor Research and Treatment, 2022, 10(Suppl).
https://btrt.org/DOIx.php?id=10.14791/btrt.2022.10.F-1135#
[3]Xiao L,et al.Adoptive transfer of NKG2D CAR mRNA-engineered natural killer cells in colorectal cancer patients[J]. Molecular Therapy, 2019, 27(6): 1114-1125.
https://www.cell.com/molecular-therapy-family/molecular-therapy/fulltext/S1525-0016(19)30097-8_returnURL=https%3A%2F%2Flinkinghub.elsevier.com%2Fretrieve%2Fpii%2FS1525001619300978%3Fshowall%3Dtrue
[4]Liu E,et al.Use of CAR-transduced natural killer cells in CD19-positive lymphoid tumors[J]. New England Journal of Medicine, 2020, 382(6): 545-553.
https://www.nejm.org/doi/10.1056/NEJMoa1910607
[5]https://www.biospace.com/press-releases/senti-bio-granted-u-s-fda-orphan-drug-designation-for-use-of-first-in-class-off-the-shelf-logic-gated-selective-cd33-or-flt3-not-emcn-car-nk-cell-therapy-senti-202-to-treat-acute-myeloid-leukemia