GCC19CART治疗肠癌多个病灶消失,40%缓解率创新高,中位总生存近2年
GCC19CART是一种自体CAR-T细胞混合物,通过慢病毒载体转导表达CD-19CAR或GCCCAR基因。对于无其他治疗方案的转移性结直肠癌(mCRC)患者,靶向GCC的CAR-T细胞疗法在安全性和耐受性方面表现良好,可带来合理临床获益。
该疗法首次实现自体CAR-T细胞转导表达实体肿瘤抗原,并依赖CD19CAR-T细胞进行扩增,相关研究数据已同步发表于《美国医学会肿瘤学杂志》。结果显示,该自体CAR-T细胞产品在经大量预处理的mCRC患者中展现出抗肿瘤活性,为晚期实体瘤的免疫治疗带来了新的选择!这一突破不仅证实了CAR-T疗法在实体瘤领域的潜力,更让无药可治的患者看到了长生存的希望!
▲截图源自“PMC”
GCC19CART让肠癌转移灶"代谢熄灭",中位总生存近2年,两例患者肿瘤持续退缩
该研究共纳入15例中位年龄为44岁(范围:33-61岁)的转移性结直肠癌(mCRC)患者,给予GCC19CAR-T治疗。
结果显示:客观缓解率(ORR)达40%,总体临床受益率更是高达73%。其中40%(6例)的患者达到部分缓解(PR),另外5例患者的最佳反应为病情稳定(SD)。中位缓解持续时间为5.1个月(范围:2.0-8.0个月)。中位总生存期(OS)长达22.8个月(95%CI:13.4-26.1)。剂量相关性分析显示,高剂量治疗组中位无进展生存期(PFS)为6.0个月,显著优于低剂量组的1.9个月。其中,三例患者的情况值得广泛关注:
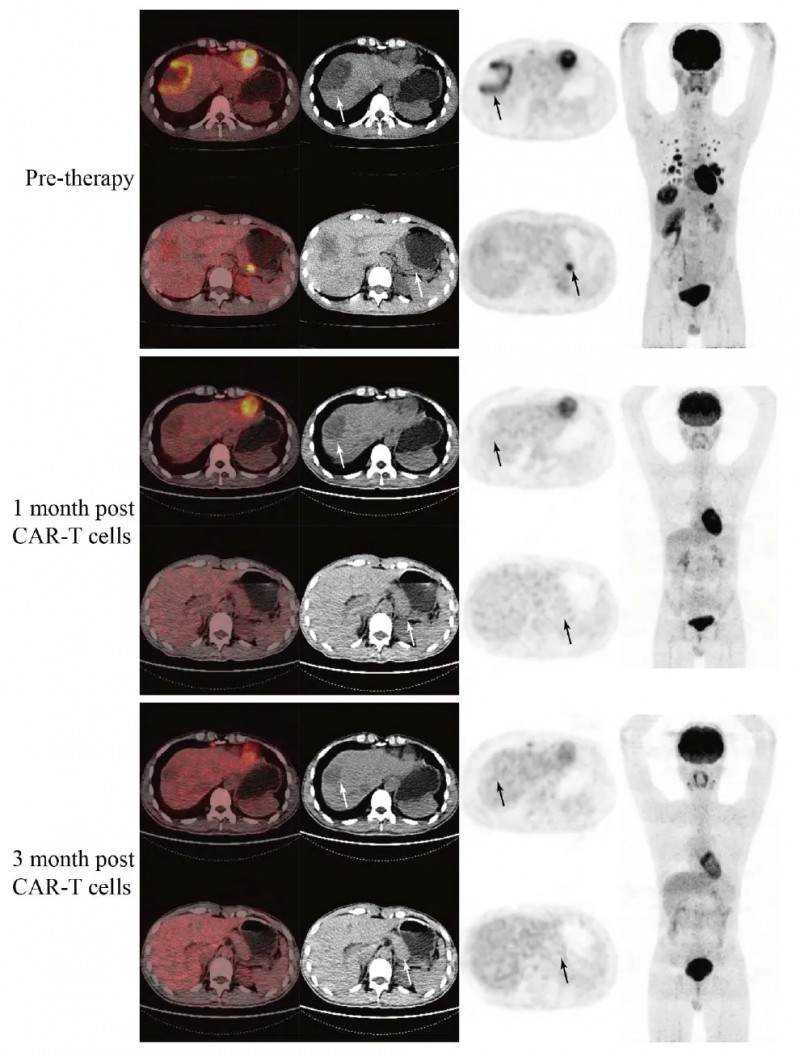
1、患者4(1×10⁶cells/kg剂量GCC19CART细胞):CT评估显示,治疗1个月后,患者肝脏及胰腺转移灶出现部分缓解(PR)。治疗3个月后,膈上/下转移灶、肝脏和胰腺的PET放射性显著降低。根据PERCIST1.0标准评估PET影像,治疗3个月后,转移灶无FDG摄取,该患者表现出部分代谢缓解。
▲图源“JAMA Oncol”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
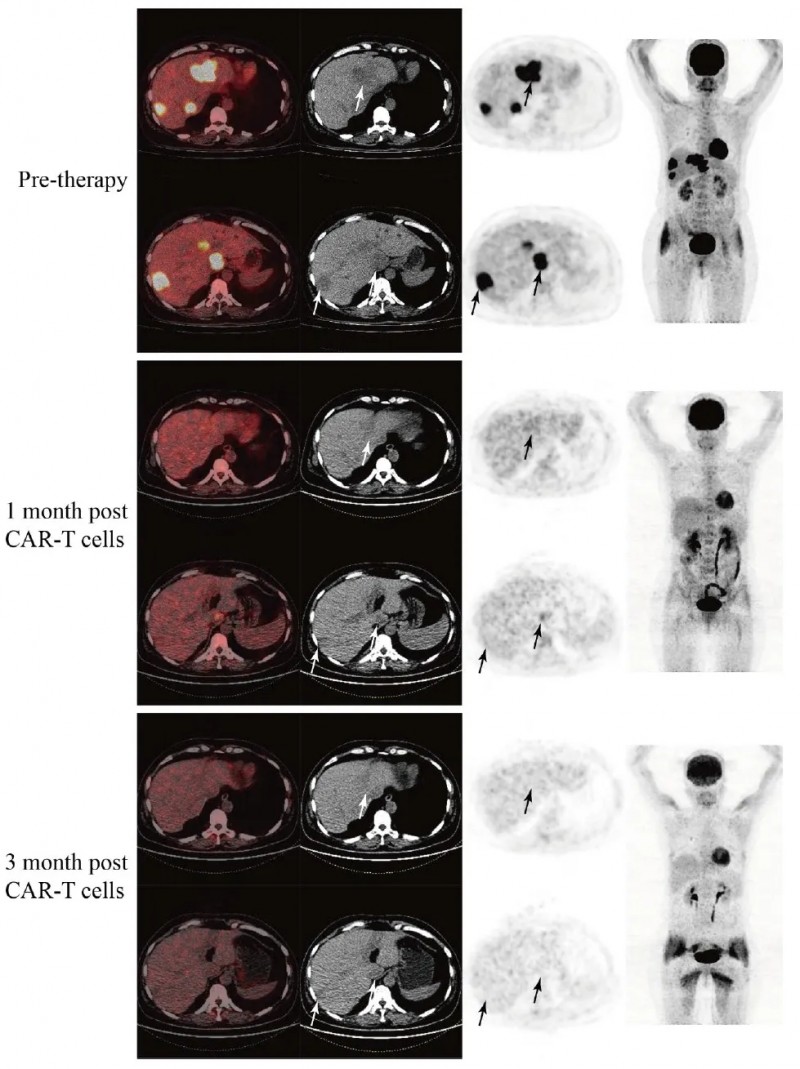
2、患者9(2×10⁶cells/kg剂量GCC19CART细胞):治疗后3个月,两个肝转移灶显著缩小,膈上/下病灶FDG摄取量持续减少,肝脏内无FDG摄取。根据RECIST1.1标准,该患者达到部分缓解(PR)。
▲图源“JAMA Oncol”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
小编寄语
近些年来,以CAR-T疗法为代表的免疫细胞疗法已取得了长足的进展,为复发/难治性肿瘤患者带来了新的希望与选择!我国的CAR-T研发热度空前高涨,相继有驯鹿医疗、科济生物、传奇生物、复星凯特等20多家制药巨头纷纷投身CAR-T的研发大军中,我国也成为了继美国之后的又一CAR-T“大国”,相继有多款产品获批上市,并在世界顶级癌症大会中“崭露头角”!
好消息是,目前有多款CAR-T疗法的临床研究正在招募中,对此感兴趣的患者,可将近期影像学检查、治疗经历、病理检查报告等资料,提交至医学部,了解详细的入排标准或进行初步评估。
参考资料
[1]Chen N,et al.Chimeric Antigen Receptor T Cells Targeting CD19 and GCC in linkstatic Colorectal Cancer: A Nonrandomized Clinical Trial.JAMA Oncol.2024 Nov 1;10(11):1532-1536.
https://pmc.ncbi.nlm.nih.gov/articles/PMC11413756/