六大细胞免疫疗法助力战胜癌症,横扫肺癌、胰腺癌、宫颈癌、血癌等,总缓解率100.0%+转移灶清零
癌症犹如深谙生存之道的"进化型猛兽",凭借持续变异的特性适应环境,加之病理类型高度多样,使得研发适用于所有患者的普适性药物始终面临巨大挑战。
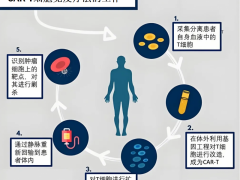
近年来,癌症治疗领域迎来革命性变革——以免疫细胞疗法为代表的精准医疗技术,正在改写传统抗癌格局。尤其随着CAR-T、TCR-T、TIL、CAR-NK等细胞治疗技术持续突破,在血液肿瘤与实体瘤治疗中展现出振奋人心的潜力,为攻克癌症点燃新的希望。本文将聚焦2025年值得重点关注的六大抗癌新技术,以期帮助更多患者重拾信心,积极拥抱治疗。
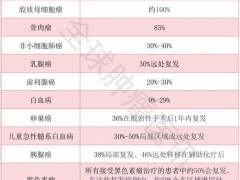
六大免疫细胞利器出鞘:暴击骨髓瘤、肺癌、宫颈癌、胰腺癌、肾癌等,从总缓解率达100.0%,到无癌生存超3年
01、OriCAR-017(CAR-T):多发性骨髓瘤总缓解率达100.0%
OriCAR-017是一种新型靶向GPRC5D的嵌合抗原受体T细胞(CAR-T)疗法,其新药IND相继获得中国国家食品药品监督管理局(NMPA)、美国食品药品监督管理局(FDA)批准。
《临床肿瘤学杂志》公布了“OriCAR-017治疗复发/难治性多发性骨髓瘤(RR MM)”1期临床研究的长期随访结果。
结果显示:在所有入组的复发/难治性多发性骨髓瘤(RR MM)患者中(n=10),总缓解率(ORR)竟达到100.0%!严格完全缓解率(sCR)达80.0%。中位无进展生存期(mPFS)为11.37个月(95%C1,5.93-18.00)。在治疗第28天,微小残留病灶阴性率(MRD)达到了100%,且在第3个月得到进一步检测确认为100%阴性。
▲截图源自“ASCO Publications”
总之,上述长期随访数据显示,OriCAR-017在治疗复发/难治性多发性骨髓瘤(RR MM)方面,表现出深入且持久的反应,且安全性良好,有望成为此类患者的有效治疗选择。
02、NY-ESO-1 TCR-T疗法:晚期肺癌患者转移灶缩小近50%,胸水完全吸收
《oncology Letters》曾报道一项"应用NYESO1特异性TCR-T细胞治疗晚期非小细胞肺癌(NSCLC)"的临床研究(NCT02457650),其数据令人瞩目。作为癌症免疫治疗的关键靶点,NYESO1在11.8%~21%的NSCLC中呈阳性表达。
研究结果显示:依据实体肿瘤疗效评价标准(RECIST)1.1,1例患者(患者1)在治疗近3个月后病情稳定(SD);另1例患者(患者2)在治疗4个月时达到部分缓解(PR)。
其中,44岁的HLA-A2阳性肺腺癌女性患者值得关注。该患者携带EGFR突变及NY-ESO-1表达,在经历多西他赛+卡铂化疗及吉非替尼、厄洛替尼治疗后病情持续进展,CT显示右肺门、纵隔、胸膜、肝叶及包膜等多处病灶进展(PD),传统疗法已无力回天。
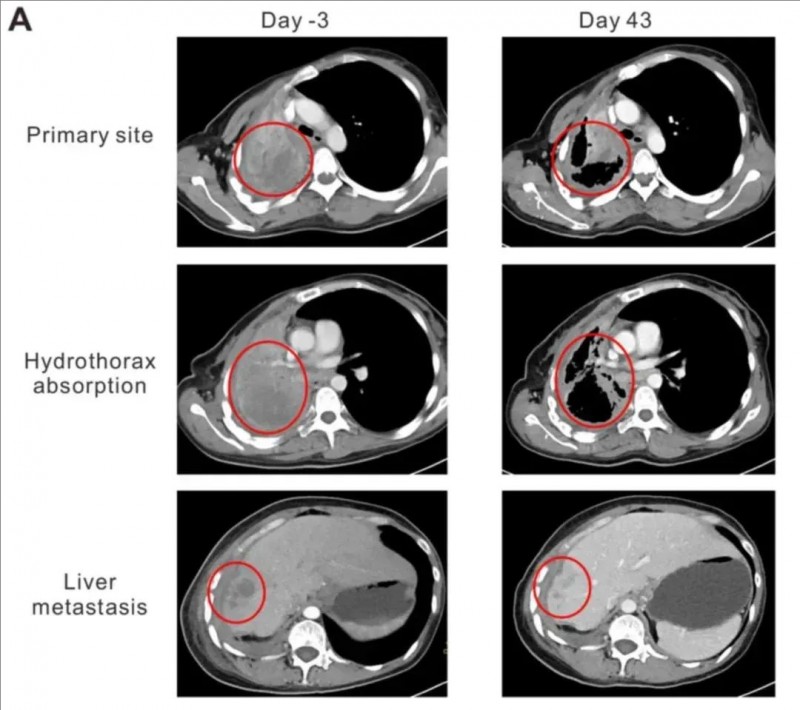
入组接受NYESO1 TCR-T治疗后,依据RECIST1.1标准达到部分缓解(PR),卡氏功能状态评分(KPS)从50分跃升至90分,咯血与胸痛症状显著缓解。治疗第43天CT显示,肺原发灶从95×86×54mm缩小至64×44×54mm,肝转移灶由19.8×19.6×20mm缩至10×10×10mm,胸水吸收、肺组织复张。这些数据充分表明,TCR-T疗法显著改善了患者的临床症状,彰显了其逆转晚期病情的强大潜力。
▲图源“OncologyLetters”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
03、GT316(TIL):宫颈癌患者治疗4周达完全缓解,38周转移灶清零
GT316是沙砾生物基于ImmuTFinder®平台,开发出的一款CRISPR/Cas9-dualKO抗衰竭TIL产品。
在2025 AACR大会上,公布了GT316首次人体试验(NCT06145802)的惊艳数据。
其中,一位难治性宫颈癌患者在输注GT316仅4周后,便达到完全缓解(CR)状态。治疗前,该患者阴道内24mm的转移性病灶,在第38周的放射影像检查中已实现100%缩小。
▲截图源自“AACR”
04、NK细胞联合WT1-DC疫苗,全身多处转移灶消失、腹水基本吸收
《Cureus》杂志曾报道一则“NK细胞+WT1-DC疫苗联合治疗”的振奋案例:一位30多岁的IV期子宫内膜癌女性患者,因单纯化疗预后差,患者接受“化疗(紫杉醇+卡铂AUC5)+多轮WT1-DC树突状细胞疫苗+高活性NK细胞”联合治疗,疗效显著:
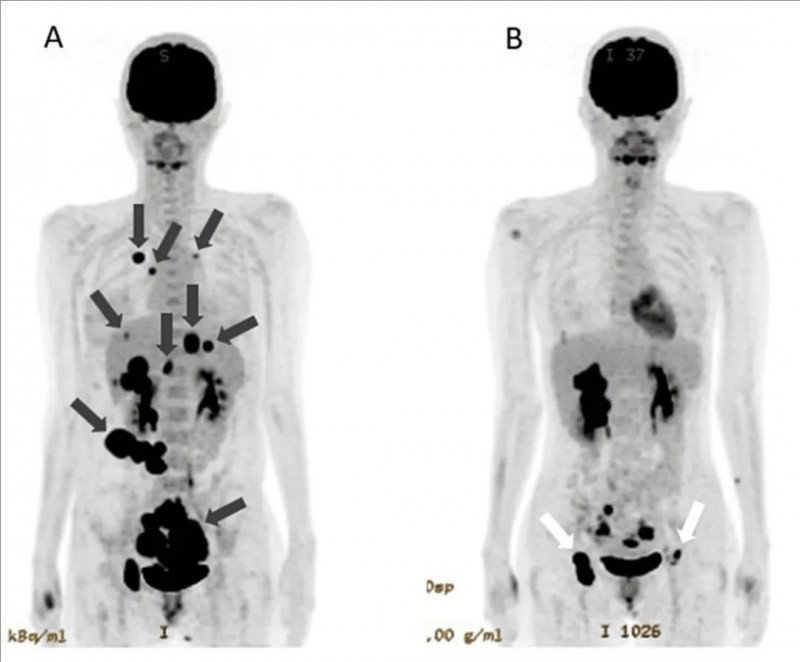
1.肿瘤体积显著退缩:治疗前全身PET-CT显示,双侧卵巢癌原发灶,伴肝、肺、腹膜、骨等多器官转移灶(详见下图A);联合治疗第142天复查显示,原发肿瘤明显缩小,肺转移灶及腹膜播散灶完全消失,肝转移灶体积显著缩小(详见下图B)。由于肿瘤明显缩小,患者计划接受原发肿瘤根治性切除术。
▲图源“Cureus”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
2.腹水控制与腹膜播散缓解:治疗前腹部CT可见大量腹水(图2A),在NK细胞治疗期间逐步减少,第56天腹部CT显示腹水基本吸收,肝转移灶缩小,提示NK细胞疗法对腹膜播散的控制效果显著。
3.肿瘤标志物与腹围改善:第三次NK细胞治疗后,癌胚抗原(CEA)、CA125(糖类抗原125)水平显著下降,腹围较治疗前明显减小。
该案例表明,NK细胞联合WT1-DC疫苗治疗在晚期实体瘤中展现出肿瘤退缩、症状改善的潜力,为多线治疗失败的患者提供了新的治疗思路。
05、Robo1-CAR-NK疗法:5个月内阻止肿瘤进展,胰腺癌总生存期突破8个月
《癌症研究与治疗学杂志》曾报道一则“应用Robo1特异性嵌合抗原受体自然杀伤细胞(CAR-NK),治疗转移性胰腺导管腺癌”病灶控制效果显著的经典案例。
该患者是一位46岁男性,确诊为胰腺导管腺癌(T4N1M1,IV期),CT及MRI显示胰腺存在6cm×2.5cm×3cm占位性病变,伴淋巴结浸润及肝转移,肝脏可见多处代谢亢进病灶,最大转移灶直径约3.5cm。因无法手术切除且拒绝化疗,加之胰腺肿瘤穿刺活检证实患者Robo1阳性表达,遂入组接受Robo1特异性CAR-NK细胞回输治疗。
结果显示:Robo1-CAR-NK细胞治疗5个月内,胰腺原发灶及肝转移病灶均得到有效控制。截至统计时,患者总生存期(OS)已达8个月。
▲截图源自“JCRT”
06、γδT细胞:治疗7个月肾癌肺转移灶消失,无癌生存超3年
《癌症免疫学与免疫治疗学》曾报道一项“应用γδT细胞治疗晚期肾细胞癌的I/II期临床试验”,其数据令人瞩目。
研究纳入11例接受过肾切除术的转移性肾细胞癌患者,基线期(治疗前-3个月至治疗开始)影像学显示,大多数转移性病灶体积呈急剧增长趋势。然而,接受γδT细胞治疗后,部分转移性病灶出现体积减小或增长速度显著放缓。其中,1例患者(TR05)达到完全缓解(CR),5例患者病情稳定(SD)。
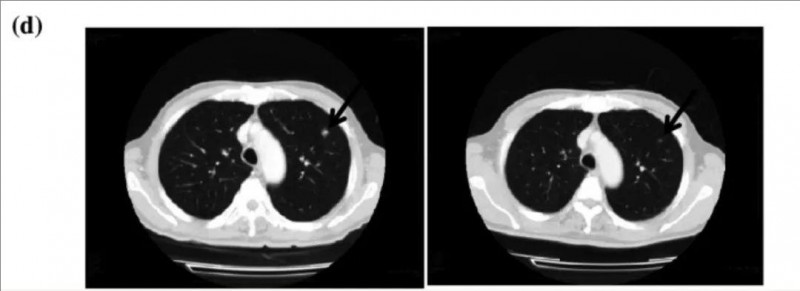
值得关注的是,患者TR05的转移性病变在γδT细胞治疗7个月内完全消失,且治疗完成后超过36个月仍保持无癌生存状态。治疗前后的CT影像对比显示,治疗开始3个月内,该患者的两处转移性病灶已在宏观层面消失(详见附图)。
▲图源“Cancer Immunol Immunother”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
此项研究表明,γδT细胞疗法在晚期肾细胞癌中展现出诱导肿瘤消退及长期病情控制的潜力。
小编寄语
免疫细胞疗法(如CAR-T、NK、TCR-T、TIL、CAR-NK)等抗癌新技术的突破,为癌症治疗带来了全新的局面。它们从不同角度和机制出发,精准打击癌细胞,激活人体自身免疫系统的抗癌潜能,在血液肿瘤和实体瘤治疗领域都取得了令人鼓舞的成果。虽然目前这些技术在应用中还面临一些挑战,如高昂的治疗费用、复杂的制备工艺、潜在的不良反应等,但随着研究的深入和临床试验的推进,相信未来这些技术将不断完善和优化,为人类最终战胜癌症提供强有力的武器。
好消息是,中国已成功研发出多款针对血液肿瘤及实体瘤的免疫细胞疗法,并在国内多家知名癌症中心启动临床,想明确自身靶点或寻求新型抗癌疗法帮助的患者,可将完整的病理报告、治疗经历、近期影像学检查资料等,提交至医学部,进行初步评估或了解详细的入排标准。
参考资料
[1]Huang H,et al.OriCAR-017, a novel GPRC5D-targeting CAR-T, in patients with relapsed/refractory multiple myeloma: Long term follow-up results of phase 1 study (POLARIS)[J]. 2024.
https://meetings.asco.org/abstracts presentations/239043
[2]Xia Y,et al.Treatment of linkstatic nonsmall cell lung cancer with NYESO1 specific TCR engineeredT cells in a phase I clinical trial: A case report[J]. oncology letters, 2018, 16(6): 6998-7007.
https://www.spandidos publications.com/10.3892/ol.2018.9534
[3]Nagai H,et al.Late-Stage Ovarian Cancer With Systemic Multiple linkstases Shows Marked Shrinkage Using a Combination of Wilms' Tumor Antigen 1 (WT1) Dendritic Cell Vaccine, Natural Killer (NK) Cell Therapy, and Nivolumab[J]. Cureus, 2024, 16(3).
https://www.cureus.com/articles/239260-late-stage-ovarian-cancer-with-systemic-multiple-linkstases-shows-marked-shrinkage-using-a-combination-of-wilms-tumor-antigen-1-wt1-dendritic-cell-vaccine-natural-killer-nk-cell-therapy-and-nivolumab#!/
[4]Li C,et al.Robo1-specific chimeric antigen receptor natural killer cell therapy for pancreatic ductal adenocarcinoma with liver linkstasis[J]. Journal of Cancer Research and Therapeutics, 2020, 16(2): 393-396.
https://journals.lww.com/cancerjournal/fulltext/2020/16020/robo1_specific_chimeric_antigen_receptor_natural.29.aspx
[5]Kobayashi H,et al.Phase I/II study of adoptive transfer of γδ T cells in combination with zoledronic acid and IL-2 to patients with advanced renal cell carcinoma. Cancer Immunol Immunother. 2011 Aug;60(8):1075-84.
https://pmc.ncbi.nlm.nih.gov/articles/PMC11029699/