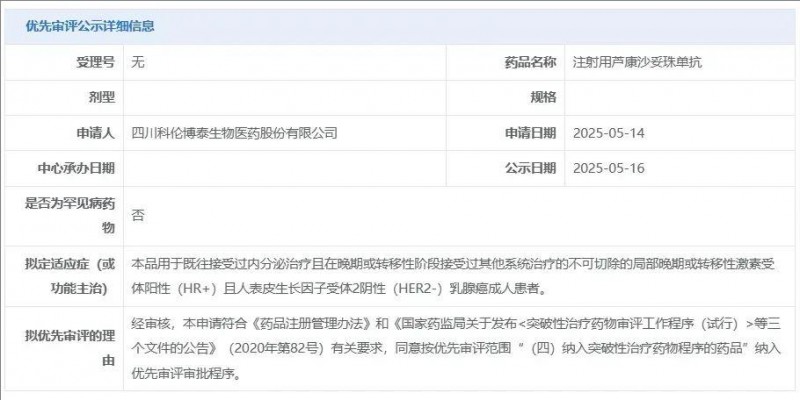
2025年5月16日国家药监局批准注射用芦康沙妥珠单抗(SKB264、佳泰莱、Sacituzumab Tirumotecan、MK2870、sac-TMT)用于乳腺癌
2025年5月16日,中国国家药监局药品审评中心(CDE)传来振奋人心的好消息——注射用芦康沙妥珠单抗正式纳入优先审评,用于成人既往接受过内分泌治疗,且在晚期或转移性阶段接受过其他系统治疗的不可切除局部晚期或转移性激素受体阳性(HR+)、人表皮生长因子受体2阴性(HER2-)乳腺癌的治疗。
优先审评的加速推进,意味着这款创新疗法即将更快惠及亟待突破治疗瓶颈的患者,为中国乳腺癌诊疗领域注入强劲动力,助力更多患者拥抱长生存可能!
▲截图源自“CDE”
中国原研ADC——芦康沙妥珠单抗震撼登场,三阴性乳腺癌/非小细胞肺癌患者迎来救命新药
芦康沙妥珠单抗(SKB264,Sacituzumab Tirumotecan,sac-TMT,佳泰莱®,MK-2870)是科伦博泰自主研发的一款靶向TROP-2的抗体偶联药物(ADC)。
其作用机制为:通过重组抗TROP2人源化单克隆抗体特异性识别肿瘤细胞表面TROP2抗原,被内吞后释放拓扑异构酶I抑制剂KL610023,诱导肿瘤细胞DNA损伤、阻滞细胞周期并引发凋亡;同时,KL610023可通过肿瘤微环境的旁观者效应渗透至邻近肿瘤细胞,扩大抗癌效应。目前,芦康沙妥珠单抗已有两项适应症在中国获批上市:
1、既往至少接受过2种系统治疗(含至少1种晚期或转移性阶段治疗)的不可切除局部晚期或转移性三阴性乳腺癌。
2、经EGFR-TKI和含铂化疗治疗后,进展的EGFR突变阳性局部晚期或转移性非鳞状非小细胞肺癌。
芦康沙妥珠单抗暴击HR+/HER2阴性转移性乳腺癌,疾病控制率高达89.5%
2023年ESMO大会上,公布了芦康沙妥珠单抗(SKB264)治疗HR+/HER2阴性转移性乳腺癌(mBC)的I/II期临床数据(NCT04152499),结果令人瞩目。
该研究共入组41例乳腺癌患者,中位年龄50岁(34-66岁),中位随访8.2个月。在38例可评估疗效的患者中,47%存在原发性内分泌耐药,79%既往接受过≥2线转移性化疗,治疗史包括紫杉烷类药物(100%)和CDK4/6抑制剂(65.8%)。
结果显示:客观缓解率(ORR)为36.8%(14/38,含12例确诊PR、2例未确诊PR),疾病控制率(DCR)高达89.5%;中位缓解持续时间(DoR)为7.4个月(4.2-14.9+个月),6个月DoR率80%;中位无进展生存期(PFS)为11.1个月(95%CI:5.4,13.1),6个月PFS率高达61.2%。
▲截图源自“ESMO”
喜讯!国内多家癌症中心启动芦康沙妥珠单抗临床招募,晚期患者迎来精准治疗新希望
相信看了上面的数据,乳腺癌患者一定重新燃起了希望!好消息是目前我国正在开展芦康沙妥珠单抗(SKB264)治疗局部晚期或转移性实体瘤的临床研究,现已有大量患者通过全球肿瘤医生网抗癌新药招募中心,成功入组接受这款抗癌新药的治疗!
适应证
适用于二线失败或标准治疗失败的Ⅰ期或Ⅱ期实体瘤、头颈鳞癌、胃食管交界处腺癌、胃腺癌、子宫内膜癌等。
招募信息(部分)
1)年龄≥18岁,性别不限。
2)经组织学确诊的无法根治的局部晚期或转移性上皮来源的恶性肿瘤患者,目前可以筛头颈,胃、子宫内膜、尿路上皮癌四种(注:TROP2评估不会在入组前进行,入组前无需通过免疫组织学或其他方法确认TROP2表达水平,但是申办方要求收集活检或存档肿瘤组织样本来测定TROP2表达水平)。
3)受试者必须有通过电子计算机断层扫描(CT)或磁共振成像(MRI)检测的可测量病灶。
4)所有经标准治疗失败,或无标准治疗方案,或现阶段不适用标准治疗的不可手术切除的局部晚期或转移性实体瘤。
5)中性粒细胞计数(NEUT)≥1.5×109/L,血小板计数(PLT)≥100×109/L;血红蛋白浓度≥9.0g/dL。
申请流程
想申请芦康沙妥珠单抗临床试验的患者,需将近期基因检测报告、病理报告等资料汇总后,提交至医学部,进行初步评估。我们的专家将为您全面分析解读检测报告,并匹配适合患者入组的临床试验项目。
小编寄语
近年来,我国抗癌新药的研发速度,正以前所未有的中国速度迈向世界前列!尤其是经历三代技术变革的ADC药物,可在杀伤癌细胞的同时,避免损伤周围正常组织或细胞。随着芦康沙妥珠单抗的正式获批,标志着我国在ADC药物的研发领域迈出了重要的一步,为乳腺癌、肺癌等晚期实体瘤患者带来了新的希望与选择!对现有治疗方案存疑或想参加方舟计划获得免费用药机会的患者,可将近期影像学及病理检查报告、治疗经历等资料,提交至医学部,进行初步评估或了解详细的入排标准。
参考资料
[1]Ouyang Q,et al. 380MO SKB264 (MK-2870) in previously treated hormone receptor-positive (HR+)/HER2-negative linkstatic breast cancer (mBC): Results from a phase I/II, single-arm, basket trial[J]. Annals of Oncology, 2023, 34: S337.
https://www.annalsofoncology.org/article/S0923-7534(23)01393-5/fulltext