癌症疫苗改写"癌王"胰腺癌预后,肺癌、卵巢癌等实体瘤有救了
NHS国家癌症临床主任Peter Johnson教授曾满怀期待地指出:"我们深知,即便手术成功,癌症仍有可能复发。这或许是因为体内仍残留着少量癌细胞,但使用针对这些残留癌细胞的癌症疫苗,就有希望阻止复发情况的发生”。
近日,《癌症免疫与免疫治疗》杂志发表的一项前沿研究,为这一前瞻性设想提供了有力佐证!在7例接受Neo-P树突状细胞疫苗辅助治疗的胰腺癌患者中,仅1例出现复发,且在术后长达61个月(约5年)的中位随访期内,所有患者均保持存活!
这项研究不仅证实了Neo-P树突状细胞疫苗在胰腺癌术后复发预防及辅助治疗中的可行性与有效性,更在"癌王"胰腺癌面前展现出独特优势——要知道,胰腺癌预后极差,5年生存率仅13%!这一突破性进展,为癌症治疗领域注入了强心动力!它不仅为胰腺癌患者点亮了新的希望之光,更标志着癌症疫苗技术正以突破性速度攀登新高峰。
▲截图源自“frontiers”
传统化疗与Neo-P DC疫苗:胰腺癌生存数据的"天壤之别",复发患者生存期从14个月跃升至超36个月,辅助治疗组5年随访存活率100%
胰腺癌因早期诊断困难、晚期化疗耐药性强,预后极差,5年生存率仅13%。因此,迫切需要开发新的突破性疗法。而《癌症免疫与免疫治疗》杂志发表的这项前沿研究,共纳入16例接受Neo-P DC疫苗治疗的胰腺癌术后患者,其中9例患者术后复发,7例患者在胰腺切除术后接受辅助治疗,回顾性评估新抗原肽脉冲树突状细胞(Neo-P DC)疫苗的安全性与有效性。
▼16例胰腺癌术后患者接受了Neo-P DC疫苗注射治疗
▲图源“frontiers”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
结果显示:在16例接受Neo-P树突状细胞疫苗治疗的患者中,13例(81.3%)诱导产生了肿瘤新抗原特异性T细胞。
在9例术后复发患者中,3例复发后生存期超36个月(详见下图A)(远超标准化疗组胰腺癌术后复发患者中位总生存14个月的既往数据)。此外,经Neo-P树突状细胞疫苗诱导产生产生特异性T细胞的7例患者,预后显著优于无应答者(详见下图B)。
▲图源“frontiers”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:
①图A:接受Neo-P DC疫苗治疗的复发患者的Kaplan-Meier OS分析(复发后OS)。
②图B:复发患者中对Neo-P DC疫苗有反应和无反应者的Kaplan-Meier OS分析(复发后OS)。
此外,7例接受Neo-P树突状细胞疫苗辅助治疗的患者中,仅1例出现单发肝转移(经射频消融后50个月内未再复发),其余6例无复发;且在中位随访61个月(范围:25-70个月)内,所有患者均存活。
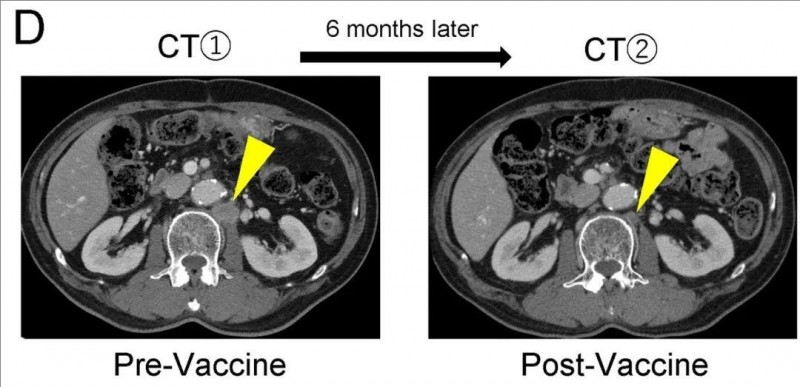
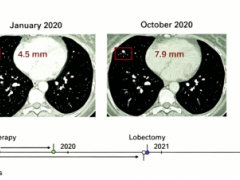
其中一个典型病例(复发#8)值得关注,该患者在联合使用长肽/短肽疫苗后,肿瘤新抗原特异性T细胞应答反应强烈。该患者术后历经新辅助化疗、根治性手术及多次化疗后出现复发,而在联合应用Neo-P DC疫苗与改良FOLFIRINOX化疗后,CT显示转移灶显著缩小(详见下图D),充分体现了疫苗与传统治疗手段的协同增效潜力。
▲图源“frontiers”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
综上,Neo-P DC疫苗诱导的肿瘤新抗原特异性T细胞与预后改善直接相关,尤其在辅助治疗中展现出预防复发的显著优势。鉴于标准化疗对复发性胰腺癌疗效有限,早期引入Neo-P DC疫苗或成为提升患者生存的关键策略。这一突破为"癌王"治疗开辟了新路径,有望改写胰腺癌预后困境。
目前,癌症疫苗中疗效及预防复发效果较为突出的为树突状细胞疫苗、个性化新抗原疫苗等,比如德国和日本等国,就将树突状细胞疫苗用于临床,辅助治疗肺癌、肾癌、肝癌、皮肤癌、乳腺癌等多种癌症。
想寻求国内外癌症疫苗治疗新技术帮助的患者,可将近期病理报告、治疗经历、出院小结等资料,提交至医学部,进行初步评估。
癌症疫苗横扫肺癌、卵巢癌、CLDN6阳性实体瘤等
近年来,癌症治疗领域迎来显著突破,免疫疗法正以其独特优势成为极具前景的治疗方向。这类疗法通过激活人体自身免疫系统,实现对癌细胞的精准识别与打击。在众多免疫治疗手段中,癌症疫苗作为一种创新且高效的技术尤为瞩目——它通过强化人体对肿瘤抗原的免疫识别能力,为癌症治疗开辟了全新路径。临床实践表明,将癌症疫苗与其他免疫疗法(如PD-1抑制剂、CAR-T细胞疗法等)联合应用,不仅能通过协同效应提升治疗有效性,更可依托个性化方案设计,在增强抗肿瘤效应的同时降低副作用,为患者提供更优化的治疗选择。值得关注的是,除了前文提及的、在胰腺癌治疗中展现潜力的Neo-P树突状细胞疫苗外,多款癌症疫苗已在不同癌种的临床研究中彰显不俗实力,为预防癌症复发、延长患者的生存期带来了新的选择!
国研KRAS G12V mRNA疫苗火力全开:助肺癌达部分缓解,右肺病灶近乎消失
上海交通大学医学院附属瑞金医院胰腺疾病诊疗团队开展的“针对KRAS G12V单靶点的mRNA肿瘤疫苗在晚期实体瘤中治疗效果的研究”,为mRNA疫苗应用于晚期实体瘤治疗带来新突破。这项研究首次通过人体试验证实,针对多种新抗原的mRNA疫苗在13例晚期黑色素瘤患者中展现出安全性及初步有效性,甚至促使两例终末期癌症患者体内肿瘤出现缩小。其突破性数据同步发表于国际医学顶级期刊《Cell Research》。
典型病例(患者002)为一位69岁的男性,年度体检发现肺部结节,经CT及PET-CT检查,确诊为双肺及纵隔淋巴结多发转移的晚期非小细胞肺癌(NSCLC)。因错失手术机会,患者先接受帕博利珠单抗联合化疗(白蛋白结合型紫杉醇+奈达铂),前三周期治疗后肿瘤病灶明显消退,但后续出现治疗耐药,并伴有以肢体麻木、疲劳为主要表现的严重神经毒性,遂停止化疗,转为mRNA疫苗联合派姆单抗(帕博利珠单抗)治疗,共完成9个周期。
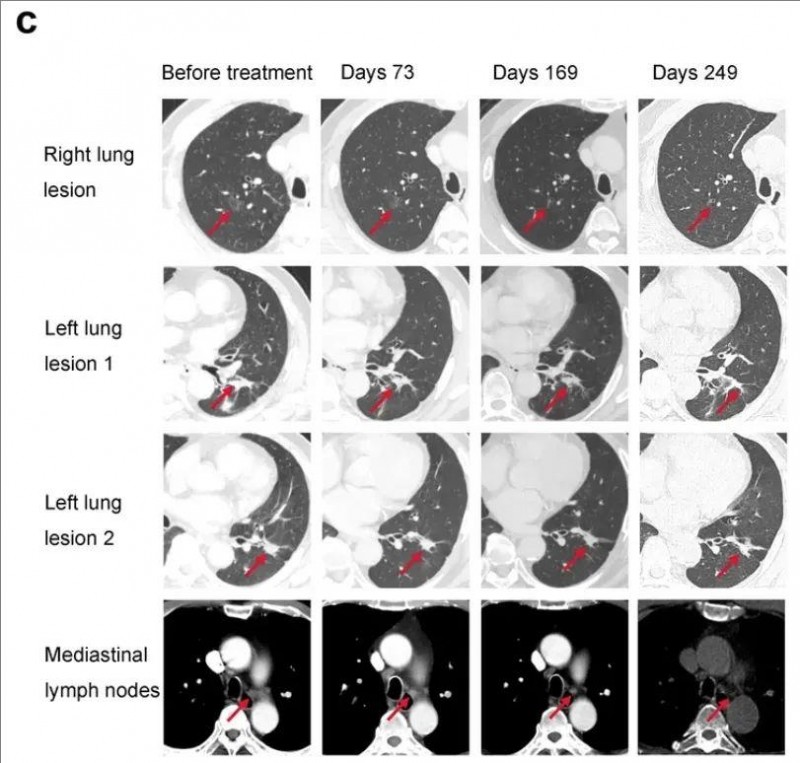
结果显示:根据实体肿瘤疗效评价标准(RECIST1.1),患者达到部分缓解(PR),右肺病灶基本消失,左肺病灶及纵隔淋巴结显著缩小(详见下图1c)。且治疗期间,患者仅出现预期可控的发热或注射部位疼痛,无其他不良反应。
▼患者002癌症疫苗治疗前后的多个肿瘤病灶CT对比
▲图源“cell research”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
mRNA疫苗联合CAR-T暴击CLDN6阳性实体瘤,疾病控制率达67%,肺转移灶经治后"清零"
BNT211是BioNTech公司研发的创新疗法,将靶向CLDN6抗原(一种在多种实体瘤中高度特异性表达的癌胚抗原)的CAR-T细胞疗法,与表达CLDN6抗原的mRNA疫苗(CARVac)相结合。疫苗注射后可将抗原RNA递送至淋巴器官的抗原呈递细胞(APC),通过增强抗原呈递强化CAR-T细胞的抗癌效应。
《自然医学(Nature Medicine)》报道了BNT211-01的1/2期临床试验(NCT04503278)的惊艳数据。该研究共纳入22例复发或难治性CLDN6阳性实体瘤患者(包括13例睾丸癌、4例浆液性癌,以及胃腺癌、子宫内膜癌等其他癌种各1例)入组。
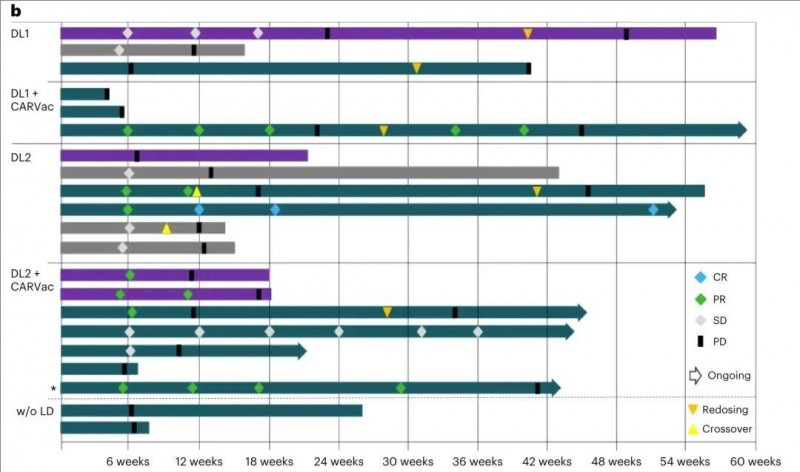
结果显示:21例可评估患者的客观缓解率(ORR)达33%,其中6例部分缓解(PR),1例完全缓解(CR),CR持续时间达10.5个月;疾病控制率(DCR)为67%,7例病情稳定(SD),5例靶病变可量化缩小。
▼所有疗效可评估患者(n=21)治疗后的反应示例图
▲图源“nature medicine”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
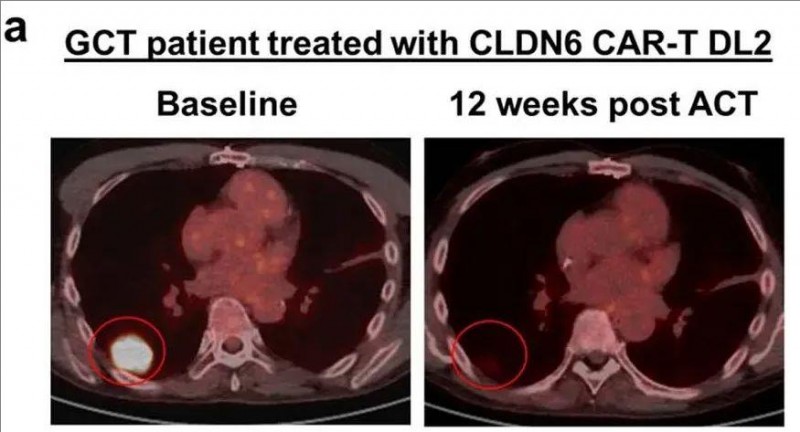
值得一提的是,其中一名合并肺转移的生殖细胞肿瘤(GCT)患者疗效显著:该患者初诊为混合型GCT,历经5种化疗方案、多次手术及放疗后,晚期复发并出现肺转移,病情进展迅速(筛选期靶病灶总和增加37%),且80%肿瘤细胞CLDN6膜染色≥2+阳性。该患者入组后,先经淋巴细胞清除化疗(LD),之后接受单剂量CLDN6CAR-T细胞治疗。
结果显示:该患者7天内肿瘤标志物甲胎蛋白(AFP)下降50%并持续受控;治疗12周后,PET-CT显示肺部大块转移灶完全消失,达到代谢完全缓解(CR)(详见图a)。
▲图源“nature medicine”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
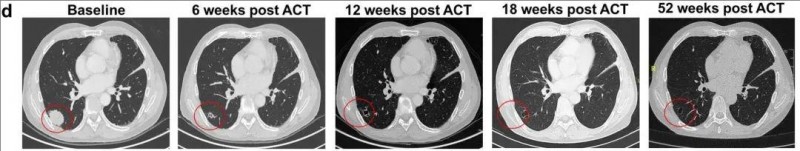
CT扫描显示,肺部大块转移灶被完全清除,截至治疗后52周的最新扫描,患者持续维持完全缓解(CR)状态(详见图d)。
▲图源“nature medicine”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
WT1-DC疫苗联合NK细胞,助卵巢癌患者肿瘤显著缩小、腹水完全消退
近期,国际医学杂志《Cureus》报道了一则IV期子宫内膜癌患者的突破性治疗案例:一位30岁女性在产后6个月确诊为晚期癌症(肿瘤全身转移至卵巢、腹膜、肝、肺、骨,伴大量腹水),经NK细胞、WT1-DC疫苗联合纳武利尤单抗治疗后,全身肿瘤显著退缩,腹水完全消失,并获得原发肿瘤根治性手术机会。
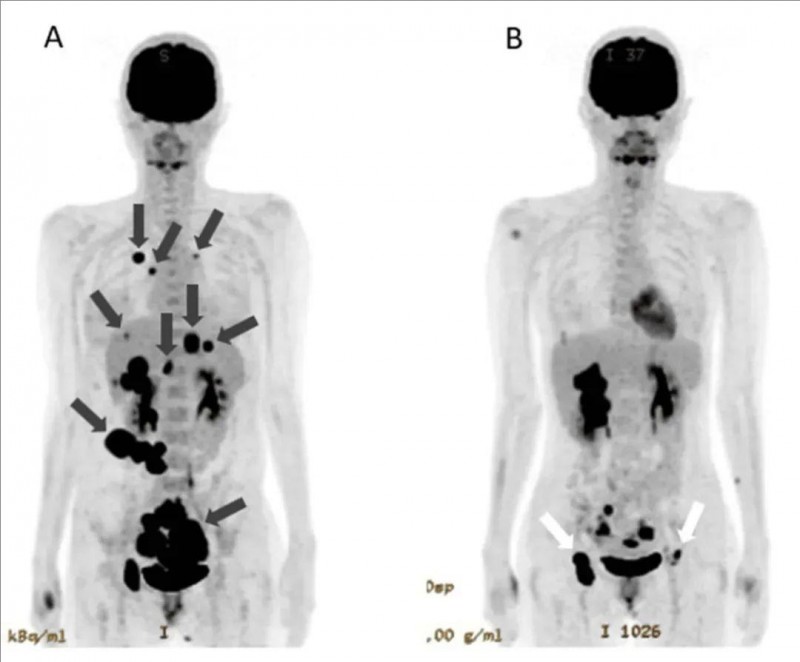
该患者因腹水就诊,经全面检查,确诊为IV期子宫内膜癌(详见图1A)。PET-CT显示双侧卵巢癌、腹膜播散、肝肺骨多发转移(图1A),腹部CT可见大量腹水(图2A)。初始化疗(紫杉醇+卡铂)效果有限,遂启动免疫细胞联合治疗方案:化疗(紫杉醇+卡铂AUC5)基础上,叠加WT1-DC疫苗(靶向高表达肿瘤抗原WT1)+高活性NK细胞联合治疗。
1、肿瘤影像学显著改善:治疗前PET-CT显示,该患者存在原发卵巢癌及肝、肺、腹膜等多处转移灶(详见下图A)。在WT1-DC疫苗联合治疗142天,原发肿瘤体积缩小,肺转移灶与腹膜播散灶完全消失,肝转移灶显著缩小(详见图B)。更令人振奋的是,鉴于肿瘤的明显缩小,患者计划考虑进行原发肿瘤根治性切除术。
▲图源“Cureus”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
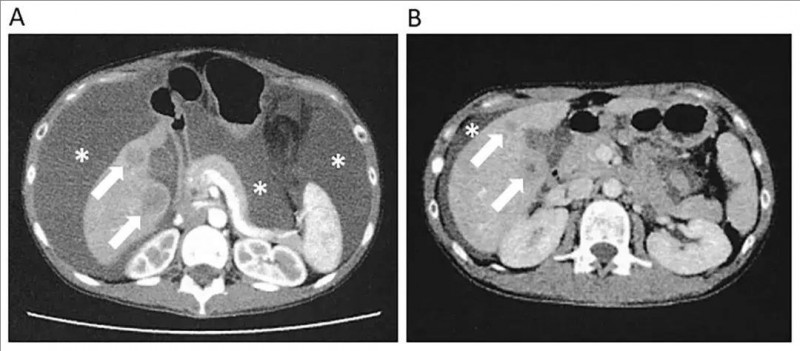
2、腹水控制:治疗56天后腹部CT显示腹水大幅减少(详见下图),最终完全消失,证实NK细胞对腹膜播散的抑制作用。
▲图源“Cureus”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
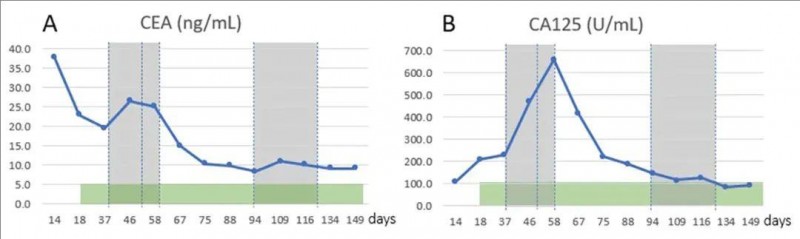
3、肿瘤标志物改善:第三次NK细胞治疗后,癌胚抗原(CEA)、糖类抗原125(CA125)显著下降至接近正常范围,腹围同步减小(图4)。而在DC疫苗治疗初期出现CA125短暂上升,提示肿瘤微环境变化或治疗应激反应,后续随联合治疗推进趋于稳定。
▲图源“Cureus”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
小编寄语
癌症疫苗作为癌症治疗领域的新兴力量,历经数十载的发展,展现出了巨大的潜力和前景。随着研究的不断深入和技术的不断进步,我们有理由相信,癌症疫苗将在未来的癌症治疗中,发挥越来越重要的作用,还可与手术、化疗、放疗、免疫治疗等传统治疗手段相结合,形成综合治疗方案,为肿瘤患者带来更高的生存获益!小编也期望随着癌症疫苗的不断优化,未来可以创造出更多的抗癌奇迹!想寻求癌症疫苗等新型抗癌疗法帮助的患者,可将治疗经历、近期病理及影像学检查结果等,提交至医学部,进行初步评估或申请国内外抗癌专家会诊。
参考资料
[1]Oyama K,et al.Neoantigen peptide-pulsed dendritic cell vaccine therapy after surgical treatment of pancreatic cancer: a retrospective study[J]. Frontiers in Immunology, 2025, 16: 1571182.
https://www.frontiersin.org/journals/immunology/articles/10.3389/fimmu.2025.1571182/full
[2]Wang X,et al.Combination therapy of KRAS G12V mRNA vaccine and pembrolizumab: clinical benefit in patients with advanced solid tumors[J]. Cell Research, 2024, 34(9): 661-664.
https://www.nature.com/articles/s41422-024-00990-9
[3]Mackensen A,et al.CLDN6-specific CAR-T cells plus amplifying RNA vaccine in relapsed or refractory solid tumors: the phase 1 BNT211-01 trial[J].Nature Medicine,2023,29(11):2844-2853.
https://www.nature.com/articles/s41591-023-02612-0
[4]Nagai H,et al.Late-Stage Ovarian Cancer With Systemic Multiple linkstases Shows Marked Shrinkage Using a Combination of Wilms' Tumor Antigen 1 (WT1) Dendritic Cell Vaccine, Natural Killer (NK) Cell Therapy, and Nivolumab[J]. Cureus, 2024, 16(3).
https://www.cureus.com/articles/239260-late-stage-ovarian-cancer-with-systemic-multiple-linkstases-shows-marked-shrinkage-using-a-combination-of-wilms-tumor-antigen-1-wt1-dendritic-cell-vaccine-natural-killer-nk-cell-therapy-and-nivolumab#!/