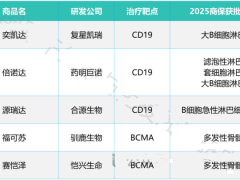
中国国产CART细胞疗法完全缓解率成功超50%,交出满意生存答卷,与ASCT梦幻联动
近日,中国专家团队携双CD19/CD20 CAR-T细胞疗法,重磅亮相第51届欧洲血液与骨髓移植协会年会(EBMT),向全球公布了针对复发/难治性B细胞淋巴瘤的1/2期试验结果,为癌症治疗领域注入一剂强心针!
一直以来,复发/难治性B细胞淋巴瘤就如同横亘在医患面前的一座大山,严重威胁患者的生命健康。但这次研究结果令人振奋!对于复发/难治性B细胞淋巴瘤患者而言,双CD19/CD20 CAR-T细胞疗法更是展现出革命性的显著疗效,总体反应率一骑绝尘,高达84%,完全反应率也达到52%。不仅如此,相较于单纯CAR-T细胞疗法,该疗法与ASCT携手联合后,如同超级战队,进一步释放出强大的治疗效能,显著改善了患者的无进展生存率和总体生存率。这一突破性的研究成果,预示着中国在癌症治疗领域已站在世界前沿,正引领全球向攻克癌症的目标大步迈进!
▲截图源自“OncLive”
国研CD19/CD20 CAR-T疗法携手ASCT,攻克B细胞淋巴瘤,斩获84%高缓解率且疗效持久,超半数患者达完全缓解
CD19嵌合抗原受体(CAR)T细胞疗法在复发/难治性B细胞淋巴瘤(r/r-BCL)患者的治疗中展现出显著疗效。然而,由于CD19抗原可能缺失,这一疗法的效果受到限制,在复发/难治性BCL中,CD19靶向CAR-T细胞疗法的疗效常因CD19抗原丢失而大打折扣。为克服r/r-BCL中的CD19复发问题,我国开发了一款同时靶向CD19与CD20抗原的CAR-T细胞药物,相较于单独输注,串联CD19/CD20 CAR-T细胞联合自体造血干细胞移植(ASCT),可实现更高的完全缓解(CR)率。
在第51届EBMT年度会议上,公布的这项研究共纳入51例复发/难治性B细胞淋巴瘤患者,中位年龄为51岁(年龄范围:28-74岁)。这些患者的疾病类型多样,包括弥漫性大B细胞淋巴瘤(DLBCL,n=39)、滤泡性淋巴瘤(n=4)、伯基特淋巴瘤(n=4)、边缘区淋巴瘤(MZL,n=2)、套细胞淋巴瘤(MCL,n=2)。入组患者中,86.3%(44/51)在入组前处于III/IV期疾病阶段,68.6%(35/51)接受过三线或更高线数的治疗。所有患者入组后,均接受了串联CD19/20 CAR-T输注。
结果显示:截至2024年12月5日,患者的最佳和3个月总缓解率(ORR)为84%(42/50)。其中,52%(26/50)的患者达到完全缓解(CR),32%(16/50)的患者获得部分缓解(PR)。此外,亚组分析结果显示,接受ASCT后输注CD19/20 CAR-T细胞的患者,其CR率高于仅接受CD19/20 CAR-T细胞治疗的患者,CRR分别为83.3% vs 34.4%。
所有入组患者的预估1年无进展生存(PFS)率为74.0%(95%CI,60.0%-84.2%),1年中位总生存(OS)率为86.0%(95%CI,72.8%-93.1%)。对于在第3个月达到ORR的患者,其估计1年PFS率为85.4%(95%CI,70.3%-93.2%),1年OS率更是高达97.4%(95%CI,83.2%-99.6%)。此外,亚组分析结果显示,ASCT后输注CD19/20 CAR-T细胞的患者,1年生存率优于单纯接受CD19/20 CAR-T细胞治疗的患者,PFS率分别为83.0% vs 69.4%,OS率分别为94.1% vs 81.5%。
▲图源“EBMT”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
总之,上述结果表明,优化的铰链CD19/20CAR-T,尤其是与造血干细胞移植(ASCT)联合使用时,在r/r-BCL患者中实现了持久缓解且安全。
国研PD-1Ab21-CD19 CAR-T细胞直击复发性白血病难题,助患者走向完全缓解
在过往CD19 CAR-T细胞治疗临床试验中,脑部转移患者通常被排除在入组范围外,无法接受治疗。而我国自研的一款PD-1Ab21-CD19CAR-T细胞能够分泌细胞因子(interleukin)融合蛋白,促使进入颅内的CAR-T细胞有效活化与增殖,因此对脑转移肿瘤具备良好治疗效果。
在2024年美国癌症研究协会(AACR)年会上,我国研究团队公布了PD-1Ab21-CD19 CAR-T治疗难治复发性急性B淋巴细胞白血病的单臂临床研究(IIT)结果。该研究目前入组10例白血病患者,其中5例在接受异基因造血干细胞移植后出现缓解-复发,4例伴有中枢神经系统(CNS)浸润并出现相关症状。
初步研究结果令人振奋:在已入组且可评估的3例复发/难治晚期B细胞恶性肿瘤患者中,接受CD19 CAR-T细胞回输治疗后,均在治疗后三周内实现完全缓解(CR)和/或中枢神经系统症状消失。这些成果为白血病患者,尤其是伴有CNS侵袭的患者带来了新希望!
值得一提的是,其中一位69岁女性患者。在2021年8月确诊为急性混合细胞(B/髓系)白血病。经过一年多的持续化疗,次年9月,患者因双下肢无力、头脑发胀等症状再次入院,确诊白血病复发。颅脑核磁共振检查显示:其右侧颞部、左侧颞顶枕部存在白血病脑膜、颅骨和脑浸润。患者遂入组接受PD-1Ab21-CD19 CAR-T细胞回输治疗。
结果显示:治疗半个月后,脑脊液和骨髓中均未检测出残留白血病细胞;治疗1个月后,增强核磁检查显示脑部肿瘤显著缩小,最大瘤块缩小至原来的1/6;治疗3个月后,核磁检查显示脑部肿瘤完全消失,患者达到完全缓解(CR)。目前,患者仍在持续随访中。值得关注的是,69岁的她创造了国内CAR-T治疗患者年龄的新高!
▼本例患者CAR-T治疗前后,脑部肿瘤的核磁共振检查对比
▲图源“CD BIOPHARMA”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
AUTO4 CAR-T暴击外周T细胞淋巴瘤,中位总生存期翻倍,两位患者肿瘤"消失"并维持长效代谢缓解
全球知名期刊《Nature Medicine》近期报道了一项“AUTO4CAR-T细胞疗法治疗复发或难治性外周T细胞淋巴瘤(r/rPTCL)”的1/2期LibraT1临床研究(NCT03590574)数据。
研究共纳入76例r/rPTCL患者,平均年龄为55岁(范围:34-63岁)。其中,80%的患者处于III/IV期疾病阶段,28例(37%)患者为TRBC1+。所有入组患者均接受AUTO4CAR-T细胞回输治疗。
研究结果显示:在9例可评估疗效的患者中,通过PET-CT检测,AUTO4输注后任意时间的最佳总体反应率[完全反应(CR)+部分反应(PR)]高达66.6%(6/9)。其中,4例患者达到完全代谢反应(CMR),2例患者获得部分缓解(PR)。在接受450×10⁶CAR-T细胞(最高剂量)治疗的4例患者中,3例(75%)在治疗第1个月就达到CMR,且其中2例在18个月后仍维持CMR,这表明AUTO4CAR-T疗法有可能在部分患者中诱导长期缓解。值得注意的是,2例达到PR的患者,在未接受新抗癌药物治疗的情况下,生存期均超过12个月。
▲图源“Nature Medicine”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
此外,在全部入组的10例患者中,中位无进展生存期(PFS)为4.7个月[95%CI:0.9-不可评估(NE)]。第9个月时,PFS率约为90%(95%CI:47.3,98.5);第18个月时,PFS率约为78.8%(95%CI:38.1,94.3)。随访结束时,有8例患者存活,中位总生存期(OS)达13.8个月,远超该类患者队列小于6个月的历史平均值。
▲图源“Nature Medicine”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
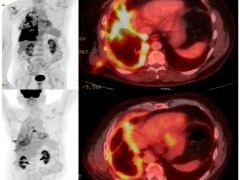
值得重点关注的是,有两位患者(47岁和55岁)的治疗效果极具代表性。通过对比他们接受AUTO4治疗前、治疗第1个月、第12个月时的FDG PET-CT成像结果发现,两位患者在接受治疗后,均实现并维持了长期的完全代谢反应(CMR)。
▲图源“Nature Medicine”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
探秘CAR-T细胞抗癌密码,中美获批产品大盘点,多癌种免费临床试验火热招募中……
CAR-T细胞制备过程与抗癌原理
CAR-T细胞(嵌合抗原受体T细胞)疗法是一种以T细胞介导的CAR为基础的细胞免疫疗法,通俗地讲,就是利用基因转导技术,在T细胞上安装一个名为CAR的“导航头”,回输到患者体内后,可以精准地找到癌细胞,并将其绞杀。
CAR-T 细胞通过白细胞分离术初步收集患者来源的白细胞。随后,这些T细胞被运送到生物制药设施进行基因改造,使其能够在其表面表达 CAR。此后,工程化的 CAR-T 细胞进行体外扩增,然后送回医院输注到患者体内(详见下图)。
▲图源“Heliyon”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
全面盘点中美CAR-T获批产品
目前,美国FDA批准商业化上市的CAR-T细胞产品主要有七款,主要用于治疗不同的血液系统恶性肿瘤,包括B细胞白血病和淋巴瘤、套细胞淋巴瘤、多发性骨髓瘤等。而中国获批上市的CAR-T产品主要有五款,包括阿基仑赛、瑞基奥仑塞、伊基奥仑赛、纳基奥仑赛、泽沃基奥仑(详见下表)。
▲数据源自“Front Immunol”,医学部整理汇总
CAR-T多癌种临床试验招募开启,或享"天价"疗法免费治疗
好消息是,目前有多款CAR-T临床实验正在火热招募中,主要针对Claudin18.、C3、GUCY2C、PSMA、CEA、间皮素(mesothelin)、MUC-1、BCMA、CD1、CD20等靶点。以及胰腺癌、胃癌、肝癌、结直肠癌、神经胶质瘤、肺癌、多发性骨髓瘤、多发性骨髓瘤、弥漫大B细胞淋巴瘤等癌种。
做过基因检测的患者,可自行查看基因检测报告,一旦发现存在上述突变,可将近期病理报告、基因检测报告等资料汇总后,提交至医学部,初步评估是否有机会参加相关临床试验。一旦审核通过,有机会获得”天价“疗法免费治疗的机会。看不懂检测报告或想要明确相关靶点的患者,也可联系医学部,详细解读报告或了解检测详情。
小编寄语
时至今日,CAR-T 细胞疗法在血液系统恶性肿瘤的治疗领域已取得突破性进展,众多患者从中受益。令人欣慰的是,近年来全球的研究人员从未停止探索的脚步,持续钻研各种新型策略,致力于降低肿瘤抗原异质性,打破免疫抑制的困境,为癌症患者带来更多希望!
好消息是,目前我国正有多款CAR-T临床试验正在招募中,主要针对B细胞淋巴瘤、T细胞淋巴瘤、T细胞白血病(T-ALL)、非霍奇金淋巴瘤、急性淋巴细胞白血病、胰腺癌、胃癌、肝癌、结直肠癌、间皮瘤、卵巢癌等癌种!想寻求CAR-T细胞或国内外其他前沿抗癌技术(如TIL、TCR-T、NK细胞、益生菌等)帮助的患者,可将出院小结、详尽的病理报告、治疗经历等资料,提交至全球肿瘤医生网医学部,进行初步评估或申请国内外抗癌专家会诊。
参考资料
[1]Cwynarski K,et al.TRBC1-CAR T cell therapy in peripheral T cell lymphoma: a phase 1/2 trial[J]. Nature Medicine, 2024: 1-7.
https://www.nature.com/articles/s41591-024-03326-7
[2]Wang C,et al.CAR-T cell therapy for hematological malignancies: History, status and promise[J]. Heliyon, 2023, 9(11).
https://www.cell.com/heliyon/fulltext/S2405-8440(23)08984-3
[3]https://www.onclive.com/view/optimized-tandem-cd19-cd20-directed-car-t-plus-asct-elicits-durable-responses-in-r-r-b-cell-lymphomas
[4]https://www.cdbiopharma.com/enyy_details_787921.html