早期甲状腺癌术后五年生存率超99%,但要注意,这5件事一定要做好
一、早期甲状腺癌为何能实现超高生存率
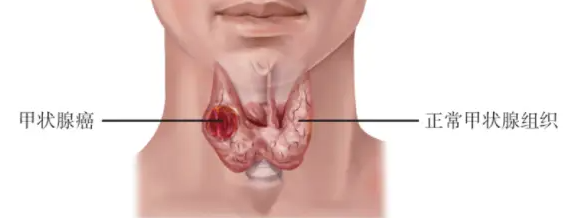
甲状腺癌和正常甲状腺组织对比
甲状腺癌被称为“懒癌”并非毫无根据,最新数据显示,我国早期甲状腺癌(Ⅰ期)的五年生存率已突破99%,日本和美国的部分研究甚至达到100%(参考来源:中国癌症中心2022报告)。这得益于以下优势:
1.病理特性温和:乳头状癌占比超85%,生长缓慢且转移率低;
2.早筛技术普及:高分辨率超声让微小癌(<1cm)检出率提升3倍;
3.治疗手段精准:达芬奇机器人手术可保留甲状旁腺,降低并发症风险。
> 数据延伸:日本甲状腺协会研究显示,直径<1cm的乳头状癌患者,10年无复发生存率达98.7%
二、术后防复发的「黄金五年」管理策略
虽然生存率高,但术后五年仍是复发关键期,研究表明,80%的复发发生在术后3年内(参考来源:《甲状腺癌诊疗指南2022》)。需从以下维度建立防护体系:
1.终身随访机制
- 血清学监测:每6-12个月检测甲状腺球蛋白(Tg)+Tg抗体,当Tg>2ng/ml时需警惕复发;
- 影像学检查:术后6个月首次颈部超声,低危患者5年后可延长至2年/次;
- 分子检测:BRAF V600E突变患者需加强监测(突变率与复发风险正相关)。
2.TSH抑制治疗的精准调控
注:TSH中文叫促甲状腺激素,是反映甲状腺功能最敏感的指标。
- 高危患者:TSH控制在0.1mU/L以下(美国甲状腺协会ATA指南);
- 中危患者:TSH维持0.1-0.5mU/L;
- 低危患者:TSH可放宽至正常范围上限(2.0mU/L)。
3.碘131治疗的选择性应用
- 清甲治疗:肿瘤直径>4cm或淋巴结转移>5枚需行碘131;
- 清灶治疗:远处转移患者需多次治疗,治疗前需严格低碘饮食2周(参考来源:《核医学杂志》2023)。
4.生活方式的科学干预
- 饮食管理:术后2周低脂饮食,单侧腺叶切除者限制海带/紫菜,全切除者无忌碘要求;
- 运动处方:术后3个月内避免剧烈运动,推荐瑜伽/游泳等低强度锻炼;
- 心理调节:术后抑郁发生率高达25%,建议加入患者互助社群。
三、警惕术后六大「隐形杀手」
尽管生存率高,但并发症仍可能影响生活质量:
| 并发症类型 | 发生率 | 预警信号 | 应对措施 |
| 喉返神经损伤 | 0.3-15.4% | 声音嘶哑>2周 | 喉镜检查+神经修复术 |
| 甲状旁腺功能减退 | 2-15% | 手足麻木/抽搐 | 钙剂+骨化三醇 |
| 乳糜漏 | 1-3% | 引流量>500ml/日 | 低脂饮食+负压引流 |
| 颈部瘢痕挛缩 | 20-30% | 活动受限 | 术后2周开始颈部操训练 |
四、前沿技术,DC+NK细胞疗法重塑免疫防线
传统治疗手段之外,免疫细胞疗法正在改写术后防复发格局:
1.DC细胞:激活抗癌「雷达系统」
- 作用机制:提取患者自身树突状细胞,负载肿瘤抗原后回输,可激活特异性T细胞;
- 临床数据:日本研究显示,DC疗法使术后复发率降低42%(参考来源:《Cellular Immunology》2023);
- 治疗方案:8次注射,间隔2周,形成长期免疫记忆。
2.NK细胞:启动天然免疫「杀手程序」
- 双重作用:直接杀伤肿瘤细胞+分泌细胞因子调节免疫微环境;
- 联合优势:与DC细胞协同,可使肿瘤杀伤效率提升3-5倍;
- 治疗周期:4次回输,每次间隔1个月。
3.联合治疗方案
- 适用人群:中高危复发风险患者(肿瘤>2cm或淋巴结转移);
- 治疗流程:术后1个月开始,先DC后NK交替进行;
- 疗效追踪:每3个月检测肿瘤标志物,6个月复查PET-CT。
五、复查黄金时间表
| 时间节点 | 必查项目 | 可选项目 |
| 术后1个月 | 甲功+Tg | 颈部超声 |
| 术后3个月 | 颈部超声+胸片 | 全身骨扫描 |
| 术后6个月 | 甲状腺球蛋白抗体 | 基因检测 |
| 术后1年 | 胸部CT | PET-CT |
六、从绝望到新生的患者故事
> 案例分享:32岁的李女士术后3年发现Tg持续升高,通过DC+NK细胞治疗6个月后,颈部淋巴结转移灶完全消失,现已正常怀孕生子。
七、科学管理+前沿技术=生命保障
早期甲状腺癌的高生存率印证了「早发现早治疗」的重要性,术后规范随访、精准药物控制、健康生活方式与免疫细胞疗法的结合,为患者构筑起多重防护网,若您或家人正处于康复期,如果有什么问题的话,可以随时咨询全球肿瘤医生网,帮助患者5年生存率从99%的希望变为100%的现实。
参考文献:
1. 《甲状腺癌诊疗指南(2022版)》国家卫健委
2. 日本甲状腺协会2023年年会报告
3. 《Cellular Immunology》DC细胞临床研究
4. 中国抗癌协会甲状腺癌专业委员会白皮书