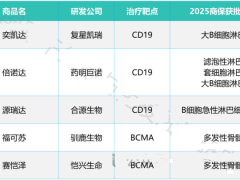
又一款国研CART细胞疗法获得药监局突破性疗法认定,疾病控制率96.1%
2025年3月2日,科济生物研发的一款CAR-T疗法——satricabtagene autoleucel(简称“satri-cel”,编号CT041),获中国国家药品监督管理局(NMPA)药品审评中心(CDE)授予突破性疗法认定(BTD),用于既往接受至少两种疗法失败的Claudin18.2阳性的晚期胃/胃食管连接部癌(G/GEJ)的治疗。
科济生物创始人李宗海博士表示:“我们非常高兴satri-cel获得突破性疗法认定。目前,我们正全力推进satri-cel新药申请的准备工作,这将加快其审批进程,使这种疗法能够尽快惠及患者”。据悉,该公司计划于2025年上半年向国家药监局提交satri-cel的新药申请(NDA),如果能顺利获批,satri-cel有望成为全球首创产品,让我们拭目以待,小编也将为您持续进行后续报道!
▲截图源自“PR Newswire”
中国首创CLDN18.2 CAR-T疗法satri-cel荣登《Nature Medicine》,疾病控制率高达96.1%
Satri-cel是一种针对蛋白质Claudin18.2的自体CAR-T细胞候选产品,旨在治疗Claudin18.2阳性的实体肿瘤,主要针对胃癌/胃食管交界处癌(GC/GEJ)以及胰腺癌(PC)。2022年1月,Satri-cel就曾获得美国FDA授予的再生医学先进疗法(RMAT)资格,用于Claudin18.2阳性的晚期胃癌/胃食管交界处癌(GC/GEJ)肿瘤的治疗;还曾于2020年9月获得美国FDA颁发的孤儿药资格,用于胃癌/胃食管交界处癌(GC/GEJ)的治疗。
2024年,美国临床肿瘤学会(ASCO)会议上,北京大学肿瘤医院的研究团队公布了“satri-cel(CT041-CG4006)治疗胃肠道肿瘤的1期临床试验(NCT03874897)”最终结果,引发了学界的巨大轰动。这是全球首个公开的CLDN18.2-CAR-T细胞治疗实体瘤的临床研究数据,该成果同步发表于国际顶级期刊《Nature Medicine》杂志。
本次研究共入组98例CLDN18.2阳性晚期胃肠道肿瘤患者,包括胃癌(n=73)、胰腺癌(n=10)、胆道癌(n=4)、肠癌(n=8)和其他肿瘤(n=3)。入组接受不同剂量的satri-cel(即CAR-T细胞)回输治疗,回输剂量分别为2.5×10^8(89例患者)、3.75×10^8(6例患者)、5.0×10^8(3例患者)。中位随访期为29.7(范围:1.2,35.5)个月。
结果显示:所有患者(N=98)的客观缓解率(ORR)达到37.8%,疾病控制率(DCR)达到75.5%,中位无进展生存期(PFS)为4.4个月(95% CI:4.0, 6.0),中位总生存期(OS)为8.4(95% CI:7.0, 10.0)个月。
在接受CT041单药治疗的疗效可评估的胃癌(GC)患者(n=47)中,有可测量病变患者的客观缓解率(ORR)为57.4%,疾病控制率(DCR)高达83.0%。所有疗效可评估的胃癌(GC)患者(n=55),中位无进展生存期(PFS)为5.8个月(95%CI:4.2,8.4),中位总生存期(OS)为9.7(95%CI:7.1,14.4)个月。
▲图源“ASCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
综上,Satri-cel/CT041 在接受过大量治疗的 CLDN18.2 阳性晚期胃肠道癌患者中表现出良好的安全性和令人鼓舞的疗效。
CAR-T细胞疗法的在研癌种及靶点
目前有多款CAR-T治疗的临床试验正在招募中,主要针对以下癌种及靶点:
1、血液肿瘤
①CD19:用于淋巴瘤、白血病、B细胞急性淋巴细胞白血病等;
②BCMA:用于多发性骨髓瘤等;
③CD20:用于淋巴瘤、B细胞非霍奇金淋巴瘤、弥漫大B细胞淋巴瘤等;
④CD33:用于急性髓细胞白血病等;
⑤CD3:用于多发性骨髓瘤等;
⑥CD7:用于外周T细胞淋巴瘤等;
⑦CD4:用于淋巴瘤等;
⑧CLL-1:用于急性髓细胞白血病等;
⑨EBV:用于淋巴瘤等。
2、实体瘤
①GPC3:用于肝癌等;
②GUCY2C:用于结直肠癌的治疗;
③PSMA:用于治疗前列腺癌等;
④Claudin18.2:用于胰腺癌、胃癌等;
⑤EGFRvII:用于治疗神经胶质瘤、头颈部肿瘤等;
⑥MUC-1:用于治疗肺癌、胃癌、胰腺癌、肝癌、结肠癌等;
⑦CEA:用于治疗胰腺癌、肺癌、结肠癌、胃癌、乳腺癌等;
⑧间皮素(mesothelin):用于治疗间皮瘤、胰腺癌、卵巢癌、肺癌等;
⑨B7-H3:用于治疗尤文肉瘤、髓母细胞瘤、肾母细胞瘤、神经母细胞瘤、横纹肌肉瘤、特别难以治疗的脑干肿瘤(DIPG)等。
做了基因检测的病友可以拿出报告看看,一旦存在上述癌症或突变,可将近期影像学检查、病理检查、治疗经历等资料,提交至医学部,进行初步评估或了解详细的入列标准。看不懂的基因检测报告的病友,也可致电医学部解读报告。
CD19 CAR-T细胞暴击三线复发或难治性弥漫大B细胞淋巴瘤,完全缓解率超67%
弥漫性大B细胞淋巴瘤(DLBCL)是最为常见的侵袭性B细胞淋巴瘤。在美国,约占美国非霍奇金淋巴瘤(NHL)病例的30%,复发或难治(R/R)患者的病程往往侵袭性更强,可选择的挽救治疗手段有限,预后通常不佳。因此,开发新的治疗方案迫在眉睫。
近日《Hemato》报道了一项“应用CD19CAR-T细胞,作为复发或难治性弥漫性大B细胞淋巴瘤(DLBCL)三线或后续治疗”的临床研究数据。本次共入组82例为复发或难治性弥漫性大B细胞淋巴瘤(R/R DLBCL)患者,接受了3种抗CD19CART细胞产品中的1种:axi-cel(64.6%)、liso-cel(18.3%)和tisa-cel(17.1%)。
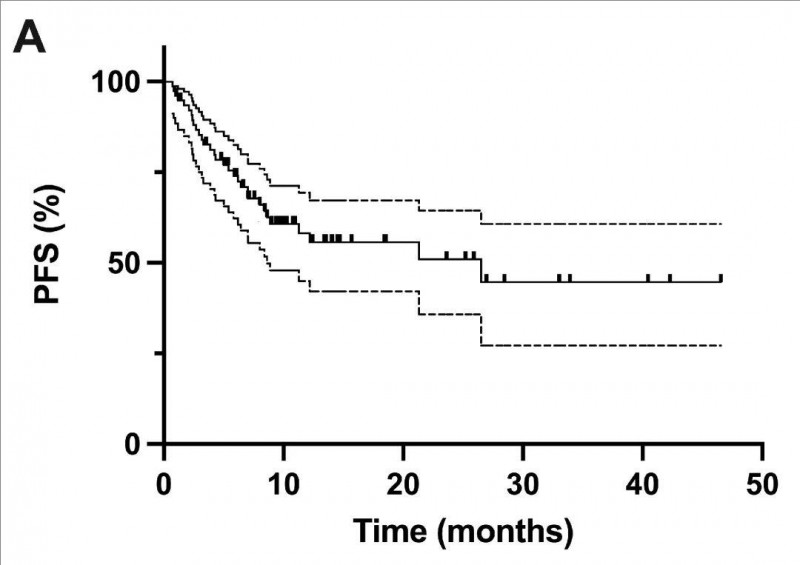
结果显示:在接受抗CD19CAR-T细胞输注的82例患者中,最佳总体缓解率(ORR)为74.4%(95%CI,64.9~83.8),完全缓解率(CR)为67.1%(95%CI,56.9~77.2)。从CAR-T细胞输注开始,中位无进展生存期(PFS)为26.5个月(95%CI,8.6个月无法估计)。随访12个月、24个月的中位无进展生存(PFS)率分别为58.2%(95%CI,44.9%~69.3%)、51.0%(95%CI,35.8%~64.4%)(详见下图)。
▼从CAR-T细胞输注时起的中位无进展生存期(PFS)
▲图源“MDPI”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:虚线代表95%置信区间的上限和下限。
随访12个月、24个月的中位总生存(OS)率分别为77.5%(95%CI,64.7%至86.2%)、8.3%(95%CI,39.8%至72.9%)(详见下图)。
▼从CAR-T细胞输注时起的中位总生存期(OS)
▲图源“MDPI”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:虚线代表95%置信区间的上限和下限。
AUTO4 CAR-T震撼出击:无进展生存率达90%,治疗1个月已有患者实现肿瘤奇迹"消失"
英国研究团队近日在全球知名期刊《Nature Medicine》上,公布了一款名为“AUTO4”新型CAR-T细胞疗法的1/2期LibraT1临床研究(NCT03590574)数据。本次共纳入76例复发或难治性外周T细胞淋巴瘤(r/r PTCL)患者,平均年龄55岁(年龄范围为34至63岁),其中80%患有III/IV期疾病,28例(37%)为TRBC1+。这些患者入组接受AUTO4 CAR-T细胞回输治疗。
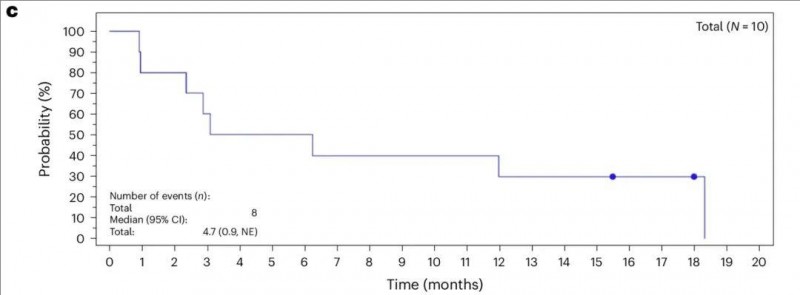
结果显示:在全部入组患者(n=10)中,中位无进展生存期(PFS)为4.7个月[95%置信区间(CI)0.9,不可评估(NE)]。第9个月时的PFS率约为90%(95%CI:47.3,98.5),第18个月的PFS率约为78.8%(95%CI:38.1,94.3)(详见下图)。有8例患者在最后一次随访时存活,中位总生存期(OS)持续时间为13.8个月,远超该患者队列小于6个月的历史平均值。
▲图源“Nature Medicine”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
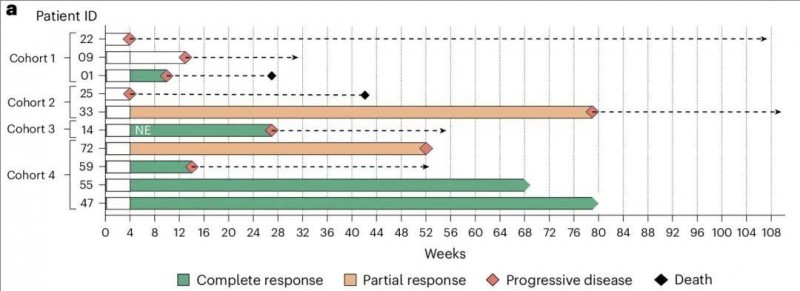
此外,在所有可评估反应(n=9)的患者中,通过PET-CT显示,AUTO4输注后任何时间的最佳总体反应率[完全反应(CR)+部分反应(PR)]高达66.6%(6/9)。具体而言,有4例观察到完全代谢反应(CMR),2例患者达到部分缓解(PR)。此外,在接受450×10⁶CAR-T细胞(最高剂量)治疗的4例患者中,3例(75%)在治疗第1个月即达到完全代谢反应(CMR),其中2例在18个月后仍保持CMR。这表明AUTO4 CAR-T可能在部分患者中诱导长期缓解。值得注意的是,2例达到部分反应(PR)的患者,在未接受任何新抗癌药物的情况下,生存期超过12个月。
▲图源“Nature Medicine”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
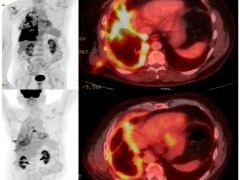
值得一提的是,有两位患者(分别为47岁和55岁)尤为典型。下图展示了这两位患者在接受AUTO4治疗前、治疗第1个月、第12个月时的FDG PET-CT成像结果。从图中可以看出,在接受AUTO4治疗后,这两例患者均维持了长期完全代谢反应(CMR)(详见下图)。
▲图源“Nature Medicine”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
小编寄语
在现代医学的漫长探索之路上,CAR-T细胞疗法宛如一颗璀璨新星,在恶性肿瘤,尤其是血液肿瘤治疗领域成功实现重大突破,为众多饱受病痛折磨的患者带来希望曙光,使他们得以重获新生,开启全新人生篇章。
令人振奋的是,当前我国CAR-T研发事业开展得如火如荼,呈现出“百家争鸣”的蓬勃景象。以驯鹿医疗、复星凯特、科济生物、传奇生物等一众领军企业,积极投身CAR-T的研发浪潮,且已取得令人瞩目的成果。如果您也想寻求CAR-T细胞疗法,或其他前沿抗癌技术(如TIL、TCR-T、NK细胞等)的帮助,可将治疗经历、近期病理报告、影像学资料等,提交至全球肿瘤医生网医学部,进行初步评估或申请国内外抗癌专家会诊。
参考资料
[1]QI C,et al.Claudin18. 2-targeted chimeric antigen receptor T cell-therapy for patients with gastrointestinal cancers: Final results of CT041-CG4006 phase 1 trial[J]. 2024.
https://meetings.asco.org/abstracts-presentations/232455
[2]Sridhar A,et al.Real-World Outcomes of Anti-CD19 Chimeric Antigen Receptor (CAR) T-Cell Therapy for Third-Line Relapsed or Refractory Diffuse Large B-Cell Lymphoma: A Single-Center Study[J]. Hemato, 2025, 6(1): 3.
https://www.mdpi.com/2673-6357/6/1/3
[3]Cwynarski K,et al.TRBC1-CAR T cell therapy in peripheral T cell lymphoma: a phase 1/2 trial[J]. Nature Medicine, 2024: 1-7.
https://www.nature.com/articles/s41591-024-03326-7