《自然通讯》震撼发布GOCAR-T产品BPX-601 CAR-T细胞疗法I期临床试验数据,治疗胰腺癌、前列腺癌6个月改写治疗格局
近年来,以CAR-T细胞为代表的过继性免疫细胞疗法已成为某些血液系统恶性肿瘤的成熟治疗方法,反应率显著。目前,已有多款CAR-T细胞疗法相继在中国和美国获批上市。
然而,CAR-T细胞疗法在实体瘤治疗领域的应用一直受限,其主要原因包括易受T细胞衰竭的影响、扩增能力和持久性受限,以及免疫抑制性肿瘤微环境等因素的制约。
不过值得欣慰的是,近期,全球权威期刊《Nature》的子刊《Nature Communications(自然通讯)》杂志,报道了一项令人振奋的研究成果:转基因自体GoCAR-T®细胞产品——BPX-601,在治疗转移性胰腺癌(mPDAC)、去势抵抗性前列腺癌(mCRPC)的1期剂量递增试验展现出良好疗效,为攻克实体瘤带来了新的曙光!
BPX-601:通过药理学方式激活的新型CAR-T细胞,克服胰腺癌、前列腺癌的治疗限制
为了克服实体瘤中组成型激活CAR-T细胞方法存在的局限性,我们研发出一种全新方法——BPX-601,即通过药理学手段激活CAR-T细胞,以此激发抗肿瘤活性。
BPX-601是一种靶向前列腺干细胞抗原(PSCA)的自体GoCAR-T®细胞产品,它采用“3+3”剂量递增设计,含有可诱导的 MyD88/CD40 ON-switch,可对小分子rimiducid(曾用名AP1903)作出反应,用于转移性胰腺癌(mPDAC)、去势抵抗性前列腺癌(mCRPC)的治疗。
▲截图源自“nature communications”
BPX-601 CAR-T细胞1期临床研究公布,6个月内保持稳定至改善
《Nature Communications(自然通讯)》杂志报道的“BPX-601 CAR-T细胞的1期临床研究(NCT02744287)”,共入组24例转移性胰腺癌(mPDAC)患者、9例去势抵抗性前列腺癌(mCRPC)患者,入组接受BPX-601 CAR-T细胞治疗。其中29名患者(88%)以某种方式接受了rimiducid治疗,19名患者接受了单剂量治疗,10名患者接受了每周剂量治疗(剂量数范围为2~48)。
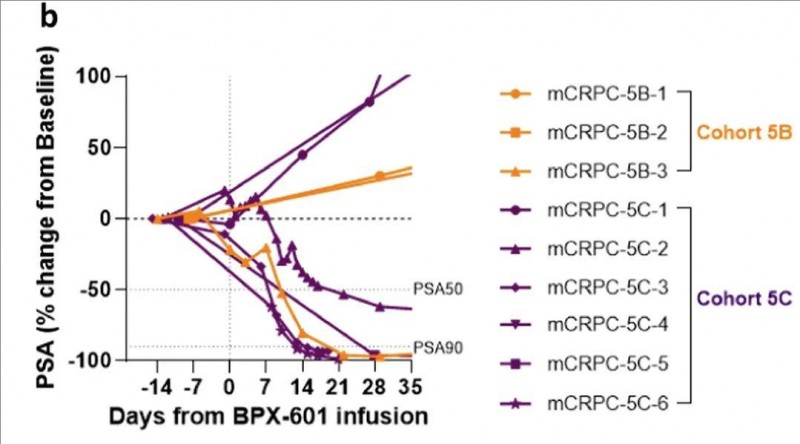
结果显示:BPX-601与rimiducid在接受过大量治疗的mCRPC患者中表现出令人鼓舞的抗肿瘤活性,9例患者中有5例(55.6%)出现血清前列腺特异性抗原(PSA)下降≥50%(PSA50反应);其中4例出现PSA90反应(即PSA水平下降≥90%)(详见下图)。
▼蜘蛛图显示BPX-601细胞输注后第1个月内,每个患者的血清前列腺特异性抗原(PSA)反应动力学
▲图源“nature communications”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
此外,6例可评估疗效的患者(33.3%)中,有2例出现部分反应(PR),1例患者淋巴结病变稳定超过1年。两例仅有骨病变的去势抵抗性前列腺癌(mCRPC)患者中,有1例出现PSA90反应,且骨扫描结果6个月内保持稳定至改善(详见下图)。
▼在治疗前和 BPX-601 细胞输注后第 42 天的计算机断层扫描对比
▲图源“nature communications”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:
①放射图像显示:去势抵抗性前列腺癌(mCRPC)患者(mCRPC-5B-3),在输注BPX-601细胞+单次输注rimiducid后,肿瘤缩小。
②肿瘤部位用橙色箭头指示。
小编寄语
时至今日,CAR-T 细胞疗法在血液系统恶性肿瘤的治疗领域已取得突破性进展,众多患者从中受益。然而,在实体瘤治疗方面,其效果仍存在一定局限性。这主要是因为实体瘤内部 T 细胞浸润程度较低,同时免疫抑制性的肿瘤微环境也在从中作梗,阻碍了 CAR-T 细胞疗法充分发挥作用。令人欣慰的是,近年来全球的研究人员从未停止探索的脚步,持续钻研各种新型策略,致力于降低肿瘤抗原异质性,打破免疫抑制的困境,为实体瘤患者带来更多希望。《自然通讯》杂志发布的这项研究结果表明,GoCAR-T® 细胞的药理学激活是可行的,并且可能提供一种有希望的途径来控制嵌合抗原受体-T 细胞活性,并持续剂量优化以提高耐受性。
值得欣慰的是,我国CAR-T研发正在如火如荼地进行,并呈现出“百家争鸣” 的繁荣景象。驯鹿医疗、复星凯特、科济生物、传奇生物等众多制药巨头纷纷投身于 CAR-T 的研发浪潮,并且已经取得了令人瞩目的成果,且已有部分幸运患者实现了完全缓解!如果您想寻求CAR-T细胞或国内外其他前沿抗癌技术(如TIL、TCR-T、NK细胞、益生菌等)的助力,可将出院小结、详尽的病理报告、治疗经历等资料,提交至全球肿瘤医生网医学部,进行初步评估或申请国内外抗癌专家会诊。
参考资料
[1]Stein M N,et al.PSCA-targeted BPX-601 CAR T cells with pharmacological activation by rimiducid in linkstatic pancreatic and prostate cancer: a phase 1 dose escalation trial[J]. Nature communications, 2024, 15(1): 10743.
https://www.nature.com/articles/s41467-024-53220-6