癌症是怎么转移扩散的,癌症转移后怎么治疗好
在全球范围内,每年约有 1800 万人被确诊患有癌症。过去 30 年间,随着早期癌症检测技术的问世、创新治疗手段的涌现,以及靶向药物、免疫检查点抑制剂等的应用,癌症治疗手段得以迅速发展,癌症幸存者人数也有所增加。然而,癌症转移仍然是导致患者死亡的主要原因,世界卫生组织的数据显示,超过 90% 的癌症相关死亡由癌症转移所致。
2024 年 8 月 2 日,南京医科大学研究团队在全球著名期刊《Nature》上,发表了一篇题为“肿瘤转移的机制洞察和治疗干预:最新进展和观点”的研究论文。在这篇综述中,该团队从多个角度阐述了肿瘤转移过程中的遗传转变,并探讨了具有前瞻性的治疗干预措施。本文对目前癌症转移方面的最新研究进展进行了总结,同时对未来开发新疗法的可能性进行了展望,例如利用癌症免疫疗法、细胞疗法等对抗癌症转移,提高生存率,期待有朝一日,人类能够彻底攻克癌症!
南京医科大学团队深度解析肿瘤转移机制与原因,从源头破解癌症复发转移难题
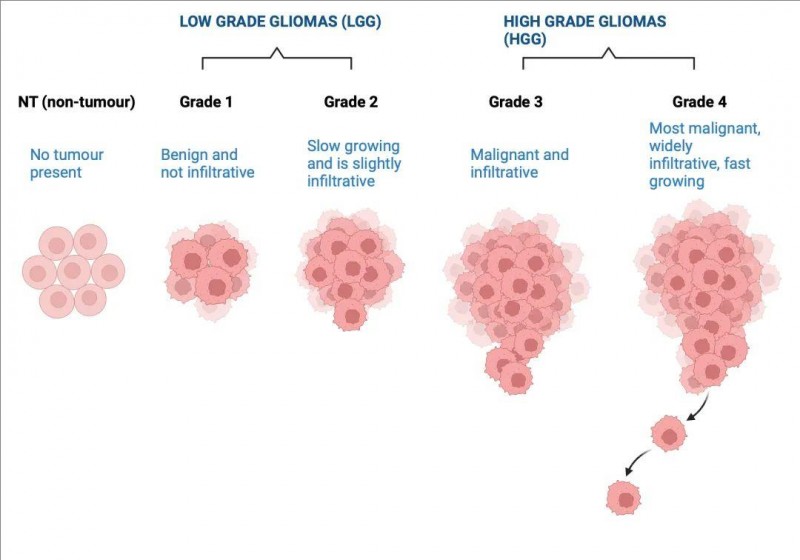
癌症转移是癌症的一个关键特征,也是导致癌症相关死亡的主要原因。转移过程复杂且成功率低,其中包含了一系列连续步骤,同时具有随机成分。它不仅是患者致死的主因,还在癌症的诊断与治疗上带来了巨大挑战。深入探究转移性癌症的发病机制及其发展进程,有助于实现更精准的诊断,以及为有效治疗干预提供支撑,正所谓“知己知彼百战不殆”。
肿瘤转移过程
肿瘤的转移是由一系列的动态事件所组成的,最终会使得癌症患者的存活率大大降低。为转移至远端器官,肿瘤细胞及其相关因子会借助多种体液系统,在机体内实现传播。例如,血液和淋巴循环系统的流动机制,就常被癌细胞利用,以提高自身从原发肿瘤处外渗和转移的效率。在这一过程中,体液的流速、血管大小以及剪切应力等因素,都会对循环中癌细胞的存活率产生影响。
新南威尔士大学的 Paul Timpson 教授与斯特拉斯堡大学的 Jacky G. Goetz 教授展开合作,对循环肿瘤细胞和肿瘤相关因子利用体液进行转移的相关机制,进行了全面综述。同时,两位教授对体液引发的转移性级联生物学问题,也进行了详细阐释,这一研究成果为深入了解转移中的癌细胞,提供了全新策略。
▲图源“nature”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
从时间线的角度来看,目前存在两种被广泛接受的肿瘤转移模型:
第一种是线性模型,该模型认为,转移性肿瘤细胞会在大家通常所认为的癌症晚期阶段,才在不同的器官中进行定植。也就是说,肿瘤细胞从原发部位开始,按照较为有序的进程逐步发展,直至晚期才具备转移到其他器官并扎根生长的能力。
第二种是平行模型,此模型主张癌细胞在癌症早期阶段便开始扩散。这种模型与线性模型的区别主要体现在在于转移性细胞带了多少与原发性肿瘤相同的基因,以及它们是否独立于原发性肿瘤细胞的进化模式。
▲图源“BioRender”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
基因突变对肿瘤转移的影响
在转移相关基因的研究领域,促进肿瘤转移的基因吸引着众多科研人员的目光。驱动基因在肿瘤的发生过程中,被视为具有高度特异性的关键因素。一旦发生致癌突变,恶性细胞便会获得一系列危险特性,如不受控制的快速增殖能力,使其能够在体内肆意生长;具备躲避人体免疫系统监测的能力,从而逃过免疫防线的围剿;拥有突破组织边界、侵袭周围正常组织的能力;以及能够调节自身所处微环境,营造利于自身生存和发展的条件。
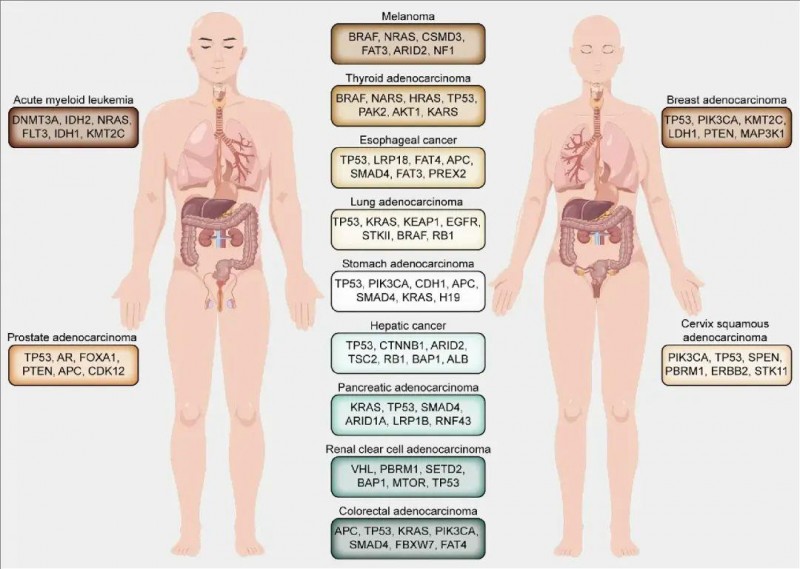
如下图罗列了常见癌症类型中重要的突变驱动基因。驱动基因发生突变后,会在恶性细胞内持续激发增殖信号,促使癌细胞不断分裂生长,同时还会诱发癌细胞的侵袭和转移行为,极大地增强了癌细胞的扩散能力。这些突变在相应癌症的起始、发展以及病情恶化的各个阶段都扮演着不可或缺的角色。正因为如此,它们有望成为极具潜力的治疗靶点,为癌症治疗开辟新的途径。
▲图源“nature”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:该图对一系列癌症进行了分类,包括黑色素瘤、甲状腺腺癌等,并确定了与每种癌症相关的最常发生突变的驱动基因。
癌症为何会发生复发或转移
1、癌症本身特性——擅长"休眠"及"隐藏"
癌细胞极其狡猾且能隐藏较长时间,约20%~45%的雌激素受体阳性乳腺癌患者,可能会在成功治疗数年~数十年后复发。此外,初期抗癌治疗后,部分癌细胞可能处于“休眠状态”,更加雪上加霜的是,目前的影像学检查很难发现这些“休眠”的癌细胞。一旦人体免疫力降低或免疫功能紊乱时,这些幼年癌细胞,会从休眠状态复苏,从而造成癌症的复发或转移。
2、常规治疗未能完全清除体内的癌细胞
放化疗仅能杀死局部成年的癌细胞,但对部分低分化的幼年癌细胞的治疗效果并不理想。此外,手术治疗仅能切除已成形的肿瘤原发病灶,对于部分病理或影像学检查无法发现的“微转移”癌细胞或高危淋巴结,可能无法完全切除或清扫干净,从而埋下隐患,日后也可能形成转移灶。
3、免疫力低下
人体免疫系统由免疫器官(包括胸腺、扁桃体、淋巴、脾脏、肠道和骨髓的淋巴组织)、免疫细胞(包括T细胞、NK细胞、B细胞、巨噬细胞等)、分子(如抗体、细胞因子、趋化因子等)组成(详见下图)。它保护机体免受外来病原体的侵害、消灭癌细胞,并维持正常的身体功能。
4、癌症的复发风险依然存在
对于癌症患者而言,虽然通过各种治疗手段,将体内现存的癌细胞“消灭”了,但如果治疗后未能及时去除致癌的高危因素,也会导致癌症卷土重来。比如,与戒烟的幸存者相比,维持中~重度吸烟习惯者,其肺癌的复发风险增加>7倍!因此,建议肺癌患者在治疗完成后,要积极戒烟,以免功亏一篑。
▼各类癌症复发率的评估
▲医学部整理汇总
癌症转移治疗路在何方?南京医科大学研究团队给出答案:癌症转移最怕这七大"神奇钥匙"
癌症的治疗方案丰富多样,具体治疗方法的选择取决于癌症的类型、所处分期以及患者个体情况等诸多因素。部分癌症患者仅需接受单一疗法便能取得一定疗效。然而,多数患者往往需要采用联合治疗与个性化治疗相结合的方式,例如将手术治疗与化疗、放疗中的一种或两种联用。
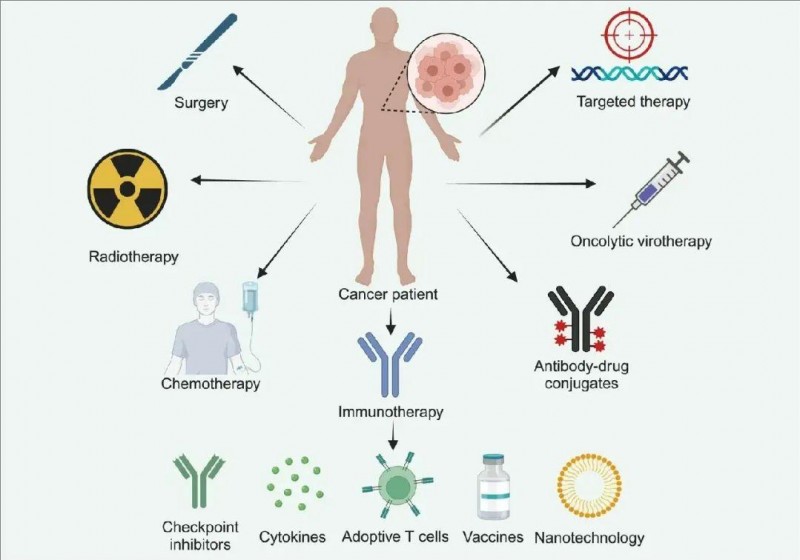
近年来,靶向治疗与免疫治疗领域取得了重大突破,这些创新疗法极大地变革了癌症治疗格局。其中,免疫治疗涵盖了免疫检查点抑制剂、细胞治疗、基于过继细胞转移(ACT)的免疫疗法、肿瘤疫苗以及纳米技术等多种手段。同时,一些新兴疗法也在蓬勃发展,如溶瘤病毒疗法和抗体药物偶联疗法,它们正朝着攻克癌症的目标不断迈进,为癌症患者带来新的希望。下面小编简单为大家盘点一下,南京医科大学研究团队在《Nature》杂志中提到的几大类常见的癌症治疗方法,以供癌友们参考。
▲图源“nature”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
01、传统治疗
当代癌症治疗通常采用手术、化疗和放疗等综合治疗方式。手术和放疗主要作为局部干预,而化疗则作为全身治疗,对播散性癌细胞和迁移到血液和淋巴系统的癌细胞产生细胞毒性作用。
1.手术治疗
手术切除仍然是原发性肿瘤或转移瘤的治疗基础,具有延长生存期和/或提高生活质量的潜在益处。研究已证明手术切除可改善转移灶局限性患者的疾病控制和生存率,尤其是在乳腺癌等伴有孤立性骨转移的病例中。尽管如此,但手术切除后,原发性肿瘤依然存在转移性复发的显著风险,如乳腺癌术后12~18个月是复发率的高峰。
2.化疗
化疗是全身干预的基石,主要针对易于广泛扩散或已经转移的肿瘤。在转移性乳腺癌中,尤其是三阴性乳腺癌亚型中,在没有可行的靶向治疗的情况下,化疗仍然是唯一的全身治疗选择,旨在通过靶向快速分裂的细胞来阻止肿瘤再生。然而,化疗虽然可以延长生存期并缓解症状,但很少能治愈或完全消除转移。
3.放射治疗
采用靶向辐射来消除肿瘤,仍然是局部治疗的关键方式。正电子发射断层扫描(PET)结合临床诊断可改善肿瘤的生物学特征,有助于解释潜在的治疗耐药性。然而,对于部分患者辐射可能会动员循环肿瘤细胞,无意中刺激肿瘤细胞扩散,促进随后的转移发展。加之,放疗可能会在杀伤癌细胞的同时,伤害周围正常的组织,引起放射性皮炎、心肌缺血、认知功能受损等一系列副作用,故而近年来提倡副作用更小、辐射部位更精准的新型放射治疗手段——即质子治疗。
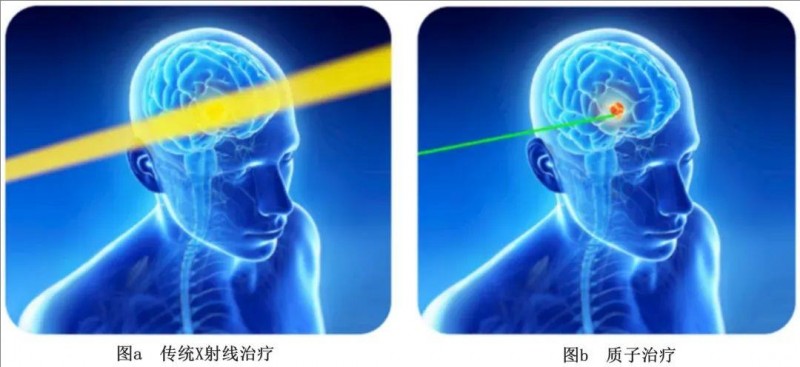
质子治疗虽然也属于放射治疗的一种,但它使用的是质子(即带正电的亚原子粒子),而非传统的X射线来杀死癌细胞。质子的速度可达到光速约三分之二,既能精确地靶向癌组织,同时可最大限度地减少附近健康组织和器官的暴露,从而在治疗癌症的同时,减少放射治疗的副作用,提高患者的生活质量,尤其适用于儿童和年轻人。
▼传统X射线放疗与质子治疗辐射范围对比
▲图源“MedStar Health”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
02、NK细胞疗法
NK 细胞是细胞毒性淋巴细胞,是先天淋巴细胞 (ILC) 的一个独特且经过精心调节的亚群。一旦激活,它们就会迅速对病毒感染或肿瘤发生作出反应,启动血液中受感染或肿瘤细胞的凋亡。广义上讲,NK 细胞可快速有效地抵抗转移性恶性肿瘤。
NK细胞显奇效,助力晚期结肠癌患者实现3年未复发奇迹
《癌症代表》杂志报道了一个应用“局部晚期结肠腺癌患者经NK细胞治疗后,3年未复发”的惊艳案例!
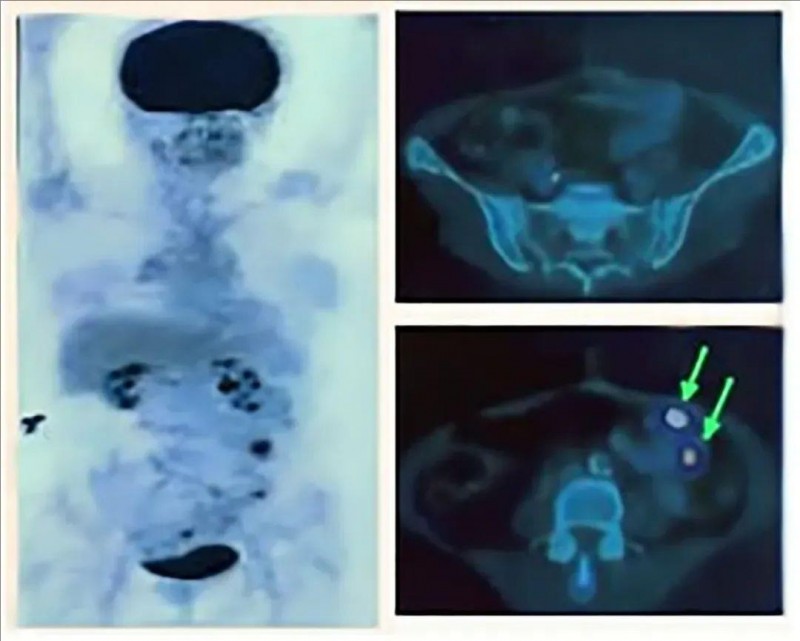
该患者是一位64岁女性,因横结肠肿瘤相关部分性肠梗阻、血性腹泻病史而就诊,最终确诊为横结肠腺癌阳性淋巴结受累(TNM期III),R0切除状态。术后两个月随访CEA水平为1.3 ng/mL。该患者未进行辅助化疗,6个月后进行PET扫描,结肠系膜淋巴结葡萄糖摄取阳性(详见图1)。
图1 切除术后6个月,腹部正电子发射断层扫描的轴向图
▲图源“Cancer Rep”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:腹部正电子发射断层扫描的轴向视图显示,结肠腔内以外的腹膜和结肠系膜区域的氟脱氧葡萄糖摄取情况(以浅箭头标记表示)。
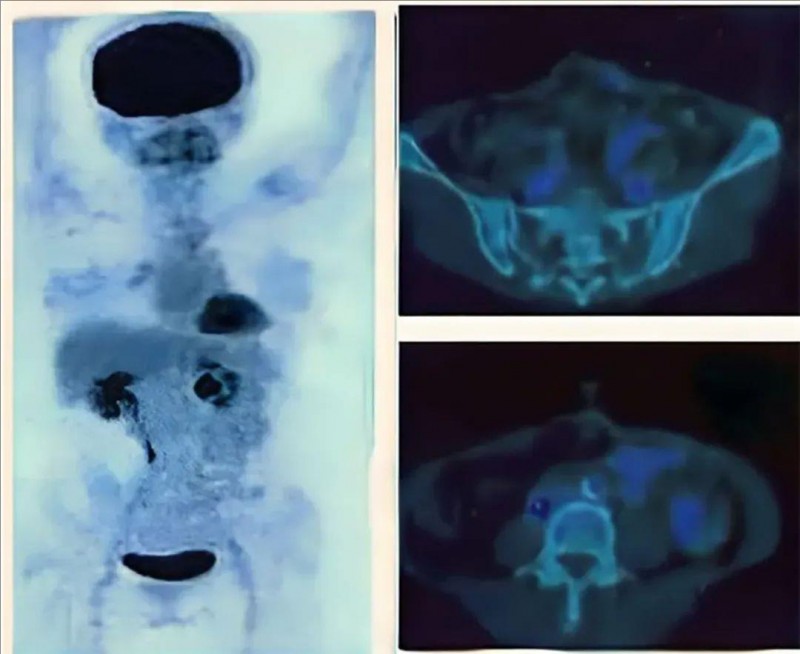
切除手术后,为预防肿瘤复发,该患者随后接受了2个周期的NK细胞治疗。在结肠癌确定性手术后3年的临床随访中,该患者对治疗耐受性良好,可以很好地耐受日常活动。PET-CT显示,未见更多的葡萄糖摄取,未报告免疫相关不良反应(详见图2)。截至2022年12月底,未见局部区域复发的症状和体征,也未见长期心肺发病率。
图2 接受NK细胞治疗且切除术后3年,腹部正电子发射断层扫描的轴向图
▲图源“Cancer Rep”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:自然杀伤细胞治疗后进行正电子发射断层扫描评估,在轴向视图显示,局部转移灶中,不再有氟脱氧葡萄糖摄取,且腹腔内也没有额外的摄取。
综上,自体NK细胞具有良好的效果,且耐受性良好,可作为局部晚期结肠腺癌免疫治疗的新选择,尤其适用于不适合接受标准化疗的患者。
国际前沿免疫疗法招募进行时:
①CAR-T疗法:正在招募肺癌、胰腺癌、肝癌、胃癌、结直肠癌、卵巢癌、复发/难治性淋巴瘤、多发性骨髓瘤等多类癌种。
②TCR-T疗法:正在招募鼻咽癌、晚期葡萄膜黑色素瘤、乙型肝炎病毒相关肝细胞癌、妇科恶性肿瘤(子宫内膜癌、卵巢癌)、血液系统恶性肿瘤等多类癌种。
③TILs疗法:正在招募黑色素瘤、肺癌、宫颈癌、乳腺癌、头颈部肿瘤等多款实体瘤。
④癌症疫苗:正在招募肺癌、肝癌、结直肠癌、食管癌、头颈癌、宫颈癌等多款癌种!
想参与上述临床试验的癌友,可将近期病理报告、影像学检查报告、完整的治疗经历等资料,提交至医学部,初步评估病情或了解详细的入排标准。
03、树突状细胞疫苗
树突状细胞(DC)作为专职的抗原呈递细胞,在免疫反应中扮演着极为关键的角色。它能够摄取外来抗原,经过内化处理后,将抗原信息呈递给 T 细胞,从而有效启动针对特定抗原的免疫应答。在树突状细胞的研究领域中,最具突破性的成果当属相关疫苗的研发。
DC疫苗联合厄洛替尼助晚期肺腺癌患者,实现587天零复发零转移奇迹
《医学病例报告杂志》近期报道了一个振奋人心的案例,一位晚期肺腺癌患者经DC疫苗联合厄洛替尼治疗后,实现587天零复发零转移奇迹!
该患者是一位63岁EGFR突变的晚期(Ⅲb期:T2aN3M0)肺腺癌患者,PD-L1表达不足1%,无间变性淋巴瘤激酶(ALK)表达,东部肿瘤协作组体能状态(PS)为0,器官功能正常,且未接受过化疗。该患者因无法耐受手术治疗,遂入组接受DC疫苗(WT1/MUC1-DC,即用MHC II类限制性WT1肽+MUC1肽疫苗冲击的树突状细胞)联合厄洛替尼治疗。
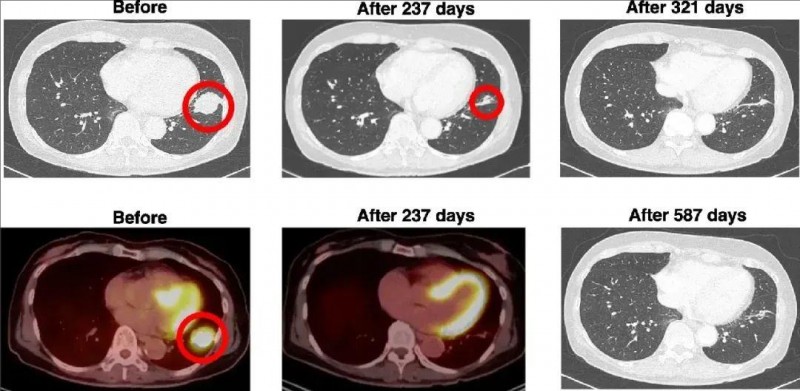
结果显示:WT1/MUC1-DC+厄洛替尼联合治疗后,该患者临床表现有所改善,肿瘤病灶显著缩小。CT+FDG-PET/CT扫描显示,治疗前该患者左下肺叶存在一处35mm×30mm的病灶。治疗第237天后,肿瘤显著缩小了65.7%,肿瘤大小减小至12mm(详见下图)。治疗第321天(此时患者已接种10次DC疫苗),计算机断层扫描未检测到肿瘤。更为惊喜的是,治疗开始后至少587天内(截至统计时止),该患者肿瘤消失的验证持续存在,且无任何复发或转移的迹象。换言之,该患者在DC疫苗联合厄洛替尼治疗后,实现了587天零复发零转移的生存奇迹!
▼本例患者DC疫苗治疗前后CT和PET/CT对比
▲图源“BMC”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:红色圆圈表示肺癌。
DC疫苗助力结肠癌肝转移全切患者,复发次数大幅削减、复发时间显著延迟
尽管采用了标准的新辅助和辅助化疗方案,但可手术切除的结肠癌同步性和异时性肝转移仍有很高的复发风险。因此,迫切需要寻求新的治疗方法,预防癌症的复发及转机。《免疫治疗癌症杂志》报道了一项临床研究(NCT01348256),针装载有自体肿瘤裂解物的DC疫苗展开了测试,旨在探究其在预防或延迟疾病复发方面的潜力。
该研究共入组15例边缘切除干净的患者,这些患者在接受新辅助化疗与手术后,继续进行辅助化疗,将这些患者随机分为两组,即疫苗组(接受DC疫苗治疗)、对照组(不接受疫苗注射)。
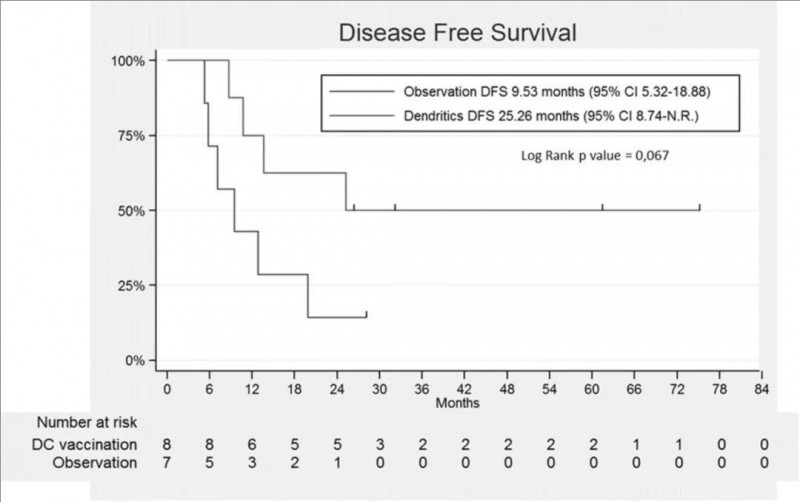
后续对患者的随访(平均随访时间为42.58个月)结果显示:与观察组相比,疫苗组的疾病复发次数显著减少,且复发时间明显延迟。这一结果有力地表明,DC疫苗在抑制肿瘤复发方面展现出了积极的效果。中位无病生存期(DFS)分别为25.26个月(DC疫苗组) vs 9.53个月(对照组)(详见下图)。
▲图源“BMJ”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
04、基于过继细胞转移(ACT)的免疫疗法
基于 ACT 的免疫疗法为治疗转移性癌症提供了一种新方法,这种免疫疗法是针对个体患者量身定制的,能够精准地契合每位患者的独特需求。其作用机制在于,通过在体外诱导肿瘤相关抗原特异性 T 细胞的分化、修饰和扩增,可以产生大量此类细胞。当这些细胞转移到肿瘤患者身上时,可以抑制和消灭肿瘤细胞。它主要包括嵌合抗原受体 T 细胞 (CAR-T) 、T 细胞受体修饰 T 细胞 (TCR-T)、肿瘤浸润淋巴细胞 (TIL)三种类型。
1.CAR-T细胞
CAR-T细胞具有抗原特异性和细胞活化的双重能力,可以选择性地消除肿瘤细胞,主要用于血液肿瘤的治疗。
2.TCR-T细胞
TCR-T细胞可识别细胞膜表面或细胞内来源的肿瘤特异性抗原,与CAR-T细胞类似,均利用自体淋巴细胞来靶向各类癌种,在治疗肝细胞癌、宫颈癌、肺癌、黑色素瘤、滑膜肉瘤等实体瘤方面,展现出了良好的安全性和有效性,是目前最有可能在实体瘤领域取得突破的T细胞免疫疗法。
3.TIL细胞
TIL细胞是一种新型的抗肿瘤效应细胞,这些淋巴细胞可以识别并破坏肿瘤细胞,并动员免疫细胞来帮助对抗肿瘤,相当于深入到敌军内部的免疫细胞敢死队,也是深藏在肿瘤中的宝藏!具有优越的肿瘤病灶浸润能力及低脱靶毒性,可被招募到肿瘤部位直接对抗肿瘤,在治疗黑色素瘤、肝癌、肺癌、卵巢癌、乳腺癌、宫颈癌等多种实体瘤方面,具有独特的优势!
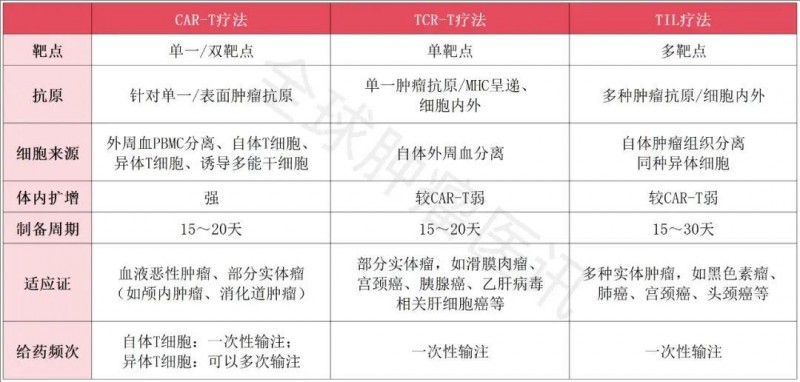
▼CAR-T、TCR-T、TIL疗法对比
晚期宫颈癌患者TIL细胞治疗12周,肿瘤显著缩小33%
《国际妇女健康杂志》近期刊登了我国一位罹患晚期宫颈癌的患者,经TIL细胞治疗后,肿瘤显著缩小33%的惊艳案例!
这是一位68岁的IV期宫颈鳞状细胞癌患者,既往接受过10个周期的化疗(包括卡铂、贝伐单抗、紫杉醇等),她在每个化疗周期后,都出现了严重的骨髓抑制,并伴有白细胞及血小板减少,此时她已无法耐受化疗了。在这种无药可治、无计可施的状态下,她入组接受了淋巴细胞清除+自体TIL细胞静脉回输+IL-2治疗。
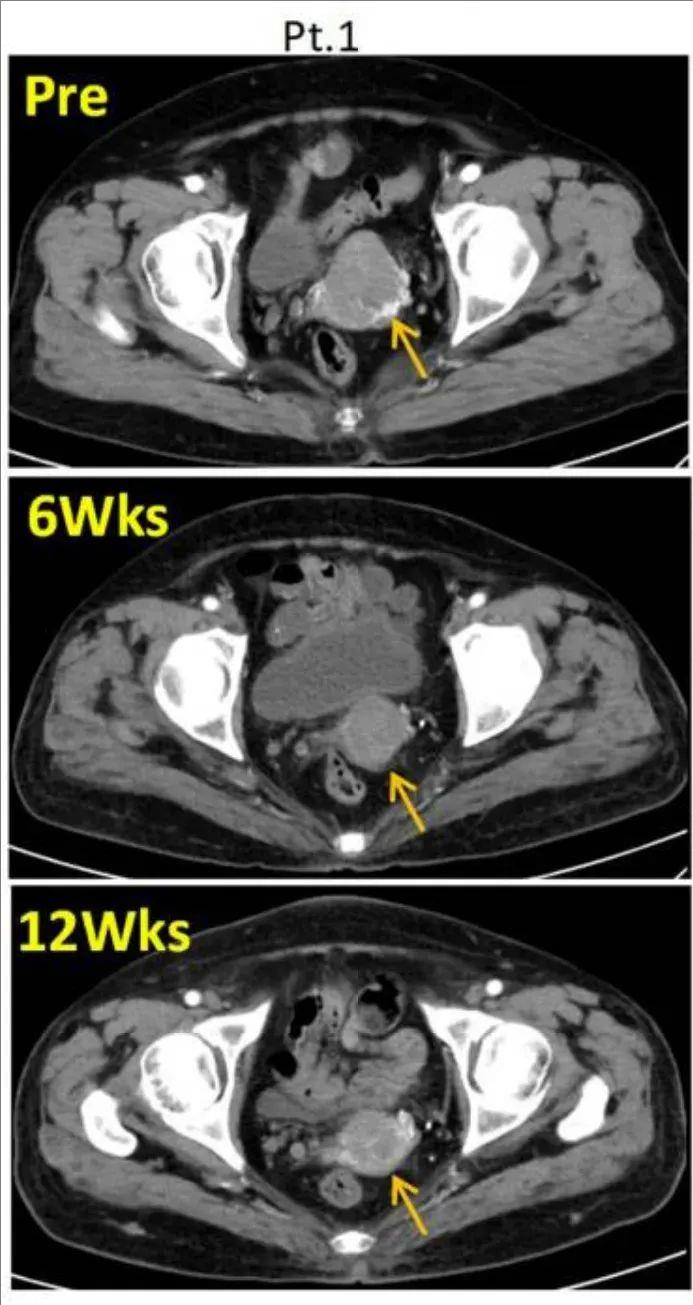
结果显示:该患者在治疗后6周,就表现出客观临床反应,并持续至TIL输注后12周,且阴道分泌物消失。此外,增强盆腔CT扫描显示,肿瘤迅速缩小,靶病变从治疗前的4.9cm,显著缩小至3.3cm(TIL细胞治疗后6周)、3.0cm(TIL细胞治疗后12周)(详见下图)。这也再次用数据验证了TIL单一疗法对患有晚期转移性宫颈癌患者(即使患有严重的骨髓抑制),是一种有前途的治疗策略,可诱导持久和长期的系统性免疫反应。
▲图源“Int J Womens Health”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
05、靶向治疗
虽然细胞毒性化疗仍然是转移性癌症的主要治疗方式,并且仍然是几种癌症亚型的唯一选择,但针对特定肿瘤蛋白的药物(简称为“靶向疗法”)的出现为许多转移性肿瘤提供了新的治疗途径。
06、免疫检查点抑制剂(ICI)
免疫检查点是维持免疫反应幅度和持续时间所必需的调节途径,肿瘤利用这些途径逃避免疫攻击。针对适应性免疫检查点的癌症免疫疗法的出现提高了各种转移性和难治性癌症患者的预后。同时,先天免疫检查点通过吞噬作用阻碍恶性细胞的识别和消除并抑制先天免疫感应,在肿瘤诱导的免疫逃避中发挥关键作用,使其成为癌症免疫治疗的潜在靶点。
但现阶段仅有一小部分癌症患者(包括转移性黑色素瘤、肺癌、膀胱癌、肾癌、错配修复系统异常的癌症患者)可从免疫检查点抑制剂(ICI)中受益。
07、抗体-药物偶联物(ADC)
与传统细胞毒性药物相比,抗体药物偶联物(ADC)致力于在增强治疗有效载荷疗效的同时,最大程度降低其对全身的毒性。ADC 进入细胞后,会在溶酶体中被分解处理,最终释放出有效载荷。随后,该有效载荷通过破坏微管结构或损伤 DNA 等方式发挥细胞毒性作用,进而导致癌细胞死亡。
ADC 凭借靶向递送机制,显著提升了药物精准抵达肿瘤细胞的比例。这一特性不仅可能降低实现治疗效果所需的有效剂量,还能提高患者可耐受的最大剂量,在提升治疗效果的同时,减少药物对正常组织的损害。
小编寄语
一般而言,癌症一旦发生转移,往往提示病情已进展到中晚期,此时不仅治疗难度剧增、治疗效果也可能不尽如人意。即便进行了放化疗,同样也要警惕“二次转移”。但这并不是意味着癌症复发转移一定“无药可治”。尤其是,近年来诸多抗癌新技术的相继出现,为癌症患者带来了新的曙光。
无论是早期亦或晚期患者,首先应积极配合医生治疗、术后辅助免疫细胞(如CAR-T、TCR-T、TIL细胞、NK细胞疗法)、癌症疫苗(如DC细胞疫苗)、饮食调理等方式,尽可能降低术后复发或转移风险。一旦不幸出现复发或转移,也应做到早发现、早期规范治疗、及时获取国内外最新抗癌资讯等,以获得更大的生存收益!抗癌的过程无论多么艰苦,只要不放弃希望,未来的办法总会比问题多!
如果您对目前的治疗方案不满意,或想寻求树突状细胞疫苗、NK细胞、TIL细胞等国内外更多抗癌新技术的帮助,可将近期病理报告、治疗经历、出院小结等资料,提交至全球肿瘤医生网医学部,进行初步评估。
参考资料
[1]Shi X,et al.Mechanism insights and therapeutic intervention of tumor linkstasis: latest developments and perspectives[J]. Signal transduction and targeted therapy, 2024, 9(1): 192.
https://www.nature.com/articles/s41392-024-01885-2
[2]Gautier Follain,et al.Fluids and their mechanics in tumour transit: shaping linkstasis. Nature Reviews Cancer. 2019
https://www.nature.com/articles/s41568-019-0221-x
[3]Li F,et al.Autologous Tumor-Infiltrating Lymphocyte Mono-Therapy Can Rapidly Shrank Tumor in Asian Patient with Stage III/IV Cervical Cancer: Two Cases Report. Int J Womens Health. 2024 Jan 9;16:31-39.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10787568/
[4]Bagus BI.Autologous natural killer cells as a promising immunotherapy for locally advanced newline adenocarcinoma: Three years follow-up of resectable case. Cancer Rep (Hoboken). 2023 Sep;6(9):e1866.
https://pubmed.ncbi.nlm.nih.gov/37439389/
[5]Rodriguez J,et al.A randomized phase II clinical trial of dendritic cell vaccination following complete resection of newline cancer liver linkstasis. J Immunother Cancer. 2018 Sep 29;6(1):96.
https://pmc.ncbi.nlm.nih.gov/articles/PMC6164167/
[6]Kosumi T,et al.Dendritic cell vaccination in combination with erlotinib in a patient with inoperable lung adenocarcinoma: a case report[J]. Journal of Medical Case Reports, 2024, 18(1): 88.
https://jmedicalcasereports.biomedcentral.com/articles/10.1186/s13256-024-04363-z