树突状细胞(DC)疗法治疗肺癌、脑瘤、子宫内膜癌、血癌等,有患者587天零复发零转移
树突状细胞(dendriticcell,DC)是一类多功能抗原提呈细胞,其主要任务是引导抗癌免疫力摧毁癌细胞。《医学病例报告杂志》近期刊载了这样一则令人振奋的病例:一位处于无法实施手术治疗的晚期肺癌患者,在接受树突状细胞疫苗与厄洛替尼联合治疗方案的干预后,收获了超乎预期的出色疗效。在长达至少587天(约1.6年)的随访观察期内,患者体内的肿瘤未出现任何复发或转移的迹象。这一突破性的治疗成果宛如一盏明灯,为晚期癌症患者带来了新的希望与方向!
▲截图源自“Journal of Medical Case Reports”
树突状细胞疫苗联合厄洛替尼,助晚期肺腺癌实现587天零复发零转移奇迹
在晚期非小细胞肺癌(NSCLC)患者群体里,肿瘤微环境(TME)呈现出免疫抑制的特性,这种特性极大地制约了患者抗肿瘤免疫反应的有效激发。对于那些无法实施切除手术的晚期肺癌患者而言,当下所采用的治疗手段难以达到令人满意的效果,患者的预后情况依然不容乐观。鉴于此,迫切需要增强免疫系统的新型治疗策略。而医学病例报告杂志》报道的这个振奋人心的案例,为此类肺癌患者带来了新的曙光!
本例患者是一位63岁的EGFR(表皮生长因子受体)突变的晚期(Ⅲb期:T2aN3M0)肺腺癌患者,无ALK(间变性淋巴瘤激酶)表达,PD-L1(程序性死亡配体1)表达不足1%。东部肿瘤协作组体能状态(PS)为0,器官功能正常,且未接受过化疗。由于该患者的情况无法接受手术切除,遂入组先接受了1个月的厄洛替尼(这是一种小分子EGFR酪氨酸激酶抑制剂)治疗,之后接受厄洛替尼+用MHC II类限制性WT1肽和粘蛋白1(MUC1)肽疫苗冲击的树突状细胞(WT1/MUC1-DC)联合治疗,以诱导WT1和MUC1抗肿瘤CTL。
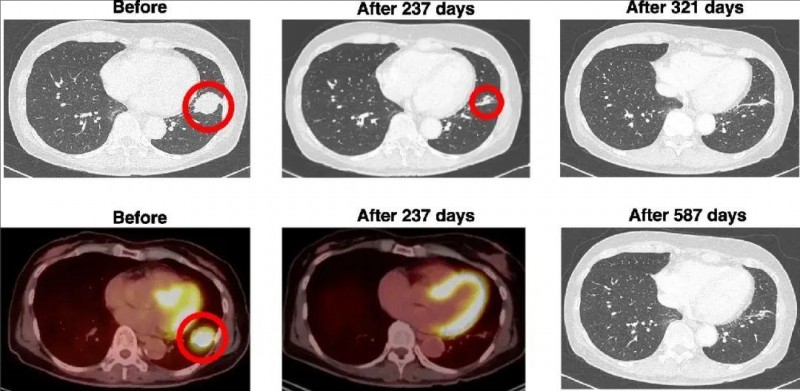
结果显示:治疗前,计算机断层扫描(CT)+FDG-PET/CT[氟脱氧葡萄糖(FDG)-正电子发射断层扫描/CT(PET/CT)]扫描显示,该患者左下肺叶存在一处35mm×30mm的病灶。在WT1/MUC1-DC+厄洛替尼联合治疗237天后,肿瘤显著缩小了65.7%,肿瘤大小减小至12mm(详见下图)。经过321天的联合治疗后(此时该患者已接种了10次DC疫苗),临床表现有所改善,并且根据计算机断层扫描未检测到肿瘤。更为惊喜的是,治疗开始后至少587天内(截至统计时止),肿瘤消失的验证持续存在,没有任何复发或转移的迹象。
▼该患者DC疫苗治疗前后CT和PET/CT对比
▲图源“BMC”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:红色圆圈表示肺癌。
树突状细胞疫苗2024重大进展,暴击脑瘤、子宫内膜癌、血癌等
树突状细胞(dendriticcell,DC)是免疫系统中最强大的抗原呈递细胞,是先天免疫系统和适应性免疫系统之间的桥梁,其主要任务是引导抗癌免疫力摧毁癌细胞。
在DC疫苗接种中,自体DC在体外负载相关肿瘤抗原并注射到患者体内,旨在诱导特定的T细胞和B细胞反应。DC细胞通过识别癌症抗原(恶性细胞表面的独特分子),并将其展示给免疫系统的杀伤细胞T淋巴细胞,一旦指定了攻击目标,T淋巴细胞就会主动摧毁肿瘤,并将其抗原成分信息传递给下一代免疫细胞。
在过去近二十载的时间里,DC细胞作为抗肿瘤疫苗的重要组成部分,针对多种类型的肿瘤开展了广泛而深入的临床试验,涵盖了乳腺癌、多发性骨髓瘤、前列腺癌、肾细胞癌、恶性黑色素瘤、结直肠癌以及非小细胞肺癌等诸多领域。步入2024年,全球范围内针对DC疫苗的研究持续深入,众多临床试验不断取得关键数据和重大突破,进一步彰显了其在癌症治疗体系中的关键价值和广阔的应用潜力!
与标准治疗相比,DC疫苗显著提升了胶质母细胞瘤的生存率
胶质母细胞瘤 (GBM)属于一种常见的中枢神经系统 (CNS) 肿瘤,尽管采取了积极的标准治疗,但其平均生存期仍为 14-18 个月。
近期,知名免疫肿瘤学公司——Diakonos oncology Corp,在2024年美国癌症研究协会年会上,公布了“DOC1021(一种创新的树突状细胞疫苗)治疗胶质母细胞瘤的1期临床结果”,结果显示多形性胶质母细胞瘤 (GBM) 患者的生存期显著延长,远超接受标准治疗 (SOC) 的患者预期的 12.7 个月中位总生存期 (mOS)。本次研究共招募16例新诊断的 GBM 患者,平均随访时间为 12.9 个月。
结果显示:16 名新诊断的 GBM 患者中,有 12 名(75%)在平均 12.9 个月的随访中仍存活,且未发生可归因的严重不良事件。目前,未甲基化 GBM 患者的 12 个月总生存率为 88%,而接受标准治疗的未甲基化 GBM 患者 12 个月历史生存率为 53%。
▲图源“AACR”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
值得一提的是,其中1例患者(患者GBM-MDAC001),在治疗后复查MRI发现,肿瘤明显缩小(详见下图)。
▼患者GBM-MDAC001(剂量队列1)治疗前后MRI对比
▲图源“AACR”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
基于上述惊艳结果,目前DOC1021已获得FDA的快速通道和孤儿药资格认定。Diakonos首席执行官 Mike Wicks 表示:“DOC1021是首创的树突状细胞疫苗,代表了一种全新的策略,可以对患者的癌症进行完全免疫反应!同时,这些令人振奋的结果增强了我们的信心,让我们相信树突状细胞疫苗能够显著改善最致命癌症患者的生活”!
树突状细胞疫苗联合卡铂/紫杉醇,子宫内膜癌中位总生存期近2年
近期一项单臂 I/II 期DECENDO研究,共纳入7位中位年龄为 65 岁的转移性子宫内膜癌 (mEC) 患者,所有患者均表达 Survivin 和 Mucin-1,所有患者均已接受子宫切除术。两名患者接受了卡铂和紫杉醇辅助治疗作为辅助治疗,一名患者接受转移性疾病治疗,三名患者接受过放射治疗。
▲截图源自“frontiers”
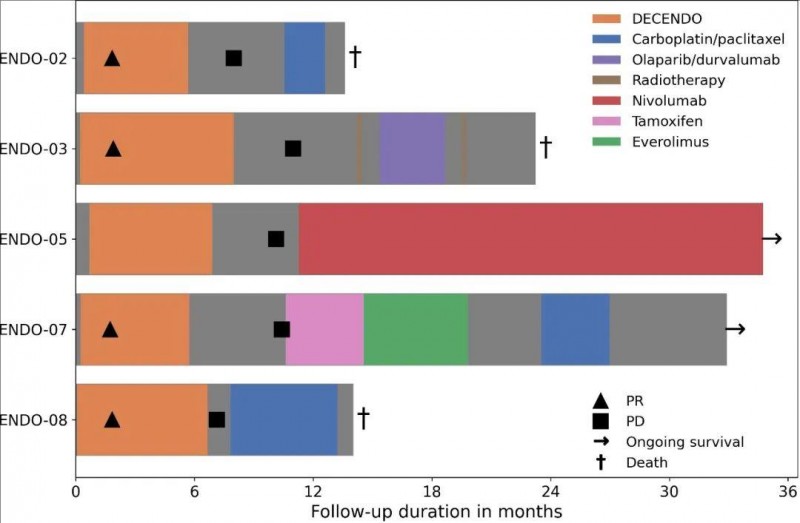
结果显示:5例接受 nDC 治疗的患者其临床反应和长期随访数据可用,其中4例获得部分缓解(PR),1例达到病情稳定(SD),这些最佳反应都是在最初两个化疗周期后达到的。此外,中位无进展生存期 (PFS) 为 10 个月(范围:7 – 11 个月)。中位总生存期 (OS) 达23 个月(范围:14 – 35 个月后存活)。截至数据截止日(2022 年 1 月 12 日),有2例患者(ENDO-05、ENDO-07)仍存活。其中,ENDO-05号患者适合接受免疫检查点抑制剂(ICI) 治疗,因为她的肿瘤被确定为微卫星不稳定,并且她对 nivolumab 反应良好且持续 PR;ENDO-07号患者依次接受他莫昔芬、依维莫司和卡铂/紫杉醇化疗。
▲图源“frontiers”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
综上,DC疫苗可与卡铂/紫杉醇联合,用于转移性子宫内膜癌患者,并在少数患者中诱发抗原特异性反应。纵向免疫表型分析提示该联合疗法具有协同作用。
无维持治疗介入时,DC/AML融合疫苗助急性髓系白血病,2年总生存率攀升至73%
全球血液学知名期刊《Blood》近期报道了一项“应用个性化癌症疫苗,治疗急性髓系白血病的II期临床试验(NCT03059485)”的惊艳疗效!即使在没有维持治疗的情况下,接受DC/AML融合疫苗接种,依然可使老年患者的2年总生存率达到73%,无进展生存率达到36%。
本次共入组41例年龄>55岁的急性髓系白血病(AML)患者,将其按2∶1的比例随机分为两组,即疫苗组[A组,27例,接受DC/AML(患者来源的AML细胞与自体树突状细胞)融合细胞疫苗接种]、标准治疗组(C组,14例)。结果显示如下:
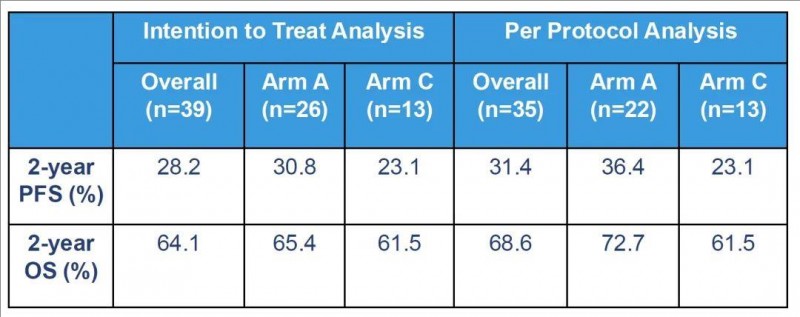
1、无进展生存(PFS)率:疫苗组(A组)患者的2年PFS率为31%,在接种疫苗的患者(N=22)中为36%,而C组(N=13)中为23%。
▲图源“Blood”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
2、总生存(OS)率:2年OS率分别为73%(A组) vs 61%(C组)。
▲数据源自“Blood”
我国多款在研DC疫苗蓄势待发,国内多个中心启动招募
除了上面提到的几款在2024年取得突破性进展的DC疫苗外,我国也有多款在研的DC疫苗正在蓄势待发,并在国内多家癌症中心启动临床,众多晚期患者已成功入组接受治疗!
1、LK101:立康生命
LK101注射液是立康生命自主研发的一款自体树突状细胞(DC)疫苗,可编码数十个患者自体肿瘤的个性化新抗原靶点,采用mRNA-DC疫苗形式,将患者个性化肿瘤新抗原mRNA体外转导入DC细胞,巧妙地融合了 mRNA 疫苗与 DC 疫苗的双重优势。这种设计使得在治疗过程中,无需在体内注射免疫佐剂以及 mRNA 包裹材料,既能够高效地激发机体产生高特异性的抗肿瘤免疫活性,又极大地提升了药物的安全性以及患者对药物的耐受性,为癌症治疗带来了新的希望与突破。
2023年9月,LK101注射液正式启动了Ⅰ期临床试验(NCT06054932),值得一提的是,它是我国首个获得中国国家药品监督管理局(NMPA)批准并进入临床阶段的个性化肿瘤新生抗原疫苗。
2、MASCT-I:恒瑞源正
MASCT-I是由恒瑞源正自主研发的一款1类细胞治疗产品,其活性成份包括负载多种肿瘤相关抗原的成熟自体树突状细胞(DC细胞)、DC细胞活化扩增的自体效应T淋巴细胞(T细胞)。
在2024年美国临床肿瘤学会(ASCO)年会上,公布了“MASCT-I治疗转移性尿路上皮癌的1期临床研究(NCT03034304)数据”,其2期临床研究已获得国家药品监督管理局药品审评中心(CDE)批准!
3、KSD-101:恒赛生物
KSD-101是恒赛生物自主研发的一款负载EB病毒相关类肿瘤复合抗原的人单核细胞来源自体DC疫苗,2024年3月,该疫苗的新药临床试验(IND)申请获得美国食品药品监督管理局(FDA)批准,KSD-101也成为了我国首个获得美国FDA IND批件的自研DC疫苗产品!
4、ZSNeo-DC1.1:中生康元
ZSNeo-DC1.1注射液是中生康元自研的一款新型个性化树突状细胞疫苗,其临床试验默示许可已获得国家药品监督管理局药品审评中心(CDE)批准,用于泛癌种恶性实体肿瘤的治疗。值得一提的是,它是我国首个进入注册临床研究阶段的负载多个肿瘤新生抗原肽的治疗性肿瘤DC细胞产品!
5、靶向Survivin DC细胞注射液:启辰生生物
靶向Survivin DC细胞注射液是启辰生生物研发的一款针对原发性脑胶质母细胞瘤的抗原mRNA负载的树突状细胞(DC)产品,同时也是世界首款靶向Survivin的针对脑胶质母细胞瘤的mRNA-DC肿瘤疫苗!其治疗目的在于帮助患者清除术后残留的癌细胞、预防肿瘤的复发及转移、延长患者的生存期。前期临床探索性研究数据显示,1例患者在治疗后,总生存期已超5年!
6、CUD002:康德赛医疗
CUD002是康德赛医疗自主研发的一款针对卵巢癌的个体化mRNA编辑的DC肿瘤疫苗,根据患者独特的突变信息定制设计并制造而成,值得一提的是,它是我国首款用于卵巢癌治疗的新生抗原的mRNA编辑DC肿瘤疫苗!其临床试验默示许可已于2023年9月,获得国家药品监督管理局药品审评中心(CDE)批准,拟用于难治性/耐药复发性卵巢癌的治疗。
7、CAR-DC癌症疫苗:翊博生物
CAR-DC癌症疫苗是一款利用工程化树突状细胞扩增技术(CelArts-DC),对外周血中的原代DC亚群进行选择性扩增,从而成功攻克了以往在 DC 细胞应用过程中所面临的DC细胞来源少、对免疫系统要求较高等诸多应用难点问题。
小编寄语
癌症作为一种高度突变的复杂疾病,很难仅靠单一治疗手段,达到理想的治疗效果。目前比较理想的治疗手段是在权威医院(手术、放化疗等)传统治疗的基础上,结合患者病情、个体情况,突变靶点、经济状况等,辅助靶向药、免疫细胞治疗(如CAR-T、TCR-T、TIL细胞疗法、DC疫苗)、质子治疗、电场疗法等新型治疗手段,以达到巩固传统治疗效果、降低肿瘤复发风险、提高患者生存质量、延长生存期等目的。
其中,树突状细胞(DC)疫苗就是利用患者独特的免疫特性,来治疗癌症的方法,通过激活初始T细胞的抗原提呈细胞,在机体免疫中发挥着重要的作用!对目前治疗方案不满意,或想寻求树突状细胞疫苗等抗癌新技术帮助的患者,可将近期病理报告、影像学检查资料、治疗经历等,提交至全球肿瘤医生网医学部,进行初步评估。
参考资料
[1]Kosumi T,et al.Dendritic cell vaccination in combination with erlotinib in a patient with inoperable lung adenocarcinoma: a case report[J]. Journal of Medical Case Reports, 2024, 18(1): 88.
https://jmedicalcasereports.biomedcentral.com/articles/10.1186/s13256-024-04363-z
[2]Georges J F,et al.Abstract CT093: Vaccine immunotherapy by homologous antigenic loading as adjuvant therapy for glioblastoma: ongoing phase I analysis[J]. Cancer Research, 2024, 84(7_Supplement): CT093-CT093.
https://aacrjournals.org/cancerres/article/84/7_Supplement/CT093/742698/Abstract-CT093-Vaccine-immunotherapy-by-homologous
[3]Koeneman B J,et al.Dendritic cell vaccination combined with carboplatin/paclitaxel for linkstatic endometrial cancer patients: results of a phase I/II trial[J]. Frontiers in Immunology, 2024, 15: 1368103.
https://www.frontiersin.org/journals/immunology/articles/10.3389/fimmu.2024.1368103/full
[4]Pophali P,et al.Randomized Phase II Trial of Dendritic Cell/AML Fusion Cell Vaccination Compared to Standard of Care Therapy in AML CR1[J]. Blood, 2024, 144: 4256.
https://ashpublications.org/blood/article/144/Supplement%201/4256/533532/Randomized-Phase-II-Trial-of-Dendritic-Cell-AML