2024年11月27日药监局批准PD-L1单抗贝莫苏拜单抗(安得卫、TQB2450、Benmelstobart)用于复发或转移性子宫内膜癌
2024年11月27日注定是抗癌圈中值得载入史册的一天,除了迎来国产首个TROP2ADC药物——芦康沙妥珠单抗外,另一款抗癌新药——贝莫苏拜单抗的新适应证也在今天获得了中国国家药品监督管理局(NMPA)批准,与盐酸安罗替尼胶囊联合,用于非DNA错配修复缺陷(非dMMR)或非微卫星高度不稳定(非MSI-H)的复发性或转移性子宫内膜癌的治疗,且既往接受过一、二线化疗方案治疗失败或不能耐受治疗者。
▲截图源自“正大天晴官网”
贝莫苏拜单抗两大适应证获批,点亮小细胞肺癌及子宫内膜癌的"生命之光"
贝莫苏拜单抗(TQB2450,Benmelstobart,安得卫®)是正大天晴药业集团自主研发的一款全新序列的创新人源化 PD-L1 单克隆抗体,属1类创新药范围。
本次获批的子宫内膜癌是贝莫苏拜单抗获批的第2个适应证;早在2024 年 5 月该药的首个适应证在中国获批,与安罗替尼及化疗药(依托泊苷、卡铂)联合,作为广泛期小细胞肺癌(ES-SCLC)的一线治疗。
除此之外,今年8月贝莫苏拜单抗的另一适应证的上市申请,已获得中国国家药品监督管理局药品审评中心(CDE)受理,用于晚期不可切除或转移性肾细胞癌(RCC)的一线治疗。
贝莫苏拜单抗联合安罗替尼,复发性或转移性子宫内膜癌,疾病控制率接近80%
贝莫苏拜单抗本次获批,主要基于2024国际妇科肿瘤学会(IGCS)年会上,公布的“贝莫苏拜单抗联合安罗替尼,治疗复发性或转移性子宫内膜癌Ⅱ期ETER200临床研究(NCTO4574284)的惊艳数据”。
本次研究共有85例晚期、复发或转移性子宫内膜癌(EC)患者(其中80.0%为子宫内膜样癌),被纳入队列1的第二阶段的研究中,这些患者的中位年龄为60.0岁,既往接受过1或2线基于铂的化疗失败。结果显示如下:
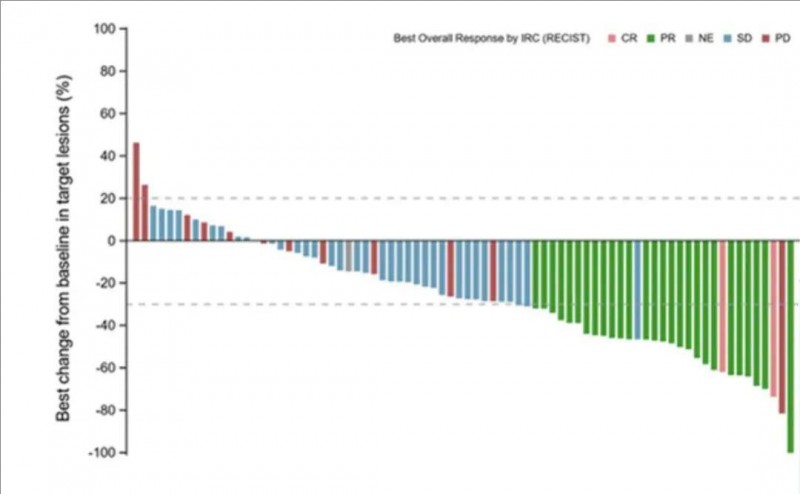
1、客观缓解率(ORR)及疾病控制率(DCR):通过独立影像学评估委员会(IRC)确认的客观缓解率(ORR)达到34.12%。其中2例患者幸运地获得完全缓解(CR),27例患者达到部分缓解(PR),另有37例患者达到病情稳定(SD),疾病控制率(DCR)高达77.7%。
▲图源“IGCS”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
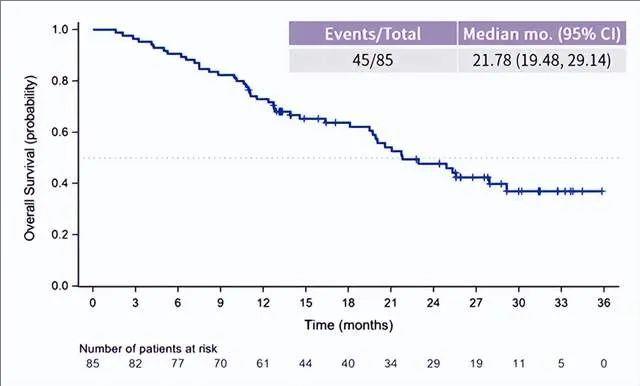
2、中位总生存期(mOS):mOS为21.78个月(95%Cl:19.48,29.14)。
▲图源“IGCS”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
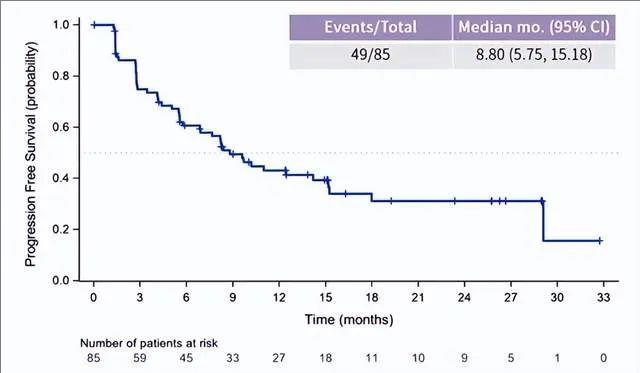
3、中位无进展生存期(mPFS):mPFS为8.80个月(95%Cl:5.75,15.18)。
▲图源“IGCS”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
综上,贝莫苏拜单抗联合安罗替尼,在治疗复发性或转移性子宫内膜癌方面显示出良好的抗肿瘤活性,且安全性可控。
贝莫苏拜单抗3期临床惊艳,小细胞肺癌1年总生存率超64%
小细胞肺癌(SCLC)是一类恶性程度高、进展迅速的癌症,患者初诊时多为广泛期SCLC(ES-SCLC),标准化疗易导致短期内复发,预后不佳。
一项“贝莫苏拜单抗联合安罗替尼,治疗小细胞肺癌的3期ETER701临床研究(NCT04234607)”,共入组738例中位年龄为62岁的广泛期小细胞肺癌患者[即意向治疗(ITT)人群],将其随机分为三组,即贝莫苏拜单抗+安罗替尼+依托泊苷/卡铂组(EC;n =246)、安慰剂+安罗替尼+EC组(n =245)、双安慰剂+EC组(单独EC;n=247)。结果显示如下:
1、中位总生存期(OS):与单独EC相比,贝莫苏拜单抗+安罗替尼+依托泊苷/卡铂(EC)组的中位总生存期显著延长,而安罗替尼+EC组的OS改善无统计学意义,中位OS分别为19.3个月(贝莫苏拜单抗+安罗替尼+EC组) vs11.9个月(单独EC组) vs 13.3个月(安罗替尼+EC组)(详见下图)。其中,12个月总生存(OS)率分别为64.1%(贝莫苏拜单抗+安罗替尼+EC组) vs 53.6%(安罗替尼+EC组) vs 49.0%(单独EC组)。18个月总生存(OS)率分别为50.7%(贝莫苏拜单抗+安罗替尼+EC组) vs 34.7%(安罗替尼+EC组) vs 26.1%(单独EC组)。
▲图源“Nature Medicine”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
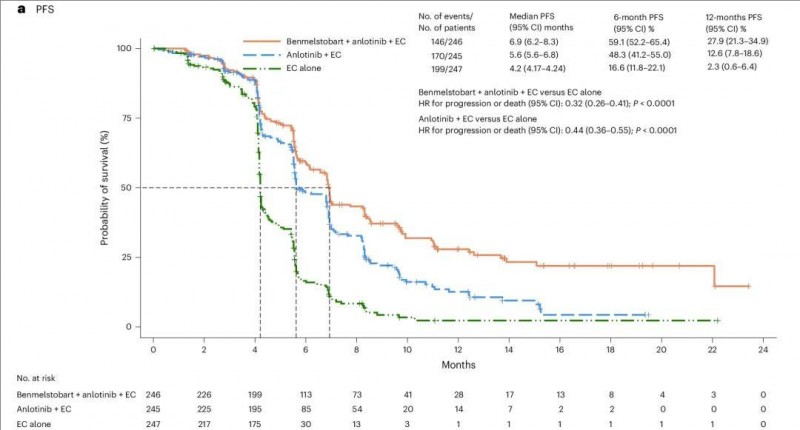
2、中位无进展生存期(PFS):与单独使用EC组相比,贝莫苏拜单抗+安罗替尼+依托泊苷/卡铂(EC)组的中位无进展生存期(PFS)显著延长,分别为6.9个月(贝莫苏拜单抗+安罗替尼+EC组)vs 4.2个月(单独EC组)vs 5.6个月(安罗替尼+EC组)(详见下图)。此外,6个月PFS率分别为59.1%(贝莫苏拜单抗+安罗替尼+EC组) vs 48.3%(安罗替尼+EC组) vs 16.6%(单独EC组)。12个月PFS率分别为27.9%(贝莫苏拜单抗+安罗替尼+EC组) vs 12.6%(安罗替尼+EC组) vs 2.3%(单独EC组)。
▲图源“Nature Medicine”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
喜讯!贝莫苏拜单抗招募进行中,国内多家癌症中心启动临床招募
肺癌招募
新药简介
①药品名称:贝莫苏拜单抗(TQB2450注射液)联合AL2846胶囊。
②研发公司:正大天晴。
适应证
适用于局部晚期或转移性或复发性非小细胞肺癌(NSCLC)患者,既往接受过含铂化疗和免疫检查点抑制剂治疗失败,且治疗线数≤2,无已知EGFR突变、ALK融合、ROS1融合等有意义的驱动基因突变,中央型且有空腔的鳞癌(原发于主支气管或肺门周围)。
招募信息(部分)
1)年龄:18-75周岁(签署知情同意书时);ECOGPS评分:0-1分;基线体重指数BMI≥17;预计生存期超过3个月。
2)根据国际肺癌研究协会和美国癌症分类联合委员会第8版肺癌TNM分期,具有组织学或细胞学证实的不能手术治疗且不能接受根治性同步放化疗的局部晚期(ⅢB/ⅢC期)、转移性或复发性(IV期)NSCLC的患者。
3)针对不可根治的局部晚期或转移性或复发性NSCLC接受过含铂化疗和免疫检查点抑制剂治疗失败(定义为RECIST1.1标准的影像学进展);但不包括上述治疗作为多模式治疗的一部分用于根治性治疗(包括新辅助(诱导)/同步/维持(辅助)治疗),除非根治性多模式治疗期间或完成后6个月内疾病复发或进展。
4)根据RECIST1.1标准证实具有至少一个可测量病灶。
5)既往接受的针对不可切除/不能进行根治性放化疗的局晚期或转移/复发疾病的系统治疗线数:1~2。
子宫内膜癌招募
新药简介
①药品名称:贝莫苏拜单抗(TQB2450注射液)联合安罗替尼。
②研发公司:正大天晴。
适应证
适用于复发性或转移性晚期子宫内膜癌(二线无靶点要求)患者。
招募信息(部分)
1)年龄:≥18周岁(签署知情同意书时);ECOGPS评分:0-1分;预计生存期超过3个月。
2)经组织病理学证实的复发性或转移性晚期子宫内膜癌;注:既往接受过1-2线全身标准化疗方案治疗失败或不能耐受。不耐受”定义为在治疗中出现≥Ⅳ级的血液学毒性或≥Ⅲ级的非血液学毒性。允许前期进行新辅助或辅助化疗。如果新辅助/辅助治疗期间或治疗结束后12个月以内出现疾病进展/复发,则认为新辅助/辅助治疗是针对进展性疾病的一线全身化疗失败。
3)根据RECIST1.1标准证实具有至少一个可测量病灶。
4)可以提供肿瘤组织样本用于中心实验室检测MSI/MMR状态;(队列3若有非MSI/MMR报告无需中心试验室复核)。
申请流程
想申请贝莫苏拜单抗(TQB2450注射液)临床试验的患者,需将近期基因检测报告、病理报告等资料汇总后,提交至医学部,进行初步评估。我们的专家将为您全面分析解读检测报告,并匹配适合患者入组的临床试验项目。注:全球肿瘤医生网作为国内权威的肿瘤患者服务平台,我们承诺对所有患者的个人信息保密,并承诺在整个过程中,遵循国家临床研究的相关法律法规。
小编寄语
贝莫苏拜单抗的获批上市,为广泛期小细胞肺癌和子宫内膜癌患者带来了新的希望与选择!小编也希望早日迎来该药在肾细胞癌治疗领域的好消息。除了贝莫苏拜单抗外,还有众多新药、新技术纷纷在研发的道路上,将帮助更多的饱受病痛折磨的癌症患者,摆脱“无药可用”的困境!对目前治疗方案不满意的癌友,可将治疗经历、近期病理报告等,提交至医学部,进行初步评估。此外,“方舟援助计划”也可为患者提供上市新药和未上市新药免费治疗的机会。
参考资料
[1]Cheng Y,et al.Benmelstobart, anlotinib and chemotherapy in extensive-stage small-cell lung cancer: a randomized phase 3 trial[J]. Nature Medicine, 2024: 1-10.
https://www.nature.com/articles/s41591-024-03132-1
[2]https://www.cttq.com/
[3]https://igcsmeeting.com/wp-content/uploads/sites/79/2024/10/IGCS-2024-Late-Breaking-Abstracts.pdf