CAR-T细胞疗法成功案例分析
CAR-GPC3 T细胞联合局部治疗,晚期肝细胞癌患者生存超8年
肝癌患者治疗选择有限,整体预后不佳,即使进行手术切除,术后中位总生存期仅为17.8个月,而世界知名期刊《癌症通讯》杂志,报道的一个“晚期肝细胞癌(HCC)患者,经创新型CAR-GPC3 T细胞疗法后,生存超8年”的经典案例,远超肝细胞癌17.8个月的中位生存期!
这位幸运患者是一位54岁男性,确诊为Ib期肝细胞癌(HCC),既往接受过肿瘤切除手术、经导管动脉化疗栓塞术(TACE)、肝癌微波消融治疗(MWA)等治疗,但病情仍迅速进展,MRI显示肝脏多灶性病变、腹膜后淋巴结转移(LM)。入组接受CAR-GPC3 T细胞治疗后,结果显示:
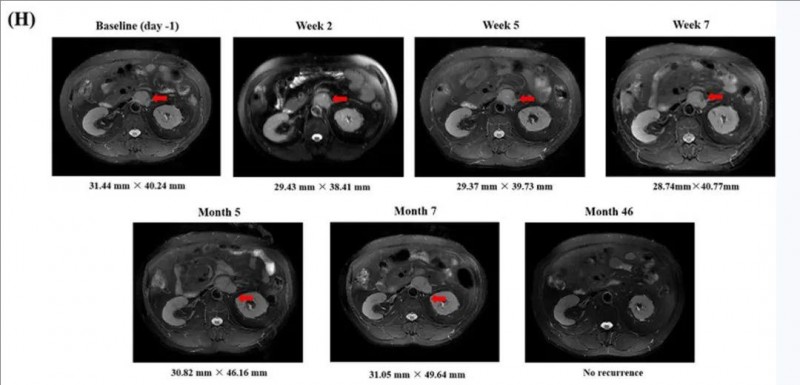
1、转移灶明显缩小:CAR-T细胞治疗后2周,腹膜后淋巴结转移灶(LM)开始缩小,病变短轴直径缩小了5.2%,长轴直径缩小了4.5%。最后一次输注CAR-GPC3 T细胞后,靶病变短轴进一步减小,在第7次输注后第7天减小了7.4%(详见下图)。
▼CAR-GPC3 T细胞输注前后,腹膜后淋巴转移的MRI成像(红色箭头)
▲图源“WILEY online Library”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
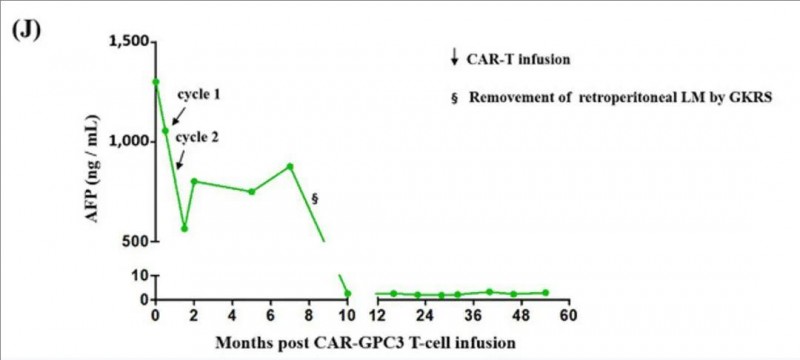
2、肿瘤标志物水平:该患者甲胎蛋白(AFP)水平降低了56.6%,从1,301ng/mL,骤降至565ng/mL(详见下图)。之后在接受伽玛刀放射外科治疗(GKRS)后,AFP水平逐渐下降至正常范围,此后患者一直处于无癌状态。
▲图源“WILEY online Library”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
3、长生存奇迹:患者除了2016年7月接受伽玛刀放射外科治疗(GKRS)治疗外,此后在没有任何进一步抗癌治疗的情况下,保持无病状态超过5年,总生存期超过8年(详见下图)!
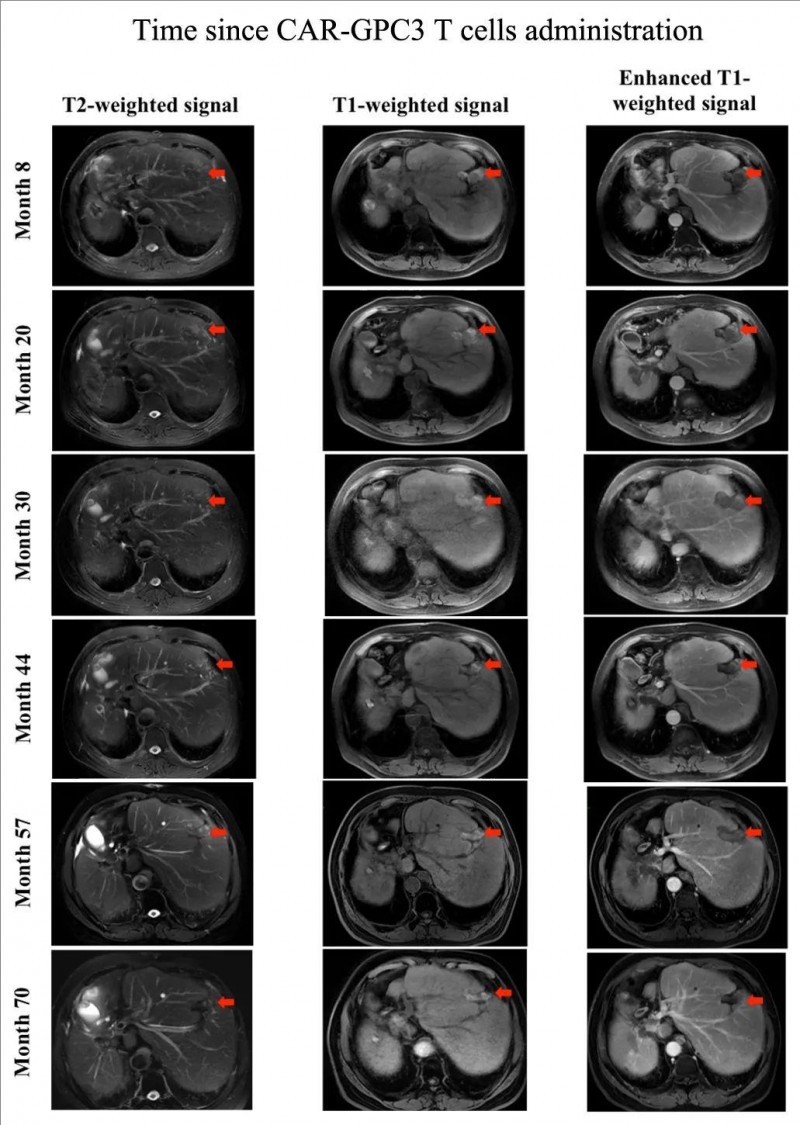
▼CAR-GPC3 T细胞治疗后肝脏MRI图像
▲图源“WILEY online Library”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:红色箭头表示治疗后的坏死肿瘤。
CLDN18.2 CAR-T:助转移性胃癌患者获得完全缓解
尽管采取化疗为主的传统治疗+免疫疗法或靶向药物可以获得客观的肿瘤反应和生存益处,但绝大多数胃癌患者仍然无法治愈。而且由于深部组织侵袭和腹膜渗透,很多胃癌患者无法通过手术切除,5年总生存率仅为5%~20%,中位生存期不足1年(11个月)。
Claudin18.2(CLDN18.2)是一种高选择性细胞表面分子,在正常胃组织中表达有限,但在原发性胃癌及其转移灶中的表达明显较高。针对胃癌的这一关键靶点,我国研发了一款名为“CT041”的CLDN18.2靶向嵌合抗原受体-T(CAR-T)细胞。
《癌症免疫治疗杂志》报道了CT041治疗转移性胃癌并获得完全缓解的出色案例。这位30岁患者确诊为CLDN18.2阳性转移性、低分化印戒细胞癌,在四线联合全身化疗、多次细胞减灭手术联合腹腔热灌注化疗(HIPEC)后,病情出现进展。
入组接受第一次CT041回输治疗后,两个腹膜靶病变显著减少;腹胀改善且左中腹部包裹性腹水减少。根据 RECIST V.1.1,在治疗第4周时,靶病变消失,患者获得部分缓解(PR),并维持8个月的总体部分缓解。在第二次回输CT041后4周,患者幸运地获得完全缓解(CR),仅出现少量腹水。
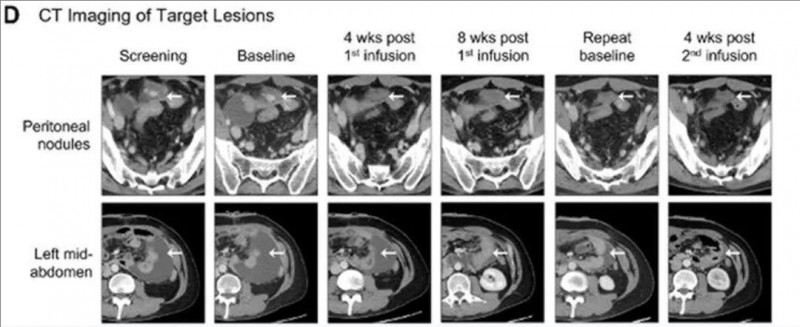
▼该患者增强轴向CT扫描结果
▲图源“J Immunother Cancer”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:
①上图:通过增强轴向CT扫描显示,该患者腹膜结节靶病变完全缓解(箭头,顶部);
②下图:通过增强轴向CT扫描显示,该患者左中腹部包裹性腹水减少(箭头,底部)。
小编寄语
迄今为止,CAR-T细胞疗法已在血液系统恶性肿瘤治疗方面取得了突破性进展。然而,它们在治疗实体瘤方面的成功仍然有限,这可能与实体瘤中T细胞的低浸润性、免疫抑制的肿瘤微环境等因素有关。值得欣慰的是,近年来各国研究人员,在不断研发各种新型策略,以减轻肿瘤抗原异质性、应对免疫抑制,深耕CAR-T在实体瘤领域的应用价值。
我国CAR-T发展也已进入“百家争鸣”的局面,相继有驯鹿医疗、复星凯特、科济生物、传奇生物等多家制药巨头纷纷加入CAR-T的研发大军中,并有幸运患者获得完全缓解!如果您也想寻求CAR-T或国内外其他抗癌新技术(如TIL、TCR-T、NK细胞、益生菌)的帮助,可将出院小结、治疗经历、完整的病理报告等资料,提交至医学部,进行初步评估,或申请国内外抗癌专家会诊。
参考资料
[1]Ganapathy T,et al.CAR γδ T cells for cancer immunotherapy. Is the field more yellow than green? Cancer Immunol Immunother. 2023 Feb;72(2):277-286.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10992831/
[2]Shi Y,et al.Combined local therapy and CAR-GPC3 T-cell therapy in advanced hepatocellular carcinoma: a proof-of-concept treatment strategy. Cancer Commun (Lond). 2023 Sep;43(9):1064-1068.
https://onlinelibrary.wiley.com/doi/10.1002/cac2.12472
[3]Botta GP,et al.linkstatic gastric cancer target lesion complete response with Claudin18.2-CAR T cells. J Immunother Cancer. 2024 Feb 5;12(2):e007927.
https://pubmed.ncbi.nlm.nih.gov/38316518/
[4]https://oncologypro.esmo.org/meeting-resources/esmo-congress-2024/safety-and-efficacy-of-a-novel-car-t-cell-therapy-brg01-targeting-the-epstein-barr-virus-envelope-glycoprotein-in-advanced-linkstatic-nasopharyng
[5]https://www.prnewswire.com/news-releases/biosyngens-first-in-class-car-t-asset-targeting-solid-tumors-has-entered-pivotal-phase-ii-trial-phase-i-trial-data-debut-at-esmo-2024-annual-congress-302251709.html
[6]https://oncologypro.esmo.org/meeting-resources/esmo-gastrointestinal-cancers-congress-2024/enhanced-antitumor-efficacy-and-safety-through-a-novel-car-t-strategy-targeting-msln-and-cldn18.2
[7]https://oncologypro.esmo.org/meeting-resources/esmo-congress-2024/first-in-human-dose-escalation-trial-of-fourth-generation-chimeric-antigen-receptor-car-t-cell-therapy-eu307-in-patients-with-glypican-3-gpc3
[8]https://oncologypro.esmo.org/meeting-resources/esmo-congress-2024/a-phase-i-clinical-trial-of-intrathecal-injection-of-allogeneic-car-gdt-cells-targeting-b7h3-for-the-treatment-of-patients-with-recurrent-glioblastoma