中国自研的CAR-T疗法西达基奥仑赛注射液(Carvykti、Ciltacabtagene Autoleucel、Cilta-cel)在国内获批上市
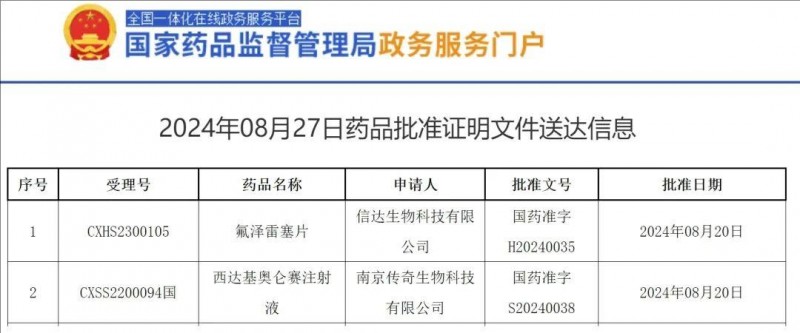
2024年08月20日,传奇生物研发的西达基奥仑赛注射液的上市申请,正式获得中国国家药品监督管理局(NMPA)的批准(受理号:CXSS2200094),用于复发或难治性多发性骨髓瘤(既往接受过1种免疫调节剂+1种蛋白酶抑制剂)的治疗。值得一提的是,西达基奥仑赛是第6款在我国获批的CAR-T产品,同时也是首款获得FDA批准的国产CAR-T疗法!以及全球目前唯一获批用于多发性骨髓瘤二线治疗的BCMA靶向疗法!
▲截图源自“NMPA”
西达基奥仑赛暴击多发性骨髓瘤,客观缓解率高达89.6%
西达基奥仑赛(cilta-cel,Carvykti,ciltacabtagene autoleucel)是由传奇生物和强生创新制药,联合研发的一款靶向BCMA的CAR-T细胞疗法。早在2024年4月5日,就曾获美国食品和药品监督管理局(FDA)批准,用于成年复发或难治性多发性骨髓瘤(R/R MM)的治疗,也是我国初代闯美成功的CAR-T产品!
西达基奥仑赛本次获批主要是基于一项在中国进行的Ⅱ期CARTIFAN-1临床研究(NCT03758417)的惊艳结果!本次共入组48位中位年龄为61岁的多发性骨髓瘤患者,经西达基奥仑赛回输治疗后,结果显示如下:
1、客观缓解率(ORR):ORR高达89.6%(95% CI,77.3~96.5)。
2、完全缓解率(CR):77.1%的患者(95% CI,62.7~88.0)在治疗后,达到完全缓解或更好。
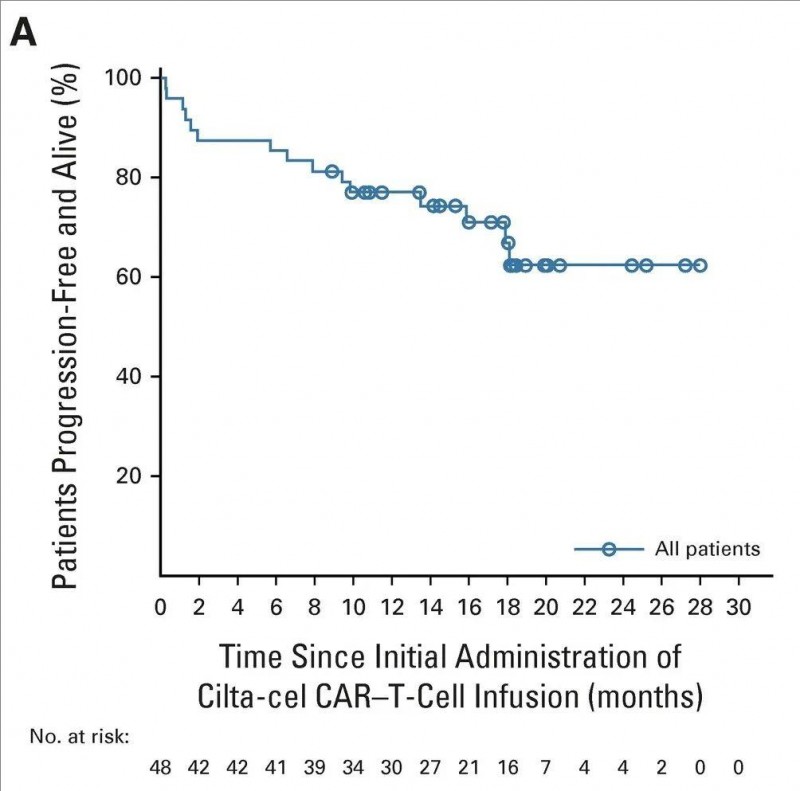
3、无进展生存(PFS)率:12个月的PFS率为77.0%(95%CI,62.3~86.5),18个月的PFS率为66.8%(95%CI,49.4~79.4),详见下图。
▲图源“JCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
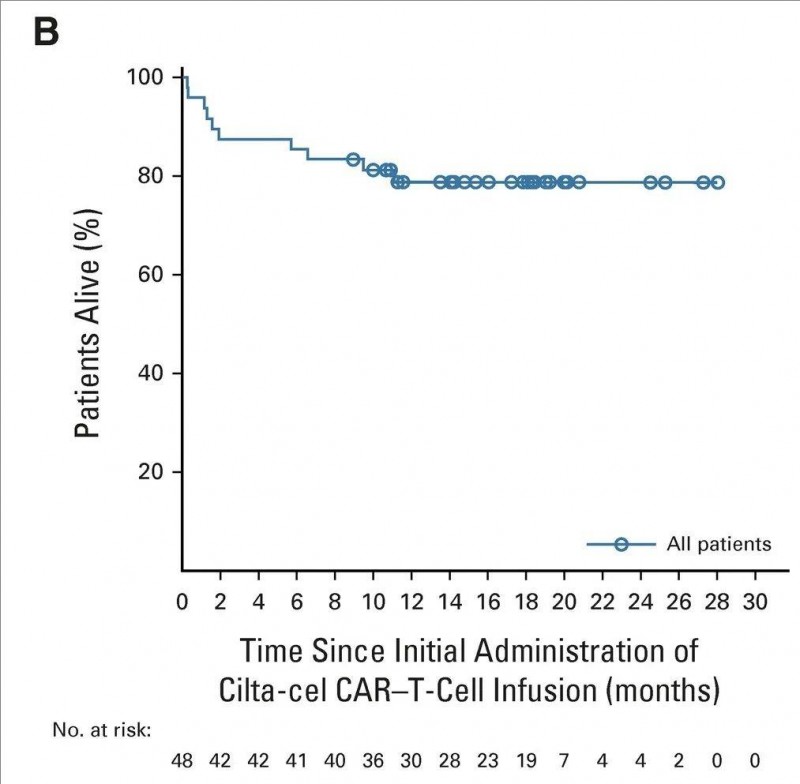
4、总生存(OS)率:18个月的OS率为78.7%(95% CI,64.0~88.0),详见下图。
▲图源“JCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
参考资料
[1]Mi J Q,et al.Phase II, open-label study of ciltacabtagene autoleucel, an anti–B-cell maturation antigen chimeric antigen receptor–T-cell therapy, in chinese patients with relapsed/refractory multiple myeloma (CARTIFAN-1)[J]. Journal of Clinical Oncology, 2023, 41(6): 1275-1284.
https://ascopubs.org/doi/10.1200/JCO.22.00690?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed
[2]Ying Z,et al.Relmacabtagene autoleucel (relma-cel) CD19 CAR-T therapy for adults with heavily pretreated relapsed/refractory large B-cell lymphoma in China. Cancer Med. 2021 Feb;10(3):999-1011.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7897944/
[3]Fu C,et al.Three-Year Follow-up on Efficacy and Safety Results from Phase 1 Lummicar Study 1 of Zevorcabtagene Autoleucel in Chinese Patients with Relapsed or Refractory Multiple Myeloma[J]. Blood,2023, 142(Supplement 1): 4845-4845.
https://www.sciencedirect.com/science/article/abs/pii/S0006497123114467
[4]https://www.nmpa.gov.cn/zwfw/sdxx/sdxxyp/yppjfb/20240827132419122.html