抗癌疫苗,48小时"起效"的癌症疫苗,强效抗击脑瘤、肺癌、胰腺癌等,近半患者病情稳定
胶质母细胞瘤是神经胶质瘤组中一种“快速生长”的脑肿瘤,异质性极强,且具有侵袭性,免疫学上“冷性”,这意味着它们对免疫反应极其不利,平均存活期约为15个月。因此,迫切需要研发新的治疗方法。
近期,佛罗里达大学的研究人员历经7年时间,研究出了一款新型mRNA癌症疫苗,首次人体临床试验结果显示,该疫苗迅速地激活免疫系统对抗癌症。在回输不到48小时内,就能迅速将“冷肿瘤”(无免疫源性的肿瘤)激活为“热肿瘤”(有免疫源性的肿瘤)。这对于解锁免疫反应的后期影响至关重要!目前其后续扩大研究仍在推进中,让我们拭目以待!
癌症疫苗:开启"打一针"防治癌症的新时代
癌症疫苗是通过激活机体的免疫系统,来识别和消除癌细胞的新型治疗方法,最终达到预防肿瘤的生长、复发和转移的目的。主要包括预防性癌症疫苗、治疗性癌症疫苗两大类,临床上所说的癌症疫苗通常指的是治疗性的癌症疫苗。
预防性癌症疫苗
常见如“宫颈癌疫苗”即“人乳头瘤病毒(HPV)疫苗”,可作为高危人群的预防措施,其目的在于预防某些癌症的发生。
治疗性癌症疫苗
可作为癌症确诊患者的治疗选择,常见包括mRNA疫苗、树突状细胞(DC)疫苗、古巴肺癌疫苗、个性化新抗原疫苗等。其中,“mRNA(信使核糖核酸)癌症疫苗”可通过编码表达肿瘤特异性抗原(如TSA、TAA),激活人体的免疫系统,以对抗体内的癌细胞,主要用于治疗非小细胞肺癌(NSCLC)、结直肠癌(CRC)、黑色素瘤等多款实体瘤。
本文开头提到的佛罗里达大学研发的这款治疗脑胶质瘤的新型癌症疫苗,就属于mRNA癌症疫苗。除了这款疫苗外,还有另一款疫苗DC疫苗也在脑瘤治疗方面,展现出了惊艳的疗效。近年来,研究人员更是不断拓展癌症疫苗的应用领域,试图实现“打一针”治疗癌症的美好愿景,让更多的癌症患者获益!
癌症疫苗重锤脑瘤、肺癌、胰腺癌
DCVax-L疫苗显著延长脑瘤患者生存期,死亡风险降低20%
世界知名期刊《影响因子(JAMA Oncol)》杂志,曾报道过一项应用“DCVax-L(即自体肿瘤裂解物负载的树突状细胞疫苗),治疗脑胶质母细胞瘤的3期非随机对照试验(NCT00045968)”。
本次研究共入组331例中位年龄为56岁(19~73岁)的胶质母细胞瘤患者,包括新诊断的胶质母细胞瘤(nGBM)、复发性胶质母细胞瘤(rGBM)。所有患者在入组前,均接受了手术切除、白细胞分离术、术后6周SOC放化疗,入组后将其随机分为两组,即DCVax-L组(232例)、安慰剂组(99例)。结果显示如下:
中位总生存期(mOS)
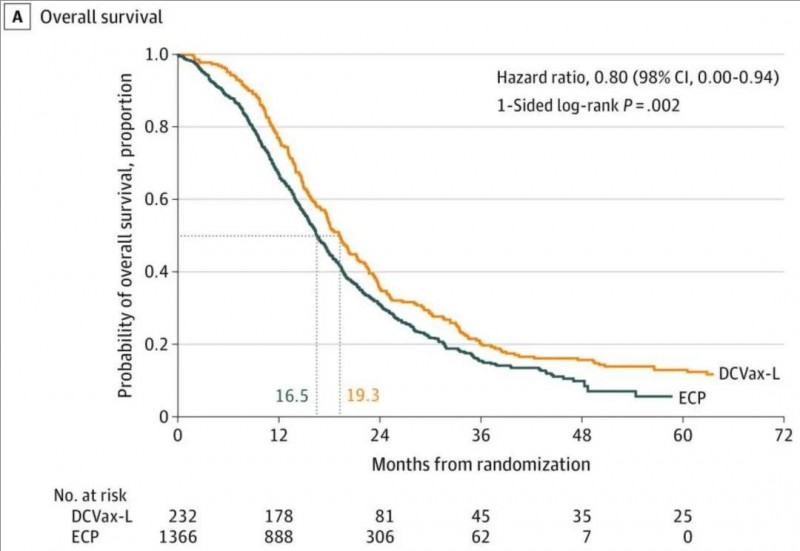
1、对于新诊断的胶质母细胞瘤(nGBM)患者(232例),中位OS为19.3个月;而对照组仅为16.5个月(详见下图)。
▲图源“JAMA Oncol”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
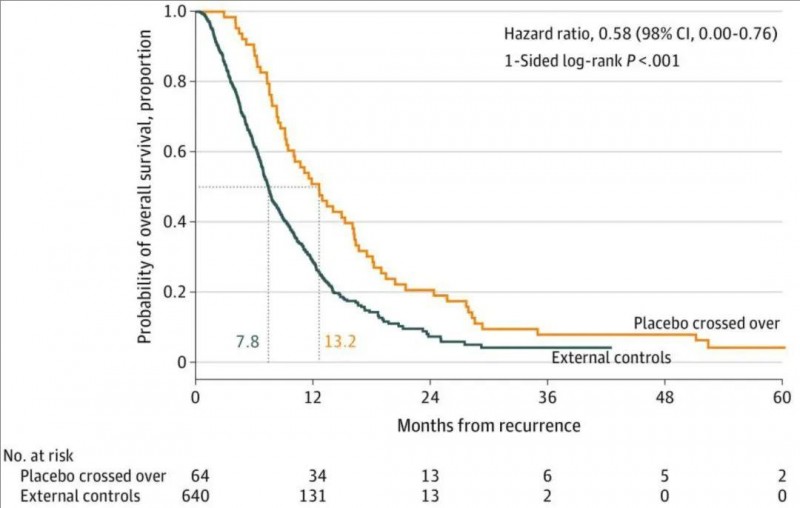
2、对于接受DCVax-L治疗的复发性胶质母细胞瘤(rGBM)患者(64例),复发后mOS为13.2个月;而对照组仅为7.8个月(详见下图)。
▲图源“JAMA Oncol”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
生存率
1、对于新诊断的胶质母细胞瘤(nGBM)患者:其死亡风险相对降低20%,且生存获益会随时间推移而显著增加。治疗48个月时的生存率为15.7%(DCVax-L组) vs 9.9%(对照组);而60个月的生存率则为13.0%(DCVax-L组) vs 5.7%(对照组)。
2、对于复发性胶质母细胞瘤(rGBM)患者:复发后24个月的生存率为20.7%(DCVax-L组) vs 9.6%(对照组);复发后30个月的生存率为11.1%(DCVax-L组) vs 5.1%(对照组)。
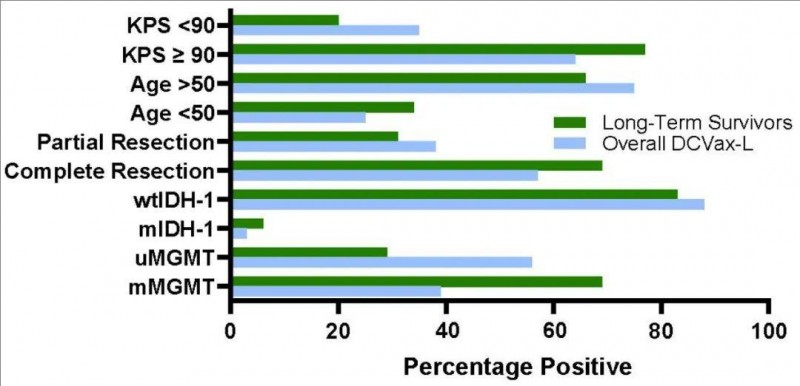
▼预后特征
▲图源“JAMA Oncol”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
总之,上述研究数据显示,DCVax-L疫苗联合SOC化疗,可使胶质母细胞瘤(包括nGBM、rGBM)患者的生存期显著延长。
目前有多款癌症疫苗,正在招募恶性实体瘤患者,包括但不限于肺鳞癌、肝癌、食道癌、结直肠癌、三阴性乳腺癌、黑色素瘤、头颈部肿瘤等癌种!
想参加临床试验的患者,可将近期病理报告、影像学检查结果、治疗经历、出院小结等资料,提交至医学部,详细评估病情!
mRNA癌症免疫疗法联合局部放疗,近半数晚期肺癌患者病情稳定
BI1361849(CV9202)是一种活性癌症免疫治疗药物,包含鱼精蛋白配制的、序列优化的mRNA,可编码六种非小细胞肺癌相关抗原包括MUC-1、MAGE-C1、MAGE-C2、NY-ESO-1、5T4、survivin,旨在诱导靶向免疫反应。
《癌症免疫治疗杂志》曾报道过“BI1361849联合局部放疗,治疗非小细胞肺癌的Ib期临床试验(NCT01915524)”结果,本次共入组的26例年龄≥18岁的IV期非小细胞肺癌(NSCLC)患者,结果显示如下:
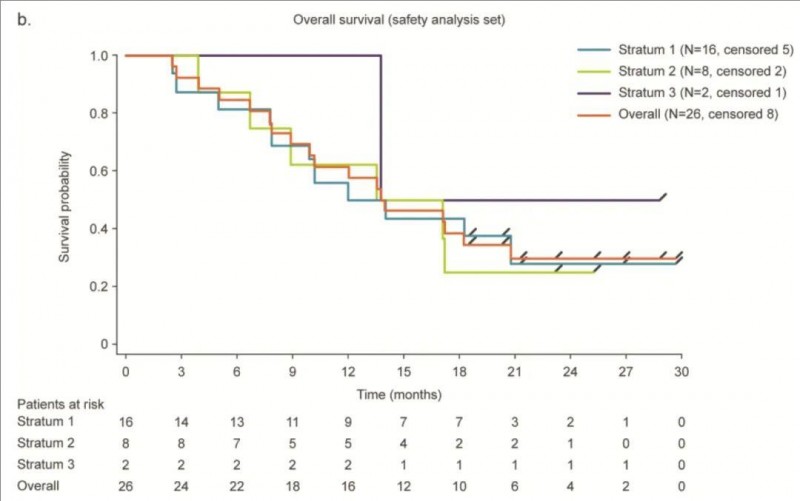
1、中位总生存期(OS):从第一次BI1361849治疗开始的中位OS为13.95个月(详见下图)。
▲图源“PMC”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
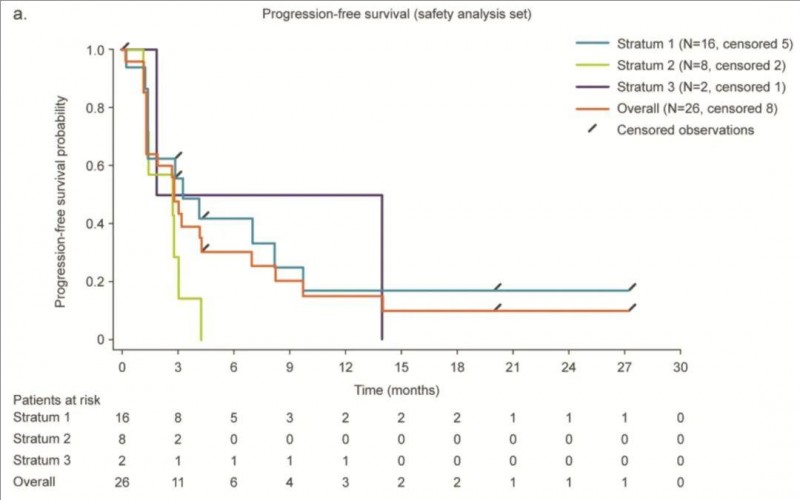
2、中位无进展生存期(PFS):入组患者的中位PFS为2.87个月(详见下图)。
▲图源“PMC”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
3、病情稳定/病灶缩小:46.2%(12/26)的患者达到病情稳定(SD)状态。截至最后1次随访,1例患者已确认达到部分缓解(PR),且肿瘤缩小范围可测量。6例患者未接受放射治疗的病变缩小>15%。
综上,BI1361849联合局部放射治疗(联合或不联合培美曲塞)耐受性良好,且检测到抗原特异性免疫反应。脑瘤因其生长位置的特殊性及其对大脑的破坏性,一直被视为病情较为凶险的一类癌种。近年来,除了mRNA、DC癌症疫苗外,CAR-T细胞疗法也在脑瘤的治疗方面,展现出了不俗的效果。
BNT122疫苗清除微转移病灶,胰腺癌中位RFS长达13.4个月
BNT122(自体cevumeran,RO7198457)属于一款个体化新抗原mRNA疫苗,用于胰腺导管腺癌(PDAC)的治疗,可编码超过20种特异性新抗原。2024年AACR年会上,公布的该疫苗1期试验临床试验(NCT04161755)显示,BNT122疫苗有助于延缓胰腺癌复发、延长患者的生存时间,该结果同步发表在国际权威期刊《Nature》上。
本次入组的28例既往接受过手术治疗的胰腺导管腺癌(PDAC)患者,入组接受BNT122疫苗+阿替利珠单抗或改良版四药化疗方案(mFOLFIRINOX,包括氟尿嘧啶、伊立替康、亚叶酸、奥沙利铂)。
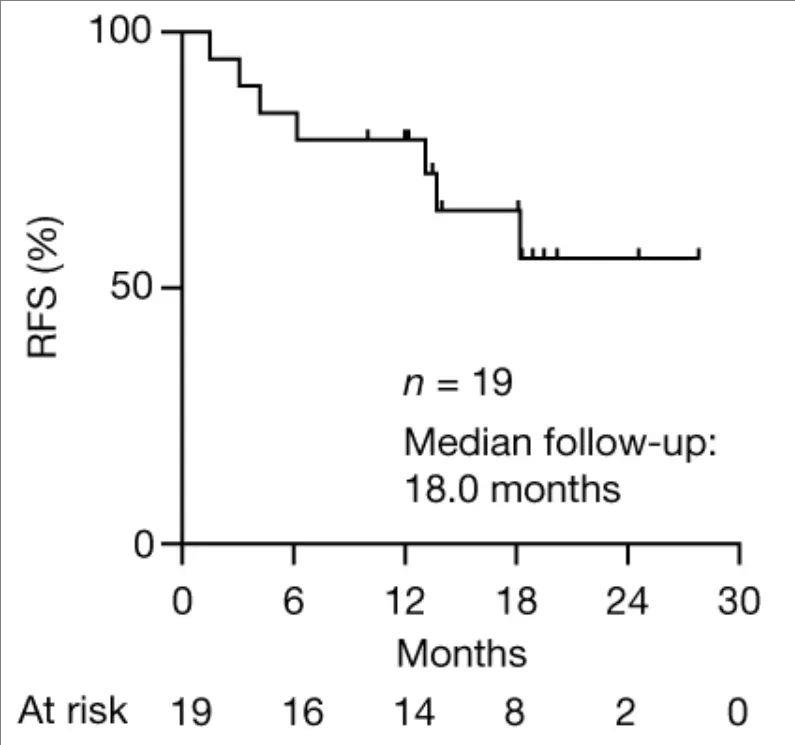
结果显示如下:接种疫苗但未产生疫苗诱导的T细胞患者,中位无复发生存期(RFS)长达13.4个月(详见下图)。
▲图源“nature”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
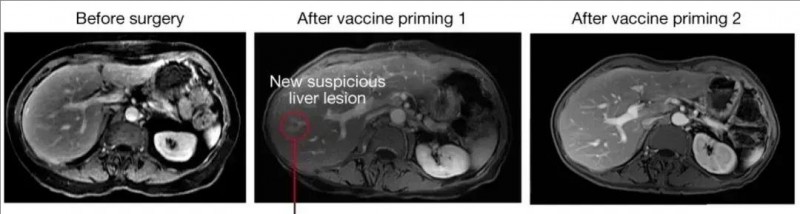
值得一提的是,其中1例患者(29号)在接种疫苗后,出现血清CA19-9水平升高,肝脏虽出现新的微小病变(7mm左右),但该病灶在后续的成像中消失。这也意味着,BNT122疫苗可能具有清除肿瘤微转移的能力(详见下图)。
图1 29号患者在回输疫苗前后腹部MRI的对比图
▲图源“nature”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
小编寄语
mRNA癌症疫苗作为癌症疫苗领域的一股清流,既能刺激强大的免疫反应,又能降低不良反应,增强机体抗癌的能力!
截至目前,美国国立卫生研究院(NIH)临床试验网站上共收录了7000余项在研的癌症疫苗项目,其中mRNA疫苗就多达600余项,此外,还包括树突细胞(DC)疫苗、新抗原疫苗等,wield肺癌、胰腺癌、肝癌、乳腺癌、黑色素瘤等实体瘤患者,带来了新的曙光!近日佛罗里达大学的研究人员更是将目光聚集到高度危险且难治的脑瘤上,并研制出针对脑瘤的mRNA疫苗,为人类攻克癌症的大业添砖加瓦!小编也期望能迎来更多癌症疫苗获批上市的好消息,让更多的实体瘤患者获益,最终实现“打一针就能精准抗癌”的美好愿景!
想寻求mRNA疫苗、古巴肺癌疫苗、DC疫苗或国内外其他抗癌新技术帮助的病友,可将近期病理报告、治疗经历、影像学资料等,提交到医学部,进行初步评估或申请国内外抗癌专家会诊。
参考资料
[1]Mendez-Gomez H R,et al.RNA aggregates harness the danger response for potent cancer immunotherapy[J]. Cell, 2024, 187(10): 2521-2535. e21.
https://www.cell.com/cell/abstract/S0092-8674(24)00398-2
[2]Liau LM,et al.Association of Autologous Tumor Lysate-Loaded Dendritic Cell Vaccination With Extension of Survival Among Patients With Newly Diagnosed and Recurrent Glioblastoma: A Phase 3 Prospective Externally Controlled Cohort Trial. JAMA Oncol. 2023 Jan 1;9(1):112-121.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9673026/
[3]Papachristofilou A,et al.Phase Ib textareauation of a self-adjuvanted protamine formulated mRNA-based active cancer immunotherapy, BI1361849(CV9202), combined with local radiation treatment in patients with stage IV non-small cell lung cancer. J Immunother Cancer. 2019 Feb 8;7(1):38.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6368815/
[4]Rojas L A,et al.Personalized RNA neoantigen vaccines stimulate T cells in pancreatic cancer[J]. Nature, 2023, 618(7963): 144-150.
https://www.nature.com/articles/s41586-023-06063-y