2024年6月14日FDA批准PD-L1抑制剂度伐利尤单抗注射液(Durvalumab、英飞凡/Imfinzi)用于治疗原发性晚期或复发性子宫内膜癌
2024年6月14日,美国食品药品监督管理局(FDA)批准阿斯利康的PD-L1抑制剂度伐利尤单抗注射液(Durvalumab、英飞凡/Imfinzi)联合卡铂和紫杉醇,随后序贯度伐利尤单抗单药治疗错配修复缺陷(dMMR)的原发性晚期或复发性子宫内膜癌成人患者。这一新适应症的获批,为dMMR子宫内膜癌患者带来了新的治疗选择和希望。
获批信息概览
度伐利尤单抗是一种人源化的PD-L1单克隆抗体,其独特的免疫调节机制使其在抗肿瘤治疗中展现出巨大潜力,此次FDA的批准基于DUO-E(NCT04269200)这一全球性、随机、多中心、双盲、安慰剂对照的III期临床研究结果,该研究表明,度伐利尤单抗联合化疗在dMMR的子宫内膜癌患者中显示出显著的无进展生存期(PFS)延长,为这一难治性疾病的治疗带来了革命性的变化。
获批依据
一、临床试验的严谨性
1.试验设计:
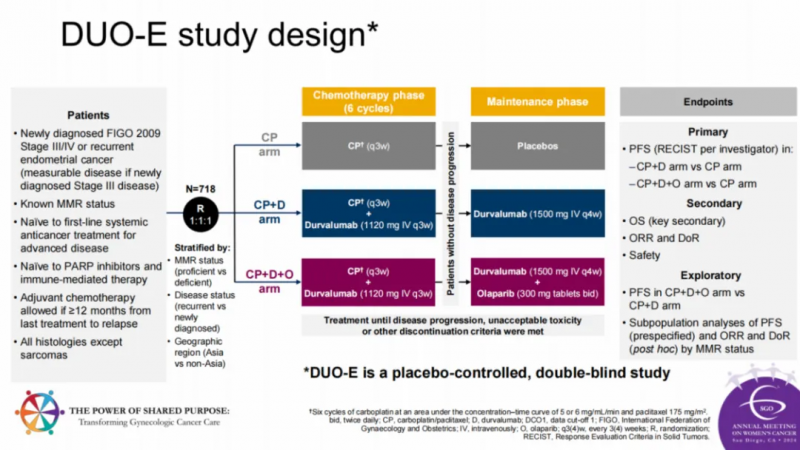
DUO-E试验采用全球性的双盲设计,确保了研究结果的客观性和可靠性,双盲设计意味着患者和研究者均不知晓患者接受的是治疗药物还是安慰剂,从而减少了主观偏倚对研究结果的影响,此外,该试验还设有安慰剂对照组,为评估度伐利尤单抗的疗效提供了科学的基准。
度伐利尤单抗治疗子宫内膜癌的临床试验设计
2.患者招募与分组:
试验招募了≥18岁的新诊断晚期III/IV期或复发性子宫内膜癌(组织学类型为上皮癌,不包括肉瘤)的患者,复发性患者的入组标准严格,要求既往接受的系统性抗癌治疗必须作为辅助治疗,且最后一次给药需在复发前至少12个月,以确保患者处于相对稳定的疾病状态;患者按1:1:1的比例随机分配至三个治疗组,分别接受度伐利尤单抗联合卡铂/紫杉醇治疗并随后单药治疗、安慰剂加卡铂/紫杉醇治疗并随后安慰剂维持治疗,以及度伐利尤单抗联合卡铂/紫杉醇后再联合奥拉帕利治疗。
二、关键疗效数据
1.无进展生存期(PFS)分析:
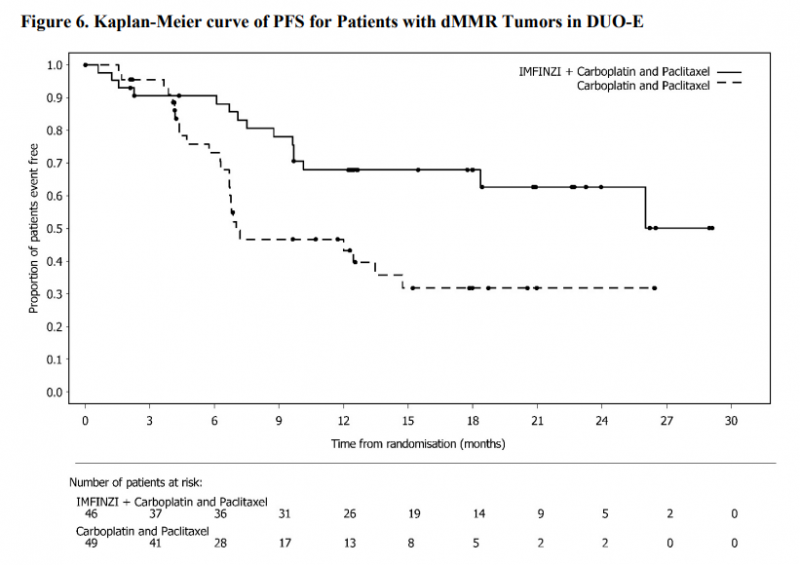
在dMMR(错配修复缺陷)亚组中,度伐利尤单抗组的中位PFS未达到(NR;95%CI,NR-NR),显示出显著的疗效优势,相比之下,安慰剂组患者的中位PFS仅为7个月(95%CI,6.7-14.8),这种差异在统计学上高度显著(HR,0.42;95%CI,0.22-0.80),充分证明了度伐利尤单抗在dMMR子宫内膜癌患者中的治疗价值。
DUO-E研究中dMMR患者疗效数据
DUO-E研究中dMMR患者的PFS曲线
2.总生存期(OS)趋势:
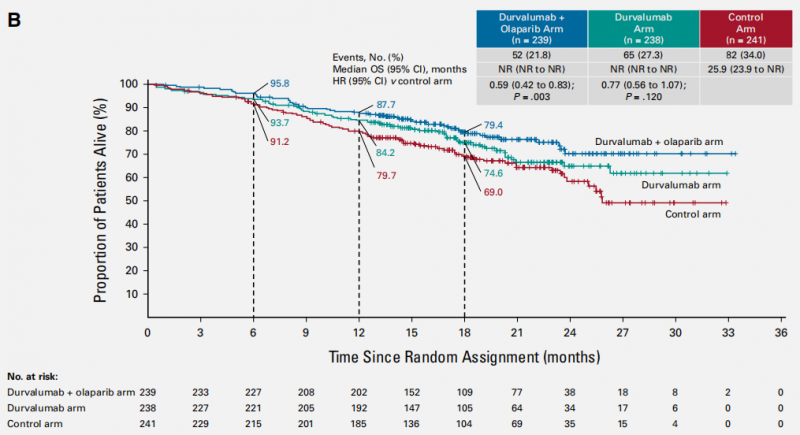
尽管总生存期数据尚未成熟,但初步分析显示度伐利尤单抗组及度伐利尤单抗加奥拉帕利组的OS均优于安慰剂组,呈现出积极的治疗趋势,这一发现进一步支持了度伐利尤单抗在延长患者生存时间方面的潜力。
OS数据
三、安全性与耐受性
度伐利尤单抗联合化疗方案的安全性评估显示,超过25%的患者报告了常见不良反应,包括周围神经病变、肌肉骨骼疼痛、恶心、脱发、疲劳等。这些不良反应多为轻至中度,且通过适当的医疗管理和支持治疗可得到有效控制,因此,度伐利尤单抗在dMMR子宫内膜癌患者中的治疗被认为是安全且可耐受的。
综上所述,DUO-E试验的严谨设计、显著的疗效数据以及良好的安全性与耐受性共同构成了FDA批准度伐利尤单抗联合卡铂和紫杉醇治疗dMMR原发性晚期或复发性子宫内膜癌患者的坚实依据,这一批准不仅为子宫内膜癌患者提供了新的治疗选择,也为肿瘤免疫治疗领域的发展注入了新的活力。
总的来说,度伐利尤单抗新适应症获批,为dMMR子宫内膜癌患者带来了新的治疗选择和希望,随着免疫治疗在肿瘤领域的不断发展,相信未来会有更多患者从中受益。