突发!AMG510和TAK-788(莫博赛替尼)可能面临退市,KRAS G12C突变靶向药和EGFR20基因突变靶向药还有哪些
国庆“黄金周”里,癌症领域接连迎来了两项重磅新闻——或者说是两个巨大“噩耗”:历史上首款KRAS G12C靶向药AMG510(索托拉西布,Sotorasib),与第二款EGFR ex20ins靶向药TAK-788(莫博赛替尼,Mobocertinib),先后因种种原因而传递出了退市的信号。
2023年10月2日,武田制药发布公告,自愿在美国撤回TAK-788(莫博赛替尼,Mobocertinib),并计划在全球范围内自愿撤回,目前正在与所有批准了莫博赛替尼的国家/地区的监管机构进行合作,推进后续的步骤。
同月5日,FDA肿瘤药物咨询委员会(ODAC)针对AMG510(索托拉西布,Sotorasib)的Ⅲ期CodeBreaK 200试验(NCT04303780)结果进行了投票表决,以10比2的票数,认为目前试验数据并不能支持AMG510的疗效优势。因此,AMG510也可能要面临撤回加速批准或退市的未来。
几乎在同时,肺癌两个新兴且难治的靶点、两款经典靶向药面对撤回的窘境——这是否意味着两个靶点的治疗水平开了“倒车”?
事实并非如此!
肺癌两大"难治"靶点,新药正在稳步"崛起"
事实上,KRAS G12C与EGFR ex20ins是非小细胞肺癌近期最受重视的“难治”靶点当中的两大代表。其中KRAS G12C在非小细胞肺癌中检出率有大约15%~20%,EGFR ex20ins的检出率大约在5%~10%左右。即使仅计算中国境内,这两个靶点会影响到的患者,每年都以百万级的数量在增加。
而针对这两个靶点的非小细胞肺癌,新药正以“井喷”般的数量与速度,快速地投入临床。AMG510和TAK-788是其中比较有代表性的两款,但并非全部。还有更多新药具有相似或更高的疗效,或已经获批、或处于临床试验阶段,这些药物也能够成为患者的选择。
KRAS G12C:AMG510率先"破冰",但并非唯一的"救命稻草"
作为近几年最热门的靶点,KRAS G12C的新药数量非常之多。不论是国内还是国外,已经在临床研究当中展现出疗效优势的新药不胜枚举。
1、阿达格拉西布
阿达格拉西布(Adagrasib,MRTX849)治疗KRAS G12C突变的非小细胞肺癌患者,整体缓解率为44%,疾病控制率为81%,中位缓解持续时间为12.5个月,中位总生存期14.1个月。
2023年的世界肺癌大会上,阿达格拉西布还公布了最新的长期随访数据,随访时间已经超过了2年!这个数据已经比较具有说服力。
中位随访26.9个月时,接受阿达格拉西布(MRTX849,Adagrasib)治疗的患者整体缓解率为43.0%,中位缓解持续时间为12.4个月;中位无进展生存期为6.9个月;患者1年无进展生存率为35.0%;中位总生存期为14.1个月,患者1年及2年生存率分别为52.8%和31.3%。
报告中还分析了KRAS G12C与其它基因共突变患者接受治疗的疗效:KRAS G12C与KEAP1共突变患者中位总生存期为5.7个月;KRAS G12C与STK11共突变患者中位总生存期为9.2个月;KRAS G12C与TP53共突变患者中位总生存期为18.7个月。
除此以外,脑转移患者也能获得很好的治疗:基线脑转移患者的中位总生存期达到了18.7个月。
2、JAB-21822
Glecirasib(JAB-21822)是一款由加科思自主研发的KRAS G12C抑制剂,目前已经在中国、美国及欧洲多国启动多项针对晚期实体瘤患者的临床试验项目。目前,JAB-21822已经获得了NMPA授予的突破性疗法称号,用于治疗胰腺癌。
根据此前公布的Ⅰ/Ⅱ期试验(NCT05009329)数据,JAB-21822用于治疗KRAS G12C突变的晚期实体瘤患者,整体缓解率为40.8%,疾病控制率91.8%。
在2022年ASCO年会上,研究者曾经公布JAB-21822治疗KRAS G12C突变非小细胞肺癌的Ⅰ期临床数据,整体缓解率为56.3%,疾病控制率更是高达90.6%。
除此以外,在400 mg/d及800 mg/d剂量组中,患者的整体缓解率更是达到了66.7%,疾病控制率100%。
3、D-1553
D-1553是一款益方生物自主研发的口服KRAS G12C抑制剂,在包括非小细胞肺癌在内的多类实体瘤当中具有良好的治疗潜力。
此前2022年ASCO大会上,上海胸科医院陆舜教授曾经公开了D-1553治疗多类KRAS G12C突变的实体瘤患者的疗效。结果显示,患者的整体缓解率为40.4%,疾病控制率高达90.4%。
4、IBI351
IBI351(GFH925)已经获得了NMPA授予的突破性疗法称号,用于治疗KRAS G12C突变且既往接受过至少1线全身治疗的晚期非小细胞肺癌患者。
对于非小细胞肺癌,IBI351单药治疗的整体缓解率为50.9%,疾病控制率92.7%;其中600 mg、每日2次的剂量组,整体缓解率达到了61.9%,疾病控制率更是有100%。
5、GDC6036
GDC-6036是一款口服KRAS G12C抑制剂,与对应靶点不可逆地结合,关闭其致癌信号传导。临床前研究(体外研究)结果表明,与已经上市的两款KRAS抑制剂Sotorasib和Adagrasib相比,GDC-6036的选择性更强。
近期发布于《新英格兰医学杂志》上的数据显示,在KRAS G12C突变的非小细胞肺癌当中,GDC-6036的整体缓解率为53.4%。
根据2022年世界肺癌大会期间公布的数据,GDC-6036治疗KRAS G12C突变的非小细胞肺癌患者,整体缓解率高达53%(其中46%已经得到影像学确认)。在受试的患者当中,90%曾经接受过铂类药物化疗,86%曾经接受过免疫检查点抑制剂治疗。
此外根据2023年世界肺癌大会上的报告,在12例曾经接受过KRAS G12C抑制剂治疗的非小细胞肺癌患者当中,JDQ443+TNO155治疗的整体缓解率为33.3%,疾病控制率为66.7%。
6、JDQ443
JDQ443是一款口服KRAS G12C抑制剂,对于包括非小细胞肺癌在内的各类实体瘤都有很好的治疗潜力。此前公布的数据,JDQ443用于治疗包括非小细胞肺癌、结直肠癌、胰腺癌和卵巢癌等在内的KRAS G12C突变患者,整体缓解率可以达到28.2%(其中已确认的整体缓解率为20.5%),疾病控制率82.1%。
申请KRAS G12C抑制剂的新药临床试验需要满足什么条件呢?
●能够配合接受临床试验、使用新药;
●晚期非小细胞肺癌;
●携带KRAS G12C突变。
AMG510:联合方案也有可能成为新出路
若单药方案无法提供足以超越保准方案的疗效,专家们自然而然地想到了联合方案——通过联合治疗的方案,例如靶向+化疗、或靶向+免疫等,是否能够获得更好的疗效?
正巧,在今年的世界肺癌大会大会上,一项使用索托拉西布联合化疗的临床试验公布了最新的数据。
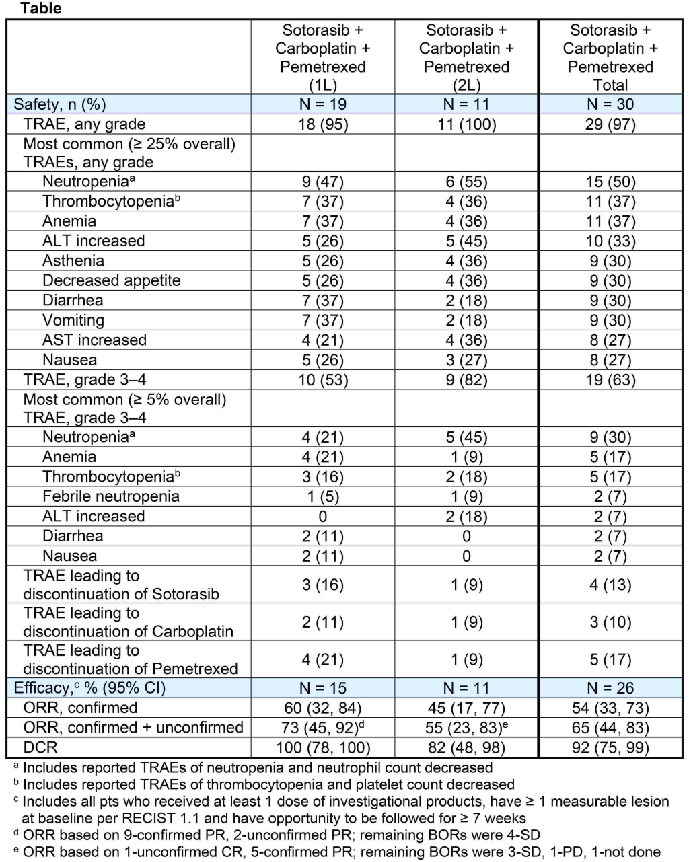
根据报告,使用索托拉西布+卡铂+培美曲塞治疗KRAS G12C突变患者,作为一线方案时的整体缓解率高达73%,作为二线方案时的整体缓解率也达到了55%。
尽管在联合化疗之后,患者发生不良事件、导致停药的风险略有升高,但从疗效上来分析,联合方案仍然为患者提供了一种获得更好疗效的途径。
EGFR ex20ins:新药分为4类,每类都已经出现了代表药
而EGFR ex20ins突变亚型的治疗,可以说是更加“多样化”,目前已经公布过临床试验数据的治疗策略就已经超过了4种,每一种都已经出现了“代表药”。对于这类突变的患者来说,即使有一条路上的一个小岔路“走不通”,也仍然还有很多新的道路可以尝试。
1、伏美替尼:缓解率最高可达70%
根据2023年世界肺癌大会(WCLC)上分享的Ⅰb期FAVOUR试验(NCT04858958)的报告,在初治患者当中,接受伏美替尼(Furmonertinib)240 mg QD治疗的患者整体缓解率高达78.6%,初步的中位缓解持续时间达到15.2个月;此外用于已经接受过前线治疗的经治患者,伏美替尼在240 mg和160 mg剂量组中的整体缓解率也分别达到了46.2%和38.5%。
2、PLB1004:缓解率57.7%
根据PLB1004目前已经公布的数据,在治疗剂量≥160mg QD组中,患者的整体缓解率为57.7%,疾病控制率更是达到了100%;其中脑转移患者接受治疗的整体缓解率仍然达到了37.5%。
3、CLN-081:缓解率可达41.0%
Zipmetainib(CLN-081,TAS6417)治疗EGFR ex20ins突变非小细胞肺癌,在所有剂量组中,患者的整体缓解率为38.4%,疾病控制率为95.9%。100毫克剂量组患者整体缓解率最高,为41.0%。患者的中位无进展生存期为10个月;其中100毫克剂量组最长,为12个月。
4、舒沃替尼:缓解率可达52.4%
根据2023年ASCO大会上公布的Ⅱ期WU-KONG6试验数据,用于治疗经治的EGFR ex20ins突变非小细胞肺癌,舒沃替尼在300 mg剂量组中的整体缓解率高达60.8%,疾病控制率为87.6%。
根据报告,接受舒沃替尼治疗的患者,90%实现了肿瘤缩小;其中更是有部分患者已经接受过了埃万妥单抗(JNJ-6372,一款EGFR/MET双抗,已经获批用于治疗EGFR ex20ins突变的经治晚期非小细胞肺癌)治疗,再使用舒沃替尼同样有缓解的案例。
申请EGFR ex20ins抑制剂的新药临床试验需要满足什么条件呢?
●能够配合接受临床试验、使用新药;
●晚期非小细胞肺癌;
●携带EGFR ex20ins突变。
加速批准是FDA在前几年开始推行的新政策,相比起以往的正式批准,加速批准能够帮助药物更早地上市,一方面让患者们更早用上新药,另一方面也能够让药企更快收回成本、继续下一阶段的研发。
这样做的优势明显:很多新药通过这一策略提前获得批准上市之后,又凭借着下一阶段出色的数据转为正式批准,例如RET抑制剂普拉替尼等;但风险也是存在的:有些新药在后续的Ⅲ期临床试验之中被发现数据并不具有足够的说服力,药物与原有方案相比优势并不大,就比如这次的AMG510和TAK-788。
加速批准的策略,当然也包括目前被视为癌症患者“救命稻草”的临床试验,就像是一把双刃剑。它们同时带来了“提前用上新药”的好处,以及“疗效存在不确定性”的风险。作为患者,如果能够好好利用这些策略的优势、合理规避风险,这些提前“露面”的新药同样能够成为癌症患者对抗肿瘤、延长生命的“好帮手”。
如果您对于临床试验还有任何疑问,或者希望寻找更新、更适合自己的治疗方案,希望寻求日美等国癌症专家的诊疗意见,可以联系全球肿瘤医生网医学部获得帮助。