2023AACR大会(度的美国癌症研究协会年会)精彩集锦:4代靶向药、癌症疫苗等8类抗癌新疗法震撼登场
近期,2023年度的美国癌症研究协会年会圆满落下帷幕。今年AACR年会上公布了众多癌症治疗最新进展,这场国际盛会可谓是饕餮盛宴,众多新药新疗法纷纷亮相,向癌症宣战。
AACR(美国研究协会)是世界上成立最早,规模最大的致力于全面、创新和高水准癌症研究的科学组织。它与美国临床肿瘤学会 (ASCO) 和欧洲肿瘤内科学会 (ESMO) 并称为全球三大癌症学会。全球肿瘤医生网医学部为大家盘点了会议上最值得关注的8大进展,覆盖了常见的癌症类型,希望给大家带来战胜癌症的信心。
一、打破奥希替尼耐药困境!肺癌第4代靶向药BBT-176横空出世
摘要号:4018
研究名称:BBT-207 是一种广谱、高效的第 4代EGFR TKI,对包括 T790M 和 C797S 在内的致敏和治疗出现的 EGFR 突变具有增强的活性
研究摘要:BBT-207 对激活和获得性耐药EGFR具有广泛的活性。BBT-207 是一种可逆的、突变体特异性的广谱 TKI,对临床观察到的EGFR突变具有活性,可以很好地增强EGFR突变 NSCLC 的治疗,无论是针对获得性耐药还是早期治疗,都有可能治疗或预防脑转移。
Jimmy Jin博士说“我们相信 BBT-207 有潜力成为广谱第四代 EGFR TKI,并有能力通过组合进一步增强治疗。
二、第4代ALK抑制剂NVL-655强效抗脑转
摘要号:4022
研究名称:NVL-655 在含有 EML4-ALK 融合与 G1202R 突变的艾来替尼耐药患者衍生模型中的临床前颅内活性
研究摘要:NUV-655是Nuvalent 公司研发的第4代ALK/ROS1酪氨酸激酶抑制剂。这种新型的脑渗透性 ALK 选择性抑制剂可以克服目前可用疗法局限性。NVL-655 旨在在对第一代、第二代和第三代 ALK 抑制剂产生耐药性的肿瘤中保持活性,包括具有溶剂前沿 G1202R 突变或复合突变 G1202R / L1196M(“GRLM”)、G1202R / G1269A(“GRGA”)或 G1202R/L1198F(“GRLF”)。
脑转移在 ALK 阳性非小细胞肺癌 (NSCLC) 中很常见,在第一代 ALK TKI(克唑替尼)由于其有限的脑渗透性,诊断时的发病率约为 40%,在疾病进展后约为 60% . 第二代(ceritinib、alectinib、brigatinib 和 ensartinib)和第三代(lorlatinib)ALK TKI 比克唑替尼具有更高的颅内反应,但仍受到耐药突变出现的限制,最常见的是含有 G1202R 的单一突变和复合突变。在这里,进一步证明了 NVL-655 在包含 EML4-ALK v3 G1202R 的临床前患者衍生模型中的颅内活性。
三、新型癌症疫苗为晚期肺癌患者带来全新希望
摘要号:LB196
研究名称:NOUS-PEV,一种针对新抗原的个性化癌症疫苗,可诱导持久的肿瘤浸润记忆 T 细胞
研究摘要:
NOUS-PEV 是一种个性化的癌症免疫疗法,根据患者肿瘤特有突变的选择和优先排序,为每位患者个体化设计新抗原癌症疫苗。NOUS-PEV 正在 1b 期临床试验 (NCT04990479) 中进行评估,包括黑色素瘤及非小细胞肺癌(NSCLC)。
四、治疗KRAS突变更强效的疗法来了
摘要号:5739
研究名称:靶向 WEE1 改善 KRAS G12C 突变非小细胞肺癌的治疗!
研究摘要:
虽然 sotorasib 是第一个在非小细胞肺癌 (NSCLC) 中获得临床批准的 KRAS G12C 小分子抑制剂,但单独使用 sotorasib 的疗效有限,可能是由于癌细胞的适应性耐药机制。为了扩大 sotorasib 的治疗潜力,需要开发组合策略。在这项研究中,进行了大规模筛选,以确定与 sotorasib 的新型组合候选药物。此外,在多个临床前模型中研究了协同效应的分子机制。
WEE1抑制剂 (AZD1775),是一种处于临床阶段开发中的 G2/M 检查点消除剂,作为 sotorasib 在 KRAS G12C 突变型 NSCLC 中的有前途的联合方案 。在多个 KRAS G12C 突变体 NSCLC 细胞系中广泛观察到体外协同作用。临床前研究表明,与单独使用单一药物的小鼠相比,接受 sotorasib 和 AZD1775 治疗的小鼠具有显着的肿瘤消退和持久反应。因此将 WEE1 抑制剂 AZD1775 鉴定为一种新型联合候选药物,它增强了 sotorasib 在体外和体内临床前模型中的抗肿瘤活性。这些发现可以为 KRAS G12C 突变型非小细胞肺癌提供一种新的治疗策略。
五、62%患者肿瘤显著缩小!新一代KRAS抑制剂为肠癌患者带来希望
Divarasib (代号GDC-6036) 是一种在研、口服、高效和选择性 KRAS G12C 抑制剂。
在代号为GO42144 的Ib期研究中,29 名患有晚期或转移性KRAS G12C阳性结直肠癌患者入组,这些患者都是至少接受过2种治疗方案失败的晚期患者,接受了 divarasib 和西妥昔单抗治疗。
结果显示:这款药物具有良好的临床活性和可控的安全性. 66% (n=19/29) 的患者获得了未确认的总体反应,62% (n=18/29) 的患者获得了确认的总体反应。这意味着超60%的晚期患者肿瘤显著缩小30%以上!更值得一提的是在 5 名先前接受过 KRAS G12C 抑制剂治疗的患者中,3 名患者对 divarasib 治疗出现反应,这意味着耐药的患者也有了”续命“新选择。
Desai博士说“反应是持久的——18 名有反应的患者中有 14 名继续接受积极治疗,而我们目前还没有可以报告的中位反应持续时间或中位无进展生存期。”
注:做了基因检测的病友可以拿出报告看看一旦存在KRAS突变,可以马上联系全球肿瘤医生网医学部看看是否有机会接受国内新药治疗,看不懂的病友也可以致电全球肿瘤医生网医学部解读报告。
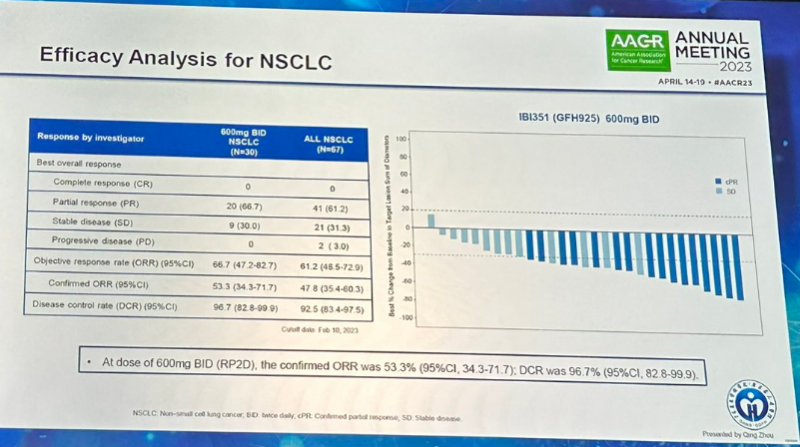
六、近100%患者病灶缩小或控制稳定!国研肺癌新药IBI351最新数据公布
IBI351 (GFH925) 是一款国研的新型、具有口服活性的强效 KRAS G12C 抑制剂,通过阻断KRAS依赖的信号转导,抑制肿瘤细胞的增殖,并诱导细胞凋亡。临床前研究显示 IBI351 对 KRAS G12C 具有高选择性,IBI351 有效抑制下游信号通路,诱导肿瘤细胞凋亡和细胞周期停滞。
在2023年AACR大会上,国研强效KRAS抑制剂IBI351 (GFH925)公布的最新Ⅰ期临床研究结果 (CTR20211933) 带来惊喜。
截至2023年2月10日,67例已接受标准治疗失败或不耐受的非小细胞肺癌患者接受了不同剂量的IBI351治疗。
结果显示:
总客观缓解率(ORR)为61.2%,疾病控制率(DCR)为92.5%。
值得一提的是,这款药物在600mg剂量组30例可评估受试者中展现出更加卓越的疗效,客观缓解率高达66.7%(20/30),这意味着近70%的晚期肺癌患者肿瘤显著缩小30%以上;疾病控制率(DCR)高达96.7%。这意味着几乎所有的患者病灶都出现了不同程度的缩小或控制稳定!
七,预防复发,延长生存期!新型癌症疫苗震撼登场
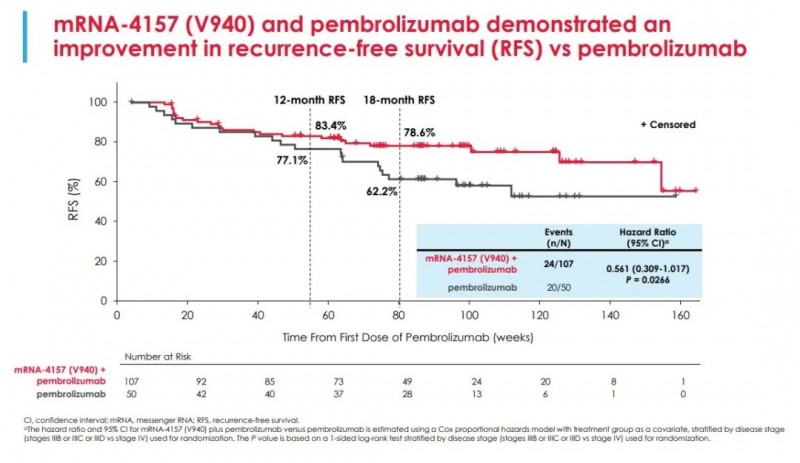
2023年AACR大会上,一款由大名鼎鼎的Moderna疫苗公司研发的,在国际上备受瞩目的新型个体化癌症疫苗mRNA-4157(V940)公布了最新的代号为 mRNA-4157-P201/KEYNOTE-942 2b 期试验最新数据 (NCT03897881) ,结果非常振奋人心。
数据显示:在157 名中晚期黑色素瘤患者中,与单独使用PD-1(K药)相比,接受癌症疫苗mRNA-4157/V940 联合PD-1(K药)作为辅助治疗,癌症疫苗组的18 个月无复发生存率(RFS)为 78.6%,而PD-1组为 62.2%,这意味着癌症疫苗可将复发或死亡风险显著降低 44%!
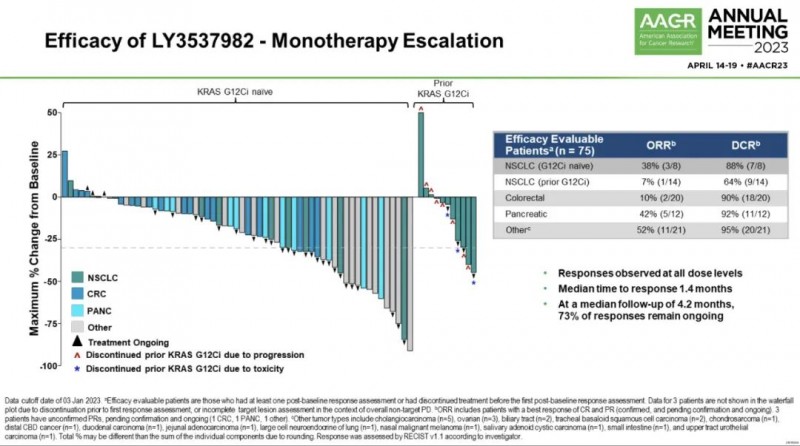
八、疾病控制率高达88%!新型KRAS抑制剂对多种实体瘤有效
LY3537982是一款新一代的KRAS G12C特异性抑制剂。在2021年的AACR大会上公布的临床前研究数据显示,这款药物具有良好的活性,在携带KARS G12C变异的肺癌细胞系中,LY3537982能够抑制KRAS与GTP结合。在多种包含KRAS G12C基因变异的小鼠肿瘤模型中,LY3537982能够显著抑制肿瘤增殖或导致肿瘤完全消退。
在2023年AACR大会上,这款药物公布了代号为LOXO-RAS-20001 (NCT04956640)最新的1a/1b 期实验数据,非常鼓舞人心。
结果显示:
客观缓解率(ORR):
初治(未接受过KRAS抑制剂治疗)的非小细胞肺癌患者为38%;
经治非小细胞肺癌为7%;
结直肠癌为10%;
胰腺癌为42%;
其他癌症为52%。
此外,KRAS G12C 抑制剂初治患者的疾病控制率 (DCR) 高达 88%,这意味着近90%的患者接受治疗后肿瘤出现不同程度的缩小或控制稳定;对于先前接受过 KRAS G12C 抑制剂的患者,DCR 为 64%。
以上最新进展仅为2023AACR大会上的一小部分,我们生活在癌症治疗的分子革命中,越来越多的癌症患者通过一代一代的靶向药和免疫治疗药物获得了更长的生存期,甚至把肿瘤吃没了。进入靶向免疫治疗时代,每个癌症患者都应该通过基因检测,PD-L1,TMB分析,获得更多用药方案指导。我们已经了解了很多关于癌症的分子遗传学以及如何将它转化临床治疗决策。未来还将有更多。