脑膜瘤基因检测,基因检测除了能指导脑膜瘤预后分级和治疗还能检测遗传风险
脑膜瘤是源自中枢神经系统蛛网膜的缓慢生长的肿瘤,大约 90% 的脑膜瘤在发生在颅内,其余 10% 发生在椎管内。脑膜瘤是成人中最常见的原发性中枢神经系统颅内肿瘤,通常引起癫痫发作、局灶性神经功能缺损或颅内压升高的症状(如头痛或恶心)。
脑膜瘤占所有原发性颅内肿瘤的39%,占所有非恶性原发性颅内肿瘤的 54.5%,中位诊断年龄为 66 岁。2014-2018 年美国的发病率为 9.49/100,000,女性发病率更高。仅在美国2021 年就有大约 36,130 名患者被诊断出患有脑膜瘤。
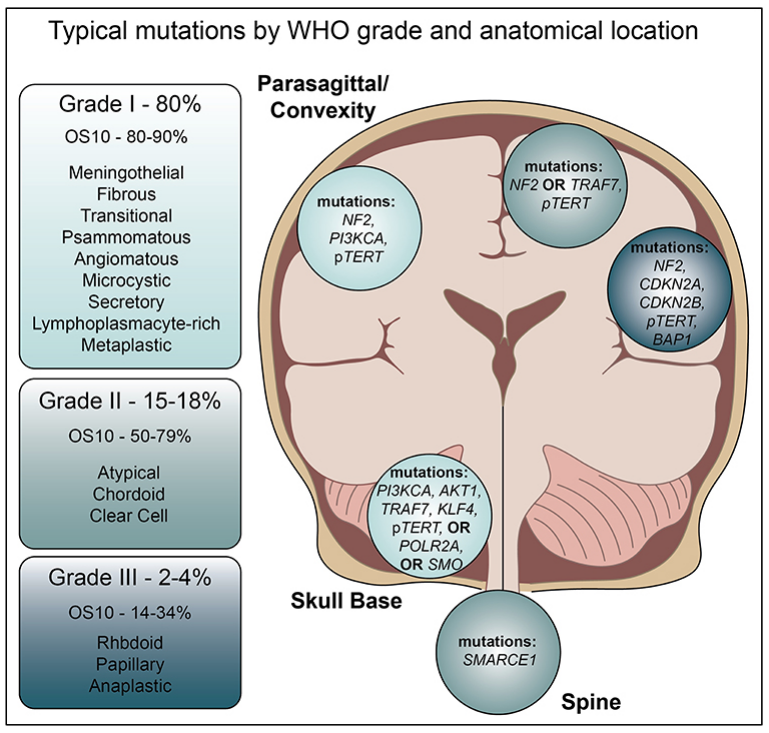
绝大多数脑膜瘤是良性的,80% 为 1 级,15-18% 为 2 级或非典型,2-4% 为3 级或恶性(图1)。脑膜瘤患者的预后与肿瘤分级相关。在非恶性脑膜瘤中,总体 5 年生存率为 88.2%,10 年生存率为 83.7%,而恶性脑膜瘤的 5 年生存率为 67.5% 。
图1、来源:Front oncol 2019;9
基因检测指导脑膜瘤预后分级和治疗
虽然影像学技术的进步未来可能会带来更有效的诊断,但目前诊断的金标准仍然是组织分析。组织学上,脑膜瘤通常做H&E 染色,其特征表现为核内假包涵体、假合胞体生长及漩涡状和砂粒体。此外,生长抑素受体2a (SSTR2a)的免疫组化(IHC)染色阳性可支持脑膜瘤的诊断。
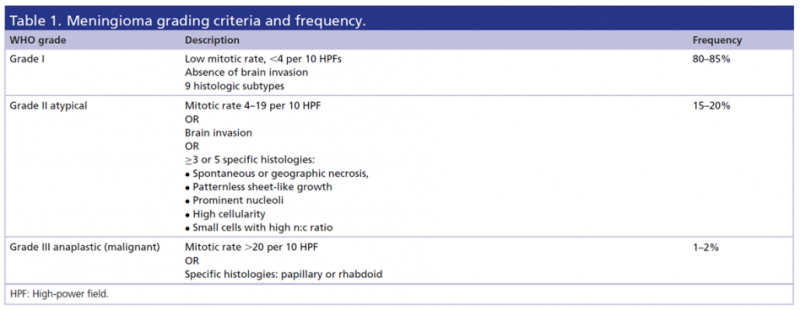
世界卫生组织 (WHO) 中枢神经系统肿瘤分类将脑膜瘤分为 15 种亚型。此后,2016 年的更新增加了核分裂象 ≥ 4 个/10 HPF 或具有的5个特征中的3个:呈灶性地图样坏死,肿瘤细胞失去原有排列或呈片状生长,核仁明显,细胞数量增多以及细胞核质比高,可作为非典型脑膜瘤,2级的诊断(图2)。
图2
然而,分级的可重复性仍然是一个挑战,一项研究报告称,参与多中心试验的不同观察者之间脑膜瘤分级的一致性仅为 87.2%。2021 年 WHO 分类澄清了历史上使用的几个诊断标准。以往,脉络膜和透明细胞脑膜瘤亚型被归类为 2 级,而横纹肌样和乳头状亚型被归类为 3 级。然而,文中指出,尽管具有这些组织学外观的脑膜瘤在很大程度上属于这些等级,但仅凭外观不应决定分级。
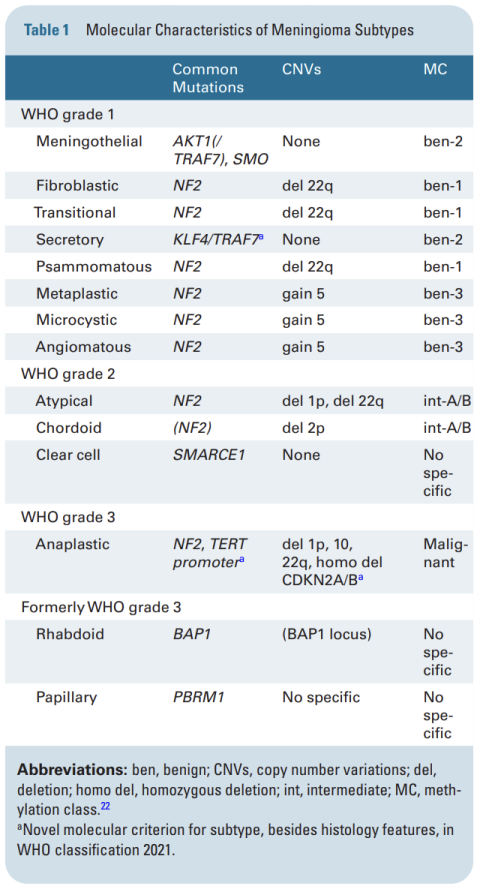
图3
而2021 年的WHO更新中还报告脑膜瘤中常见的基因变异,如SMARCE1(透明细胞亚型)、BAP1(横纹肌样和乳头状亚型)和 KLF4/TRAF7(分泌亚型)突变,并将 CDKN2A/B 纯合缺失和 TERT 启动子突变用作脑膜瘤3 级诊断,即使在没有间变性组织病理学特征的情况下,CNS WHO 3 级也可被诊断出来。
虽然这些基因的变异被认为是阴性预后标志物,但它们仅发生在少数脑膜瘤中,并且无助于识别中度风险脑膜瘤。除了 WHO 分级之外,关于脑膜瘤分级的最新研究还包括Neuro-oncology(IF=12.3)期刊发表的成果,整合染色体拷贝数变异、核分裂象以及基因变异综合评估肿瘤分级。
脑膜瘤分级反映了越来越多的临床证据支持要了解脑膜瘤的遗传和分子谱。将分子特征纳入脑膜瘤分类不但可提高预后风险评估的准确性,并可能提供新的精准治疗途径,在 2021 年 WHO 分类中列出的分子生物标志物对研究脑膜瘤新治疗方案的临床试验的设计和解释具有重要意义。
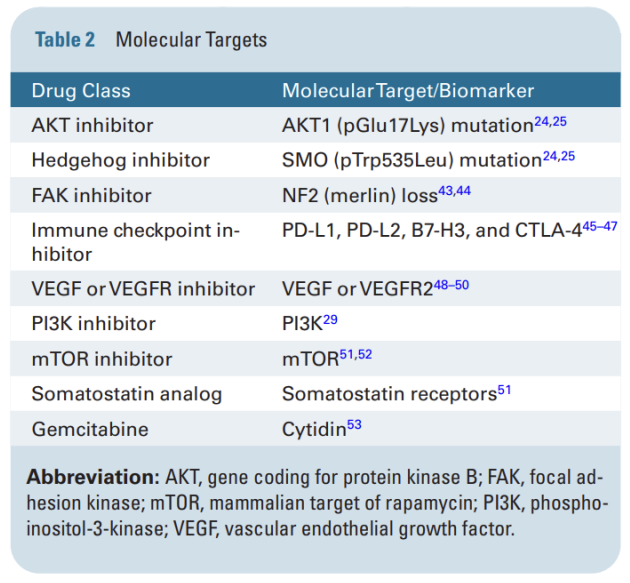
脑膜瘤的治疗包括观察、手术切除、放疗和少数化疗组合方案,对于手术或放疗不再有反应的复发性或进展性脑膜瘤患者可接受全身治疗,EANO欧洲神经肿瘤学会脑膜瘤诊治指南提到未来药物治疗主要基于潜在治疗靶点的鉴别(图4),例如有研究报道CDK4/6 抑制剂可能为CDKN2A/B纯合缺失高级别脑膜瘤的潜在治疗选择。
国家综合癌症网络 (NCCN)指南建议使用 α-IFN、生长抑素受体激动剂和血管内皮生长因子 (VEGF) 抑制剂治疗脑膜瘤 ,但是疗效目前有限。
图4
基因检测指导遗传风险评估
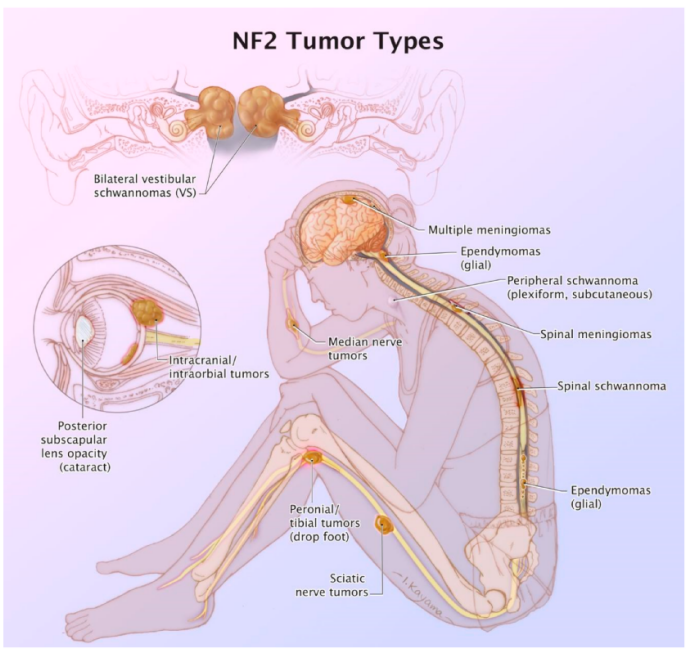
虽然大多数脑膜瘤是散发的,但一部分病例与遗传性癌症易感综合征有关。癌症易感综合征主要是由肿瘤抑癌和原癌基因的致病胚系变异引起的,2 型神经纤维瘤病 (NF2) 是这些遗传综合征中最为常见的,NF2 是由染色体 22q12 上 NF2 基因的胚系突变引起的,为一种常染色体显性遗传疾病,可导致双侧前庭神经鞘瘤(100%)、脑膜瘤 (50%) 和脊髓室管膜瘤 (<50%)。
图5、来源:Int. J. Mol. Sci. 2021, 22(2), 690
超过 50% 的 NF2 患者在其一生中至少会发生一个颅内脑膜瘤 。NF2 脑膜瘤发生年龄早(平均为30 岁),通常是多灶性的,这种多发性脑膜瘤或早发性脑膜瘤的存在应引起对 NF2的怀疑,因为这可能是第一个表现体征。与散发性脑膜瘤相比,NF2脑膜瘤通常为 II 级或 III 级,预后更差,复发率更高。
NF2 脑膜瘤的相关风险与基因突变的类型和位置相对应,截短突变的风险高于非截短突变,并且发生在基因 5' 端的突变比基因的 3' 端发生的风险更大。鉴于 NF2 突变与脑膜瘤之间存在密切且普遍的关联,一些学者建议在 30 岁以下或患有多个中枢神经系统肿瘤的患者在脑膜瘤切除术之前进行胚系 NF2 筛查。
脑膜瘤的治疗选择有限,当无法进行完全手术切除时,根据具体情况使用放疗,NF2 脑膜瘤应谨慎使用放疗。拉帕替尼、依维莫司、依维莫司 + 奥曲肽和贝伐单抗 + 依维莫司的组合在减缓肿瘤生长方面显示出益处。
例如《Clin Cancer Res》在2020年发表的一项研究:20 名复发性脑膜瘤患者接受了 10 毫克/天的依维莫司和奥曲肽的联合治疗,包括WHOⅠ级肿瘤2例,WHOⅡ级肿瘤10例,WHOⅢ级肿瘤8例,其中4名患者携带NF2胚系突变。在 3 个月时,78% 的肿瘤的生长速率显著下降 > 50%,总体PFS-6 为 55% ,总体 6 个月和 12 个月生存率分别为 90% 和 75% 。
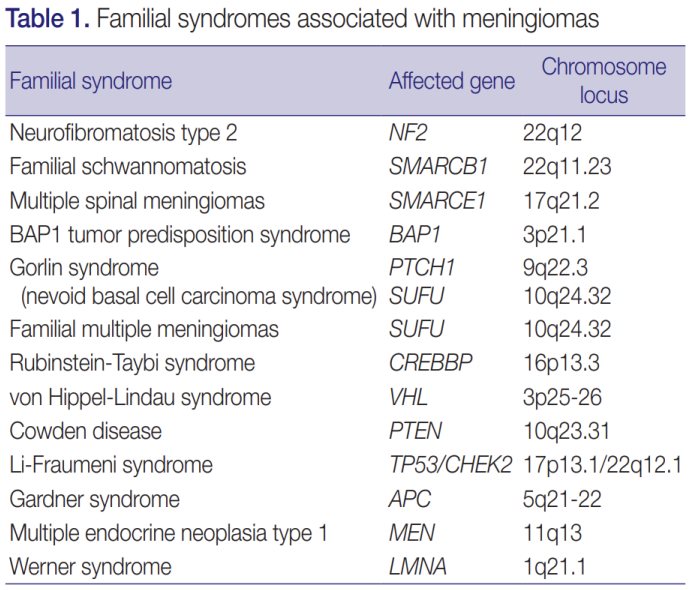
除了2 型神经纤维瘤病 (NF2),另外还有1 型多发性内分泌肿瘤综合征 (MEN)、von Hippel-Lindau (VHL)、Li-Fraumeni 综合征、Gorlin 综合征、Cowden综合征、痣样基底细胞癌综合征、BAP1 肿瘤易感综合征、Rubinstein-Taybi 综合征和家族性脑膜瘤病等也可引起脑膜瘤的发病风险增加。(图6)
图6
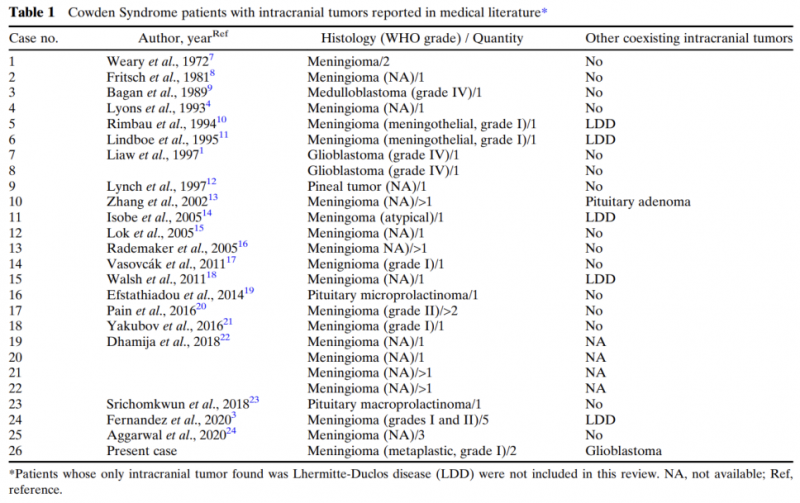
Cowden综合征(CS)是一种罕见的常染色体显性遗传病,其特征是多发的错构瘤(发育中出现错误而形成的肿瘤),与PTEN基因的胚系突变有关。CS 与颅内肿瘤的关系较为熟知的是小脑发育不良性神经节细胞瘤(Lhermitte-Duclos病,LDD) ,除此之外,也有其他CS患者颅内肿瘤的文献报道,主要为脑膜瘤,其次为垂体瘤和胶质母细胞瘤(图7)。
图7
以往有数据报道CS 患者脑膜瘤的发生率在 3.6% 和 18.2% 之间。Yakubov等人发表的荟萃分析,涉及 109 名确诊 PTEN 基因突变的 CS 患者表明脑肿瘤的总体发生率高达 20.18%,仅次于乳腺癌(37.6%)。
2022年有学者首次报道了一名伴有脑膜瘤和胶质母细胞瘤的Cowden 综合征患者,这是一名携带 PTEN 基因胚系突变 c.334C > G 的 62 岁男性诊断患有多发性脑肿瘤,并被误认为这些肿瘤是转移灶。由于未发现原发癌,因此进行诊断性手术,从切除的两个病变中获得的手术标本,一个在轴外的,另一个在脑内,分别证实为具有脂肪瘤外观的化生型脑膜瘤和IDH野生型胶质母细胞瘤。
这两种病变均经免疫组化证实PTEN基因表达缺失,这一发现支持其与 CS 的关系。基于以往的文献证明了 CS 与原发性脑肿瘤,特别是脑膜瘤的关联。研究者建议应认真考虑将颅内肿瘤纳入 CS 患者的癌症筛查。
总之,尽早的遗传咨询是必要的,详细的临床病史和检查可提高目标患者的筛选,并通过合适的基因检测进一步证实。了解这些肿瘤综合征将有助于对有家族史的患者进行管理,并为阐明脑膜瘤的肿瘤发生机制奠定基础。
参考文献:
[1] EANO guideline on the diagnosis and management of meningiomas.Neuro oncol 2021 11 02;23(11)
[2] Nervous system (NS) Tumors in Cancer Predisposition Syndromes.Neurotherapeutics 2022 Sep 02
[3] Wallace G E , Tjoelker M , Bartley K , et al. Precision Therapy for Brain Tumors in Hereditary Syndromes[J]. Current Treatment Options in Oncology, 2021, 22(9).
[4] Bachir S , Shah S , Shapiro S , et al. Neurofibromatosis Type 2 (NF2) and the Implications for Vestibular Schwannoma and Meningioma Pathogenesis[J]. International Journal of Molecular Sciences, 2021(2).
[5] Prieto R, Hofecker V, Corbacho C,Coexisting lipomatous meningioma and glioblastoma in Cowden syndrome: A unique tumor association.Neuropathology 2022 Aug 24
内容来源:绘真医讯