哪些非小细胞肺癌患者需要重点做ALK基因检测,确诊ALK阳性后首先用的ALK阳性靶向药是什么,耐药或脑转移ALK阳性用什么药
根据美国SEER数据库2022年公布的数据,55%的肺及支气管癌患者,确诊时已经发生了远处转移,也就是病理分期为Ⅳ期。而这部分患者当中能够生存5年的比例,仅为7%。
许多其它统计数据,包括来自中国的统计数据也表明,转移性非小细胞肺癌患者生存期超过5年的比例只有不到10%。也就是说,在现有的、比较普及的方案治疗之下,10位非小细胞肺患者,最终很可能只有1位能活到5年以后!
但从趋势上来看,肺癌又是形势比较乐观的癌症之一。从2000年以来的近20年里,这类癌症的死亡率有了小幅度的下降(2000~2016年间下降了0.6%)。而且在这些年里,肺癌的治疗方案、尤其是非小细胞肺癌的靶向治疗方案,已经经历了从无到有、以及从有到丰富的两次巨大进步。
在这些非小细胞肺癌的靶向治疗方案当中,有那么极少的几个靶点被誉为“钻石靶点”。这些靶点的药物疗效极好、患者有很大的机会获得很长的生存期。这一次,基因药物汇就来给大家讲一讲其中一个“钻石靶点”,ALK。
3年无进展,半数患者生存7年
2020年公布的阿来替尼的临床试验数据,这款药物用于一线治疗ALK阳性的晚期非小细胞肺癌,中位无进展生存期长达34.8个月,患者的5年生存率也达到了惊人的62.5%。
此前也有报道显示,ALK阳性非小细胞肺癌患者接受靶向治疗的中位总生存期可以达到4.3年;部分试验当中采用“1 3”序贯治疗方案时,患者的中位总生存期能够达到7年以上。
7年是什么概念?Ⅳ期非小细胞肺癌的5年生存率也才不到10%,也就是说,在现有的治疗水平下,只有大约10%的患者能够活过5年。
当然,在现实条件下,并非所有患者都有机会并且得到了最好的治疗。因此我们完全可以说,如何最大程度地筛选出ALK阳性的患者,是临床靶向治疗更大获益的重要前提。
那么,哪些患者应当重视ALK的检测?确认为ALK阳性之后,首先应该选择哪款药物治疗?如果发生耐药,应该如何选择后续的治疗方案?如果出现脑转移,用哪款药物的疗效更好呢?
Q1、哪些患者需要重点检测ALK?如何检测?
首先,肺腺癌以及包含腺癌成分的非小细胞肺癌患者都应当检测ALK。但这个问题的核心其实在于,如肺鳞癌等ALK检出率低的分型,是否还要将ALK纳入必检项目?
一般来说,单纯的肺鳞癌(非混合型)出现ALK基因融合的概率非常低。但是由于肺癌的高度异质性(简单来说就是每个患者的每个癌细胞都可能有完全不一样的特质,异质性可能表现在代谢、免疫原性、迁移特点等等方面),有些研究认为肺鳞癌当中没有ALK阳性,有些研究发现1400例肺鳞癌当中ALK基因融合阳性的发生率为1.3%,甚至也有的研究认为发生高于非小细胞肺癌的整体发生率5%。
是0还是1.3%还是5%只有测了才知道,所以部分指南会推荐不吸烟的、仅可提供小活检标本的肺鳞癌患者也进行ALK检测。
从另一方面来说,非小细胞肺癌的各类驱动基因突变都是高度排他的,这就意味着,在其它驱动基因突变(例如EGFR和KRAS)均为阴性的患者当中,ALK阳性的比例会很高(高达30%~42%)。因此,国际肺癌研究协会(IASLC)的ATLAS指南认为,EGFR阴性的患者,不论病理类型,都应该检测ALK,以免因为检测不全面而让患者错失治疗良机。
至于ALK的检测方式,主要为免疫组织化学(IHC)、荧光原位杂交(FISH)以及反转录聚合酶链反应法(RT-PCR)。检测技术发展之后的现在,患者也可以选择二代测序(NGS),结果最准确,也能提前检测出一些预后不良的融合类型,同时检测多个靶点时消耗的组织样本更少,但需要注意避免漏掉一些未知的、有价值的亚型。
关于二代测序我们在这里就不占篇幅细讲了,如果大家希望了解更多,可以阅读《他们给五万名癌症患者做了两次基因检测,结果令人震惊……》这篇专门讲基因检测的文章。如果有一些问题想尽快得到答案,也可以联系基因药物汇医学部。
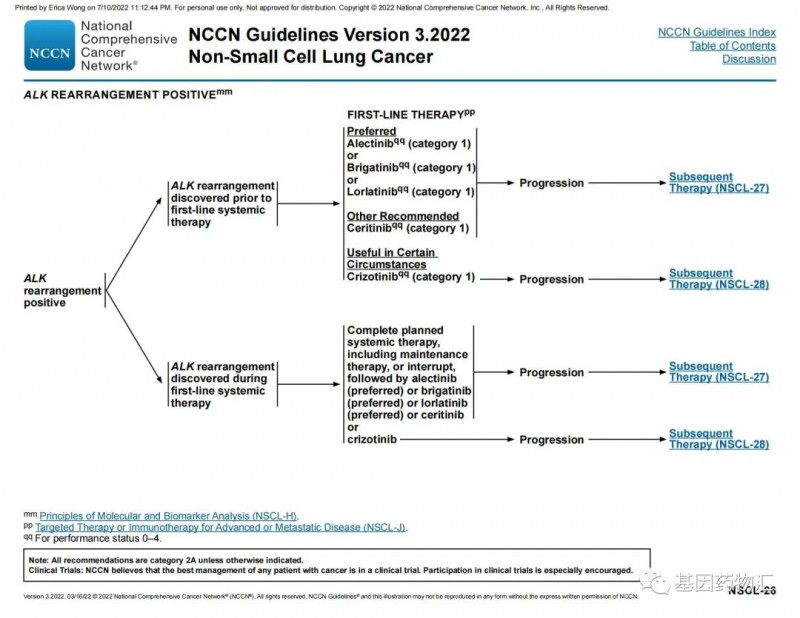
Q2、存在ALK重排,首先选择哪款治疗药物?
不论是在一线化疗前发现ALK阳性,还是在一线化疗期间发现ALK阳性,都首选第二代ALK抑制剂(阿来替尼、布加替尼)或第三代ALK抑制剂(劳拉替尼)。
另一款第二代ALK抑制剂色瑞替尼也可以作为备选,除此以外,部分特殊情况下也可以使用克唑替尼。
一线治疗就是荷瘤状态下接受的首次治疗方案。只有对于某种疾病最有效、最敏感的药物才能够成为一线治疗的首选方案。
不过呢,一线治疗也分两种情况。
如果患者能接受手术,并且确实完成了手术,那么手术之后规范的辅助化疗并不算做一线治疗。只有在肿瘤复发、患者再次接受系统治疗的时候,才算是一线治疗。
如果患者确诊时就已经没有了手术的机会,那么在这个荷瘤的状态下接受的首次治疗,就算是一线治疗了。
Q3、一线治疗后进展,该更换什么方案?
如果只是影像学进展,但患者没有出现任何的症状表现,可以考虑使用根治性的局部治疗,例如立体定向消融放疗(SABR)或者手术,并且在处理局部病灶的同时,继续使用原本的治疗方案,包括阿来替尼、布加替尼、色瑞替尼或劳拉替尼等。
如果患者已经出现了症状表现,对于脑部进展的患者来说,首先考虑局部治疗,例如立体定向放射治疗(SRS),并且在处理局部病灶的同时,继续使用原本的治疗方案,包括阿来替尼、布加替尼、色瑞替尼或劳拉替尼等。
如果患者已经出现了症状表现,转移病灶出现在脑以外的其它部位,且为寡转移(转移病灶数量较少,且局限在某个器官内),那么推荐的治疗方案仍然为局部治疗+原全身治疗方案。
如果患者已经发展为全身多部位多发转移,那么优先选择劳拉替尼方案(对于既往未接受过相同方案的患者)。
如果患者接受的一线治疗为克唑替尼,那么后续的治疗很相似,只是在前面几种方案当中“维持原治疗方案”的时候,一线接受克唑替尼治疗的患者都可以考虑换用第二代ALK抑制剂(阿来替尼、布加替尼、色瑞替尼)或第三代ALK抑制剂(劳拉替尼)。
Q4、如果出现脑转移,哪种方案效果最好?
首先,对于脑转移患者来说,继续用克唑替尼肯定是不行的。
此前的报道中称,接受克唑替尼治疗的ALK阳性患者,46%~72%首先发生颅内进展,且其中80%的案例,脑是唯一的进展部位。这说明,任何正在接受克唑替尼治疗的患者,都应当警惕脑转移的风险。
在辉瑞公布的试验结果回顾性分析当中,克唑替尼用于基线存在脑转移的患者的颅内病灶缓解率,仅为18%,远远低于其他部位转移的患者;脑转移患者对于药物的响应时间也明显缩短,仅仅只有其它患者的一半。
种种研究的数据、以及诸多案例都表明,克唑替尼在脑转移治疗当中,有些“乏力”。
案例1
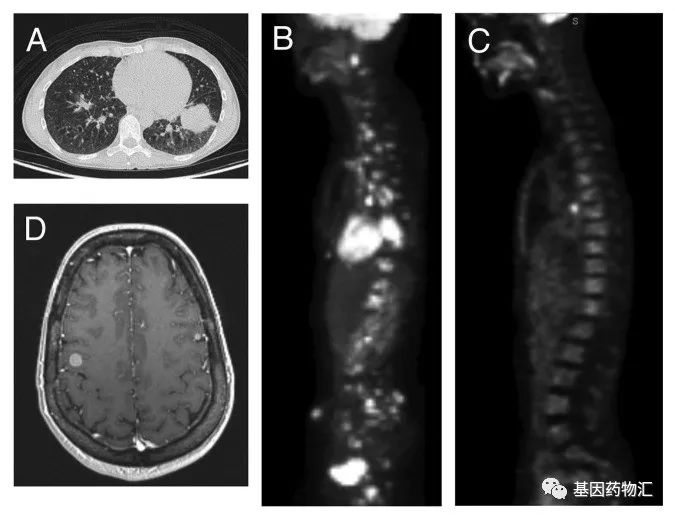
第一个案例当中的患者,属于中分化腺癌,ALK突变,原发于肺左下叶。确诊时病灶所在部位除双肺外,还包括了骨骼和纵隔。
大家都注意到了,这位患者初治时并不存在脑转移,后续接受了克唑替尼单药治疗。6个月复查时,患者达到了临床部分缓解,骨骼与肺部的病灶都得到了不错的控制,但问题是,患者此时的脑核磁共振(MRI)检查显示,颅内出现了整整12个新发的转移病灶。
图B是治疗前的影像,图C是治疗后的影像。很显然,除了对颅内效果不佳以外,克唑替尼治疗患者全身的病灶的疗效都是相当不错的。
案例2
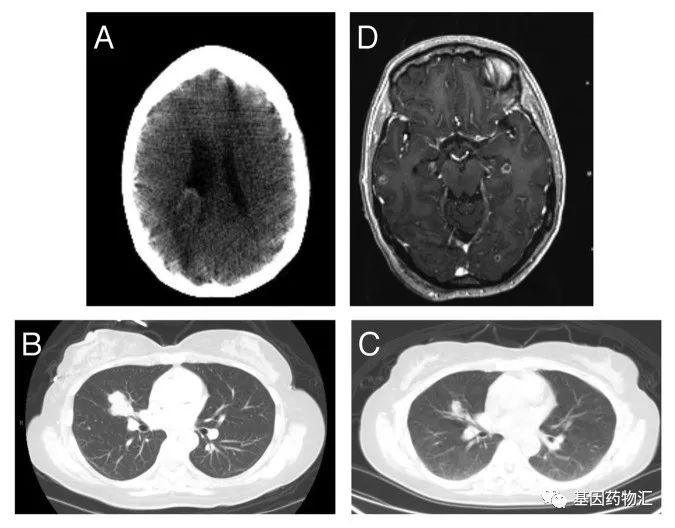
第二个案例当中患者51岁,同样属于中分化腺癌,ALK突变,原发于肺右中叶。确诊时病灶所在部位包括了脑,还有骨骼和纵隔。
这次患者接受了全脑放疗,随后接受了克唑替尼单药治疗。同样的,克唑替尼对于患者颅脑以外的病灶疗效都非常的不错,但脑内病灶还是没控制住,又进展了,新发病灶数量非常多。
图A是患者治疗前的头部影像,有3个比较大的病灶;图D是克唑替尼治疗8个月后的影像,医生指出病灶都是新发的。
这两个病例有一个非常明显的共同点:患者接受克唑替尼治疗,除了颅脑病灶以外的其它靶病灶控制都相当不错。但不论是初始存在脑转移的患者还是不存在脑转移的患者,最终癌细胞都会逐渐地向颅脑侵袭——这是一个克唑替尼“够不到”的地方,是这种方案的“致命弱点”,于是癌细胞非常“狡猾”地躲向了这里。
不过好在,不论是第二代ALK抑制剂(阿来替尼、布加替尼、色瑞替尼),还是第三代ALK抑制剂(劳拉替尼),在脑转移的治疗上效果都比较明显,都可以作为选择。其中劳拉替尼治疗脑转移的缓解率高达82%,71%的患者脑转移病灶能够完全消失。
Q5、ALK阳性患者,需要考虑临床试验吗?
如果阅读得比较仔细,大家或许会发现指南下方备注当中的这句话:
NCCN认为,对于任何癌症患者来说,最佳的治疗策略都是临床试验。NCCN非常鼓励患者参与到临床试验当中。
这是一个非常高规格的认可:NCCN认为,任何癌症患者都可能甚至是可以从临床试验当中获得最佳的治疗!
如果符合适应症,那么ALK阳性的非小细胞肺癌患者当然要考虑临床试验。大家可以将患者病例发送至基因药物汇,寻找合适的临床试验项目,或咨询医学部获取帮助。