胃癌细胞免疫治疗,国产CART疗法CT041治疗胃癌疾病控制率高达73%
随着阿基仑赛注射液、瑞基奥仑赛注射液前后在中国获批上市,西达基奥仑赛被美国FDA获批上市,癌症治疗领域火速掀起一阵“CAR-T热”,中国在2021年正式迎来细胞免疫治疗元年,并在2022年有望迎来井喷期!
这一蜕变或许有望将“抗癌”变为“治癌”,迎来反击癌症的新时代。比起“治标不治本”经常会复发的传统疗法,调用患者体内自身免疫系统的CAR-T可以说是目前最先进的治疗手段。
这项技术近年来在治疗各种恶性肿瘤方面取得了巨大进展,已成功应用于多种血液恶性肿瘤的治疗。但是,全球约90%的癌症病例是实体肿瘤,CAR-T疗法在肝癌、胃癌、胰腺癌等消化系统肿瘤中虽然也取得了一定的疗效,但是少之又少,这主要是碍于靶点选择困难、CAR-T细胞进入肿瘤组织困难、CAR-T细胞进入肿瘤组织后容易被其他免疫抑制性的分子或细胞所阻挡无法发挥作用等。
因此,国内外的学者针对CAR-T进行了多种改造,不断地发现新靶点,以用于治疗多种实体肿瘤。
基于此,中国研究人员开发了国际上首个针对 Claudin18.2的CAR-T细胞产品CT041。就在2022年5月9日,科济药业CAR-T细胞产品CT041治疗消化系统肿瘤的研究结果发表在国际顶级期刊《Nature Medicine》杂志上,这也算是首个发表于顶级学术期刊的迄今为止最大样本量的CAR-T细胞治疗实体瘤的临床研究!
疾病控制率达73%!国产实体瘤CAR-T疗法CT041闪耀国际舞台!
作为国际上首个针对Claudin18.2的CAR-T细胞,CT041早在2019年ASCO年会上就崭露头角,当时总客观缓解率为33.3%就已经惊艳世界,如今更加显著的疗效无疑是锦上添花!此次的临床数据展现出对消化系统肿瘤的良好治疗前景!
2021年欧洲肿瘤内科学会(ESMO)年会上,由科济药业开发的靶向Claudin18.2(CLDN18.2)自体CAR-T候选产品CT041展现了其在消化系统肿瘤中的突出疗效,可谓是大放异彩!
而此次在国际顶级期刊上公布的为中国开展、多中心、开放标签的I期临床试验数据,截止到2021年4月8日,纳入的37例CLDN18.2表达阳性的晚期消化道肿瘤患者接受CT041输注并完成至少12周的评估。
其中包括28例胃癌/胃食管结合部癌、5例胰腺癌和4例其他消化系统肿瘤,28例患者细胞输注剂量为2.5×108CAR-T细胞,6例患者输注3.75×108,3例患者输注5×108 CAR-T细胞。约84%的患者既往接受过至少2线治疗,中位转移器官数量为3个。
01、总疗效:客观缓解率达48.6%,疾病控制率达73%
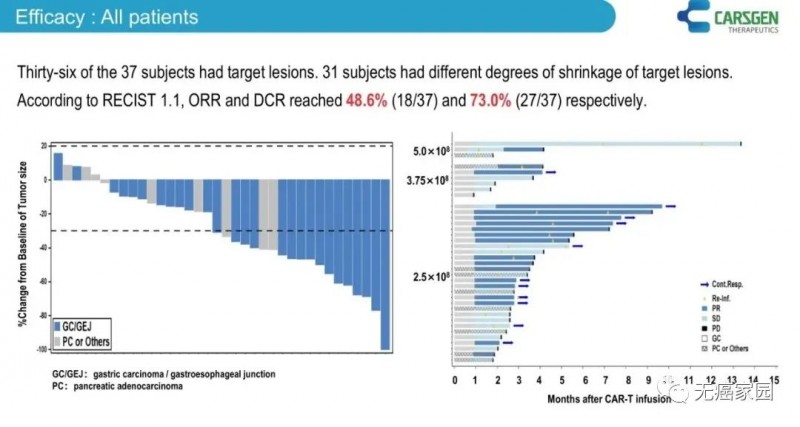
在疗效方面,36例具有肿瘤靶病灶的患者中,31例患者观察到不同程度的目标病灶缩小,总客观缓解率(ORR)为48.6%,疾病控制率(DCR)为73.0%。所有胃癌患者总客观缓解率为57.1%,疾病控制率达75.0%。
图1 全部患者的疗效
02、既往接受至少2线治疗失败的胃癌患者:ORR为61.1%,DCR为83.3%
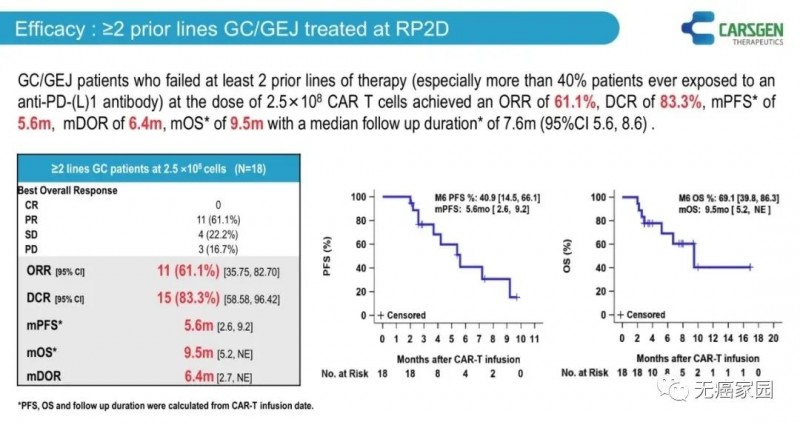
在既往接受至少2线治疗失败、接受II期推荐剂量(RP2D) 2.5×108 CAR-T细胞治疗的18例胃癌/胃食管结合部癌患者中,8例(44%)患者既往接受过抗PD-(L)1单抗治疗。
中位随访时间为输注后7.6个月,客观缓解率为61.1%,疾病控制率为83.3%,中位无进展生存期和中位总生存期分别为5.6个月和9.5个月。
图2 胃癌/胃食管结合部癌≥2线治疗患者的疗效
03、28例胃癌/胃食管结合部癌:各亚组ORR均维持在50%或以上
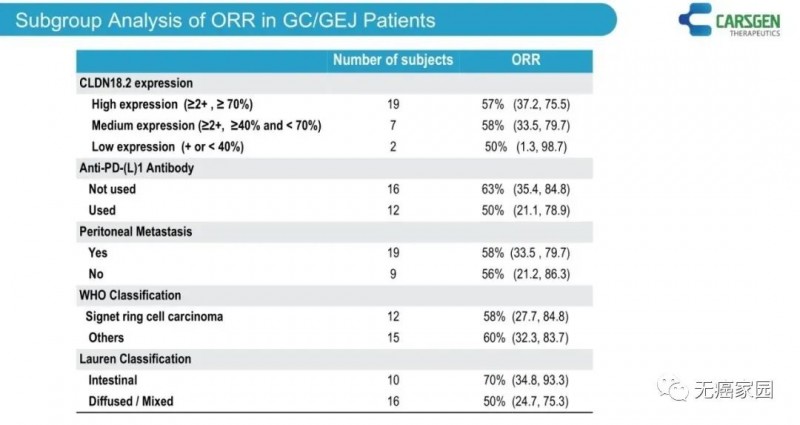
在28例胃癌/胃食管结合部癌患者中,不同基线特征的亚组分析显示,在既往PD-(L)1抑制剂治疗失败、存在腹膜转移、印戒细胞癌等预后差且已无有效治疗手段的患者中,ORR均可维持在50%或以上。
图3 胃癌/胃食管结合部癌患者各亚组的疗效
04、总体耐受性良好,安全性较好
从具体临床数据来看,CT041总体耐受性良好,未发生治疗相关死亡或免疫细胞治疗相关神经系统毒性综合征(ICANS)。约95%的患者发生细胞因子释放综合征(CRS),均为1级或2级。
1例因为肿瘤快速缩小而导致胃肠出血,6例患者报告胃黏膜损伤(只有1例达到3级),经对症治疗后均已恢复。所有患者均发生3/4级血液学不良事件,通常是由于清淋预处理治疗所致,在2周内恢复。3个剂量水平之间的安全性特征无显著差异。
无癌家园专家点评
需要强调的是,入组的患者均为标准治疗失败后,大多数曾接受过PD-(L)1免疫治疗药物的难治、预后较差的患者。
28例胃癌/胃食管结合部癌患者中,Lauren分型弥漫型或混合型者有16例,67.9%的患者伴腹膜转移,42.9%既往接受过抗PD-1/PD-L1单抗药物治疗,35.7%既往接受过TKI药物治疗。
除了CT041目前正在开展临床试验外,另外一款针对既往接受过胃全切除术/胃大部切除术后的复发或转移性晚期胃腺癌(包括胃食管结合部腺癌)的靶向Claudin18.2 的CAR-T细胞制剂,名为LCAR-C18S也在临床招募中。
目前急招B细胞淋巴瘤、T细胞淋巴瘤、T细胞白血病(T-ALL)、急性白血病、非霍奇金淋巴瘤、肝癌、胃癌、前列腺癌、甲状腺癌等癌种!
想要评估病情是否能够接受CAR-T疗法可将病理报告、治疗经历及出院小结等提交至无癌家园医学部进行初步评估!
CT041典型病例及取得成就一览
典型病例
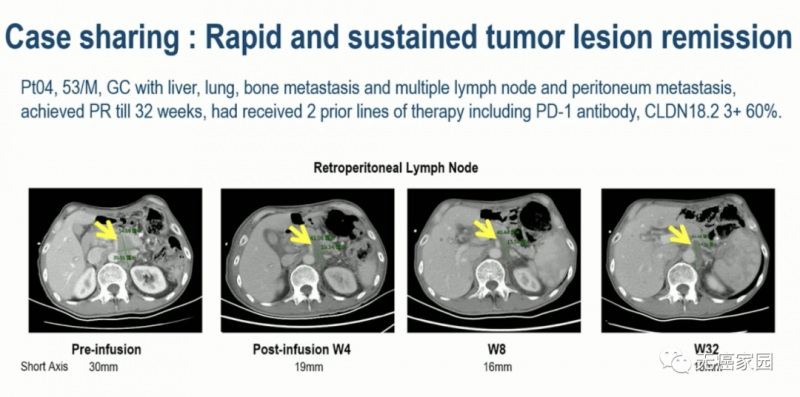
01、04号患者 53岁 男性
来源 CARsgen Therapeutics
晚期胃癌伴肝、肺、骨转移和多发淋巴结和腹膜转移,已接受包括 PD-1 抗体在内的2种全身治疗,CLDN18.2 60%(3+),接受CAR-T治疗后,肿瘤缩小近50%,持续缓解32周。
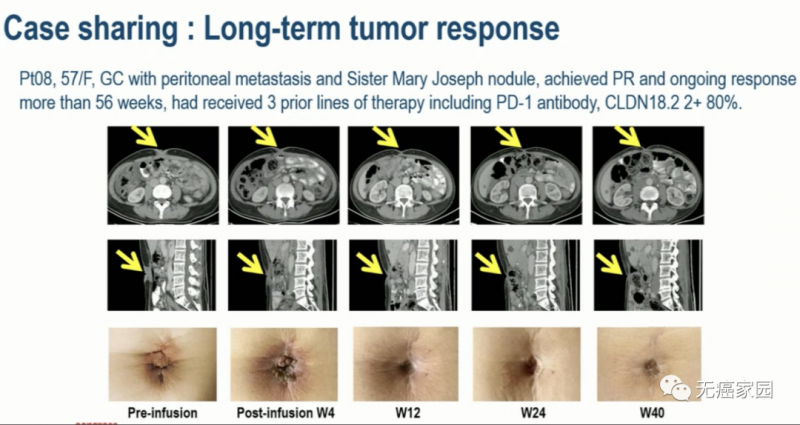
02、08号患者 57岁 女性
来源 CARsgen Therapeutics
GC 有腹膜转移和玛丽约瑟夫结节(恶性肿瘤转移到脐部形成的结节样病变),之前接受过3线疗包括PD-1抗体,CLDN18.2 80%(2+),接受CAR-T治疗后达到部分缓解,并且持续反应超过56周。
CT041取得成就一览
2020年5月,FDA批准了CT041用于治疗claudin18.2阳性的胃、胃食管连接处或胰腺腺癌患者的研究新药(IND)许可;2020年,美国FDA授予其孤儿药认定,用于治疗胃癌/胃食管结合部癌;2021年,CT041先后获得欧洲药品管理局(EMA)的孤儿药认定、欧洲“优先药物”(PRIME)资格;2022年,CT041获美国FDA授予“再生医学先进疗法”(RMAT)资格。2022年3月3日,CT041获中国国家药品监督管理局(NMPA)药品审评中心(CDE)同意进入确证性Ⅱ期临床试验!
内卷升级!国产多款Claudin18.2药物获批临床,群雄逐鹿
Claudin18.2(CLDN18.2)是Claudin蛋白质家族的一员,位于细胞膜表面,正常情况下仅低水平表达于胃粘膜分化上皮细胞,但在病理状态下,Claudin18.2在多种肿瘤中有的表达显著上调,包括80%的胃肠道腺瘤、60%的胰腺肿瘤。此外,CLDN 18.2活化还可见于食管癌、卵巢癌和肺腺癌中,因此是具有潜力治疗癌症的热门靶点。
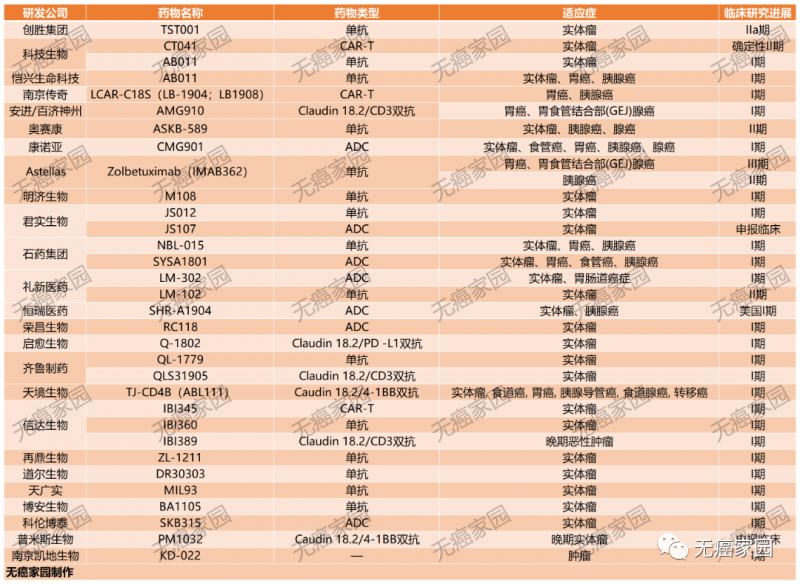
据无癌家园小编查阅ClinicalTrials及CDE(国家药监局)发现,目前批准临床的Claudin18.2产品就多达几十款,多数药物均是拟用于治疗晚期胃癌、胰腺癌及实体瘤患者。
因该靶点在正常组织中的高度特异性表达,再加上在多种癌症中的激活表达,使得Claudin18.2蛋白成为了研究人员开发胃癌、胰腺癌等实体瘤免疫疗法的理想靶点。同时,由于胃癌是国内的一大瘤种,Claudin 18.2靶点有望实现胃癌新靶点药物的瓶颈突破。
目前除了CT041在招募外,我国自主研发的首个针对Claudin18.2的单抗AB011(针对胃癌、胰腺癌)、CAR-T细胞疗法LCAR-C18S(针对胃癌),靶向Claudin18.2的抗体偶联药物(ADC)LM-302(针对实体瘤)也正在火热招募中,若有意向参加临床试验,可提交病理报告、治疗经历及出院小结至无癌家园医学部,详细评估病情。
国内药企超20多家布局CAR-T细胞疗法,中国或可弯道超车
随着阿基仑赛注射液、瑞基奥仑赛注射液在国内获批上市,CAR-T细胞疗法越来越火,让大家看到治愈肿瘤的希望,因此细胞免疫将逐步解决临床上未满足的重大需求。
据Frost&Sullivan报告显示,中国细胞免疫治疗产品市场规模2021年仅为13亿元,预计2年后涨至102亿元。
根据丁香园Insight数据库统计,国内共有24家企业布局CAR-T疗法,除复星凯特和药明巨诺外,还有传奇生物、科济生物、驯鹿医疗、西比曼生物、信达生物等。
截至目前,国内开展的CAR-T临床试验数量已经超过500项,居世界第一,这也是中国首次在一个新药研发领域走到国际前列。其中,传奇生物的西达基奥仑赛、科济药业的Claudin18.2 CAR-T都达到全球领先水平。此外,还有多公司在布局新一代CAR-T以及异体CAR-T技术,初步数据优异,有望获得全球市场。
2021年我国迎来了细胞免疫治疗的元年,作为先锋的CAR-T疗法,是未来发展方向之一。CAR-T疗法主要在于改造T细胞来使其识别肿瘤细胞的特殊靶点,理论上,可以有无数种针对不同靶点的CAR-T疗法,这意味着蕴含着无限可能。
希望不久的将来,能够在国内外医学科研工作者的努力下,降低细胞疗法毒副作用,降低价格,突破实体瘤的瓶颈,让越来越多的晚期癌症患者获益!
参考文献:https://www.nature.com/articles/s41591-022-01800-8