双抗药物有哪些,两个靶点的抗癌药物,疗效一定比单个靶点的更好吗
“双抗”,也就是双靶点抑制剂,是一个在近两年才在癌症患者当中普及并流行起来的概念。
常规的靶向或免疫治疗药物只能用于抑制某一个或一类靶点,因而诞生了一些独特的联合用药方案;而“双抗”最大的特点在于,这类药物能够同时抑制两个或两类靶点,以一药之“力”,就能够达到两药联合治疗的效果。
这样的特点,为“双抗”带来了许多超越常规靶向及免疫治疗药物的独特优势,包括但不限于更广的适应症、更高的缓解率、以及更少的不良反应等等。
仅仅从理论上来分析,显然说服力有些不足。那么,这一次我们就从数据上为大家详细剖析一下,两个靶点的抗癌药物,疗效一定比单个靶点的更好吗?
靶向"双抗":攻坚克难,先解难治、再破耐药
靶向治疗是一种比化疗更加“精准”的癌症治疗方案,其发挥抗癌效果最主要的凭依,是针对性抑制某些与癌细胞生长增殖密切相关的重要蛋白质的能力。
那么什么时候会用得上“双抗”呢?很显然,当单靶点的抑制剂难以满足需求的时候,“双抗”就担负起了这样“攻坚克难”的重任。
01、EGFR/MET双抗:先解难治、再破耐药
解难治
JNJ-6372这款新药最初“闯入”患者的视线当中,依靠的是其对EGFR外显子20插入突变(ex20ins)这个突变类型患者的疗效。
EGFR ex20ins是一类非常难治的突变亚型,连奥希替尼都对这部分患者“束手无策”。但“双抗”JNJ-6372,对于这部分患者的疗效却相当不错。
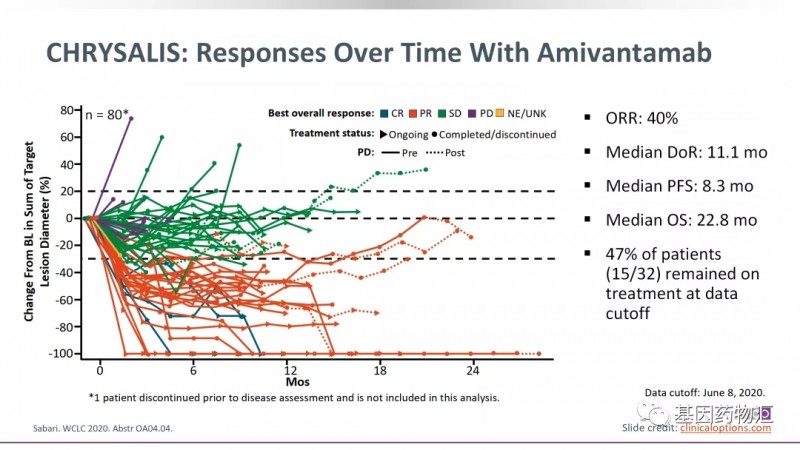
CHRYSAILS试验中,使用JNJ-6372治疗已经接受过铂类化疗且疾病进展的EGFR ex20ins突变非小细胞肺癌患者,整体缓解率为40%,中位治疗时间11.1个月,中位无进展生存期8.3个月,中位总生存期22.8个月。
这样的疗效对于ex20ins患者来说是具有颠覆性的。在一项筛选了62464例晚期非小细胞肺癌患者的统计研究中,ex20ins患者接受现有方案治疗,中位无进展生存期仅有2.86个月,中位总生存期仅有7.45个月,与其它EGFR突变亚型的10.45个月和25.49个月相比,甚至不到三分之一。
化疗耐药患者的治疗,听起来可能没有“冲击一线”来得那么有气势;如果单独看一项试验、没有其它统计结果作为支持的话,数据也很难做到颠覆性地“漂亮”。但事实上,这样用于耐药患者的适应症,更符合临床上大部分患者的需求。
在这款药物获批之前,临床上大部分患者会在明确知道EGFR抑制剂对于自己疗效不佳的情况下选择化疗,因此JNJ-6372在这项临床试验当中的后线治疗适应症反而更适合临床上数量更多的一部分患者。
破耐药
在另一部分CHRYSALIS试验当中,共有45例接受奥希替尼治疗后疾病进展的患者,接受了EGFR/MET“双抗”Amivantamab-vmjw(Rybrevant,JNJ-6372)与第三代EGFR抑制剂拉泽替尼(Lazertinib,Leclaza)联合方案的治疗。
这45例患者分别接受了1~4线前线方案治疗,其中所有患者都接受过第三代EGFR抑制剂(奥希替尼)的治疗,另外还有33例患者(73%)曾经接受过第一代或第二代EGFR抑制剂治疗。
从现有的、已经上市的方案的角度来说,这部分患者已经没有其它靶向治疗药物可以选择了。
但JNJ-6372与拉泽替尼的治疗方案,仍然使其中大部分的患者获益了!
1、整体缓解率:36%
2、中位缓解持续时间:9.6个月
3、临床获益率:64%
4、中位无进展生存期:4.9个月
换句话说,有36%的患者,在治疗的过程中靶病灶直径之和比治疗前减少了至少30%;且共有64%的患者,在治疗的过程中不仅没有新的病灶出现,也基本没有大的进展,病灶缩小,或者增大量少于20%。
“奥希替尼耐药”的什么突变型患者能够获益呢?毕竟JNJ-6372是一款EGFR/MET双靶点抑制剂,研究者同样也完成了这项分析。
在45例患者当中,17例患者存在基于EGFR或MET的各类耐药突变,28例患者存在其它类型的耐药突变,包括PIK3CA E545X/H1047R、CCND1/2扩增、KRAS A18V/G12C、PTEN I33del/N48K、SQSTM1-ALK融合突变等。
基于EGFR或MET的耐药突变患者,临床获益率是82%;其它耐药突变的患者,临床获益率也有54%。尽管有一定的差距,但很显然,即使是与EGFR或MET无关的耐药突变型患者,同样能够从这个联合方案当中获益!
不论“耐药”还是“难治”,这款创造性的双靶点抑制剂都突破了以往的记录,标志着这了,两类患者,终于进入了“有针对性药物可用”的全新时代。
目前JNJ-6372治疗第一、第二、第三代EGFR抑制剂耐药,以及治疗原发耐药相关突变(例如ex20ins)的非小细胞肺癌患者的中国中心临床试验正在招募患者,有需求的患者可以联系基因药物汇-临床新药招募中心了解招募详情,或将病历资料及联系方式发送至招募中心邮箱(doctorjona0404@gmail.com)进行申请。
免疫“"双抗":一药超越两药,更多患者获益
提到免疫治疗,大家肯定会想到纳武单抗联合伊匹木单抗的这对经典“O+Y”双免疫组合。这对组合、以及这两款药物对应的PD-1/PD-L1与CTLA-4这组靶点,又被称作免疫治疗当中的“黄金搭档”。
当然,除了这对“黄金搭档”以外,还有很多已经被证实有效果或者有潜力的免疫靶点组合。
01、PD-L1/TGF-β双抗
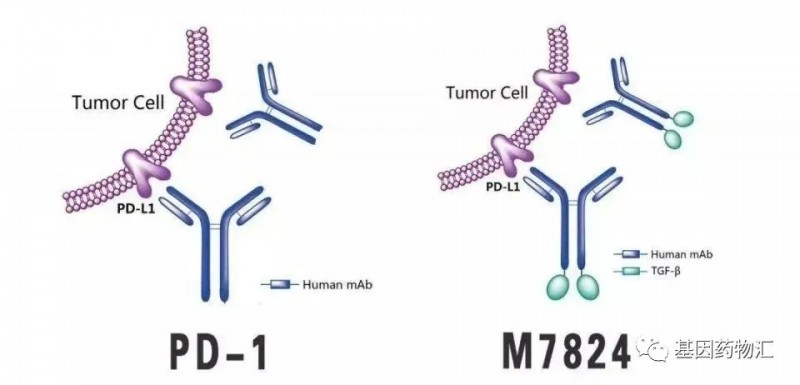
Bintrafusp alfa(代号M7824)是一款由默克公司研发的双功能抗体蛋白,能够同时拮抗TGFβ与PD-L1两个靶点。
临床前研究已经证实,PD-L1和TGFβ途径之间存在一定的互补的相互作用。这意味着,与PD-L1和CTLA-4等组合相似,PD-L1和TGFβ这对组合也有潜力成为一对全新的免疫治疗“搭档”。
非小细胞肺癌
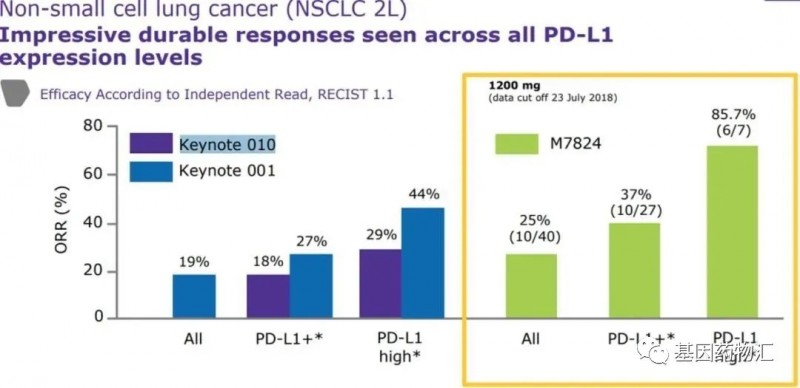
目前,M7824治疗最大样本的研究来自非小细胞肺癌领域。Ⅰ期NCT02517398试验中纳入了80例晚期经治的非小细胞肺癌患者,治疗结果显示,所有亚组患者的整体缓解率为21.3%。
其中,500 mg剂量组患者的整体缓解率为17.5%,1200 mg剂量组的患者整体缓解率为25.0%;而在1200 mg剂量组中,PD-L1表达阳性的患者整体缓解率为36.0%;在PD-L1表达水平≥80%的患者亚组中,患者的整体缓解率更是达到了85.7%!
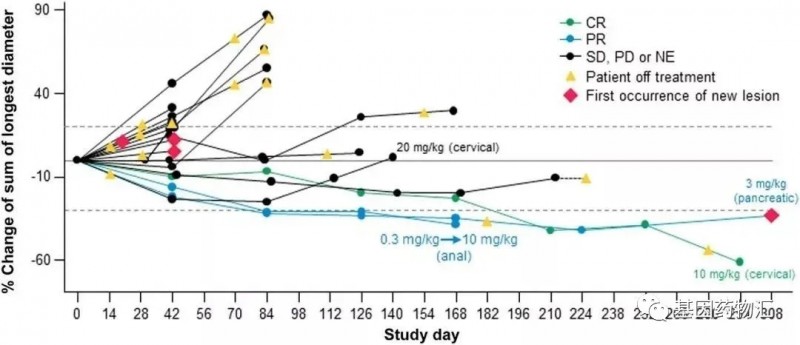
此外,M7824还展现出了出色的广谱抗癌潜力,在包括腺样囊性癌、肛门癌、支气管肺鳞癌、子宫颈癌、脊索瘤、结直肠癌、胰腺癌及小肠癌等多个实体瘤的治疗当中同样展现出了良好的潜力。
其中的这一例宫颈癌患者,更是达到了完全缓解!
有趣的是,完全缓解的子宫颈癌和部分缓解的肛门癌均为HPV阳性的患者,而部分缓解的胰腺癌患者普遍存在错配修复缺陷(HRD)。
目前为止,M7824还是一款“初出茅庐”的新药,正在进行各类临床试验,逐渐扩展适应症。包括美国、英国、加拿大、澳大利亚、欧洲、韩国、日本等多个国家与地区都已经开展了M7824的临床试验项目,验证在各类癌症以及患者人群当中M7824的治疗效果。
近期,中国中心的临床试验也已经开启,正在招募患者。有需求的患者可以联系基因药物汇-临床新药招募中心了解招募详情,或将病历资料及联系方式发送至招募中心邮箱(doctorjona0404@gmail.com)进行申请。
02、PD-1/CTLA-4双抗:比联合方案疗效更好、副作用更少
作为经典的免疫“黄金搭档”,PD-1/CTLA-4这对靶点的“双抗”数量比较多,且进展也非常快。希望了解更多药物的读者,可以阅读《双免疫“黄金搭档”再次携手!横跨十余类癌症,疗效再创新高!》。
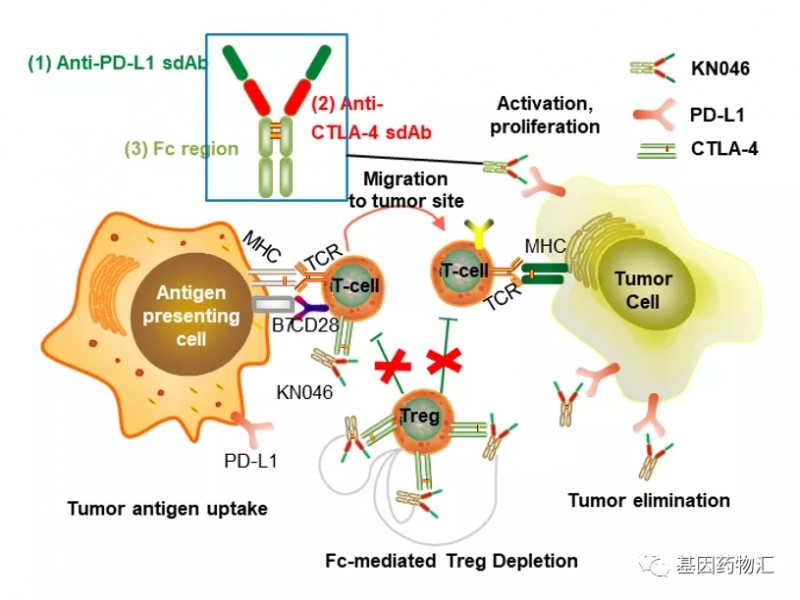
KN046是一款由我国企业自主研发的双特异性抗体药物,对于PD-L1和CTLA-4均有良好的抑制效果。
即使是在双免疫联合方案中,PD-1/PD-L1抑制剂+CTLA-4抑制剂的组合也是一个大热门,KN046的诞生自然收到了广泛的关注。
2020年9月,KN046获得FDA授予的孤儿药资格,用于治疗胸腺上皮肿瘤,成为了首个获得官方认可用于实体瘤的双靶点免疫治疗药物。目前,在澳大利亚与中国两个中心,KN046的临床试验已经覆盖了非小细胞肺癌、三阴性乳腺癌、食管鳞癌、肝癌、胰腺癌等10余个癌种、近20项不同阶段的临床试验,结果均比较理想。
肺癌
01、疾病控制率82.1%,无进展生存7.3个月
根据最近一次世界肺癌大会(WCLC)上公开的数据,研究中共纳入63例患者,分为A(30例)、B(33例)两个试验组,两组患者的基线水平差别不大,A组患者用药剂量稍低(3 mg/kg vs 5 mg/kg)。
截至2020年7月27日的结果显示,A组患者的整体缓解率为10.7%,疾病控制率82.1%;B组患者的整体缓解率为15.6%,疾病控制率62.5%。
患者的中位无进展生存期为3.7个月;3、6、9个月的无进展生存率分别为64.1%、36.6%、34.2%,总生存率分别为91.4%、86.9%和81.0%。
在鳞状细胞肺癌患者亚组中,中位无进展生存期为7.3个月,3、6、9个月无进展生存率分别为80.0%、55.9%、46.6%,总生存率分别为100.0%、88.2%和88.2%。
与前期公开的、KN046治疗曾接受过免疫治疗且疾病持续进展的患者的疗效数据相比,此项试验中纳入的、曾接受过化疗的患者,明显从KN046治疗中获益更多,整体生存期更长。
02、疾病控制率52.0%,无进展生存期2.69个月
根据中国中心的Ⅰa/b期KN046-CHN-001试验研究结果,在29例曾接受过免疫检查点抑制剂治疗失败的患者中共25例患者疾病可评估,KN046治疗的整体缓解率为12.0%,疾病控制率52.0%。
所有患者中位无进展生存期2.69个月;3个月无进展生存率41.0%,6个月无进展生存率21.9%;6个月生存率88%,9个月生存率58.7%。
食管癌
根据2021年ASCO胃肠道研讨会上公开的一项临床试验数据,18例接受了KN046联合同步放化疗的复发或转移性食管癌患者,整体临床缓解率为44.4%,疾病控制率94.4%。
亚组分析结果显示,接受3 mg/kg剂量治疗的患者,疾病控制率为100%;2例患者达到了临床完全缓解。
2020年9月,KN046获得FDA授予的孤儿药资格,用于治疗胸腺上皮肿瘤,成为了首个获得官方认可、有潜力用于实体瘤的双靶点免疫治疗药物。
03、PD-L1/4-1BB双抗:让"冷"肿瘤变"热"
4-1BB的全称是肿瘤坏死因子受体超家族成员9(TNFRSF9)重组蛋白,又称CD137,最初由医学家们于上世纪80年代,从活化的T细胞中发现。
最初,人们发现它能够激活T细胞的杀伤能力,因此被认为具有诱导淋巴细胞激活的功能。后来的研究则发现,4-1BB并不只在T细胞中发挥作用,它同样位于多种细胞的表面,包括DC(树突状细胞)、单核细胞、B细胞等等,只是表达水平比较低。
用于癌症患者时,4-1BB激动剂能够增强人体T细胞的活性、并将惰性的T细胞转变为活性状态,使那部分能够对抗癌细胞的T细胞加速扩增,以抑制癌细胞的生长,并使实体病灶消退。
临床前试验证实了4-1BB激动剂的潜力,但后续的进一步研究也发现了这类药物的不足之处——比方说,4-1BB激动剂造成的不良反应比较特殊,肝毒性严重;且单药使用的时候疗效有限,不具备突破性。
PD-1/PD-L1抑制剂已经深刻地改变了多种癌症的治疗规范,但仍然有一些癌症对于这类药物响应不佳,比如所谓的“冷”肿瘤。
4-1BB是很有潜力的共刺激免疫靶点,但是安全性问题有些棘手,尤其是肝毒性以及疗效方面的局限。
但是4-1BB激动剂又有着刺激免疫效果的作用,换句话说,它完全有潜力将“冷”肿瘤变“热”——那么,如果将PD-1/PD-L1与4-1BB这两类靶点结合起来使用,效果又会如何呢?
已经有很多药企尝试了这一组合。作为一种全新的“双抗”,PD-L1/4-1BB双靶点抑制剂走上了抗癌的“战场”。
许多研究显示,4-1BB激动剂的毒性,与其特殊的Fc段结构相关,因此新一代的药物,要么去除其Fc段结构、另一端融合其它抗体(如结合EGFR抗体),要么改造其Fc段,消除抗体与受体之间的相互作用。
与单独4-1BB靶点的药物相比,“双抗”最大的优势在于,另一端的抗体(例如PD-L1)可以将药物带到这类靶标富集的区域,即肿瘤病灶部位,并借助4-1BB来激活病灶周围的T细胞,最终杀灭癌细胞。
且此类新一代的药物不良反应更少,肝毒性减轻甚至消除,患者的耐受性更好。
这样的机制充分利用了“癌细胞大量表达PD-L1以逃脱免疫T细胞的攻击”的特点,将“敌人”手中的“盾”,变成了刺向它们自己的利刃。
除了我们提到的靶向治疗药物,在嵌合抗原受体T细胞疗法(CAR-T疗法)的研究开发过程中,4-1BB也成为了一个备受关注的靶点。
说过了机理,我们再来谈谈新药。针对这对靶点,已经有多家药企开启了研发布局。仅仅只看国内,就有恒瑞、信达、齐鲁、科望等等众多著名企业。
这些新药无一例外都将“减轻肝毒性”视为重点,潜力十足。有兴趣尝试新药临床试验的患者,可以联系我们申请。
靶向+免疫"双抗":全新发展方向,发挥双重抗癌效果
除了双免疫方案以外,临床上最常用的免疫治疗方案其实包括两种:免疫+化疗,以及免疫+靶向(抗血管)治疗。
我们都已经了解了被称为免疫“双抗”的,能够同时抑制两个免疫检查点的双特异性抗体。如果将这种思路应用于免疫+抗血管以及其它的关键靶向治疗靶点,是否能够制造出一种,疗效超越双药方案、不良反应又更轻的新型“双抗”呢?
01、PD-1/VEGF双抗:靶免"双抗"的先驱
AK112,由我国康方生物研发。这款药物能够同时抑制PD-1与VEGF,是一款同时具备靶向药与免疫药功能的“双抗”。这款药物的在研适应症也很多,包括了关键的妇瘤等多种实体瘤。
这次的CSCO大会上,来自中山大学肿瘤防治中心二代张力教授,为我们带来了AK112联合化疗一线治疗非小细胞肺癌的出色研究成果。
非小细胞肺癌
01)缓解率:53.8%
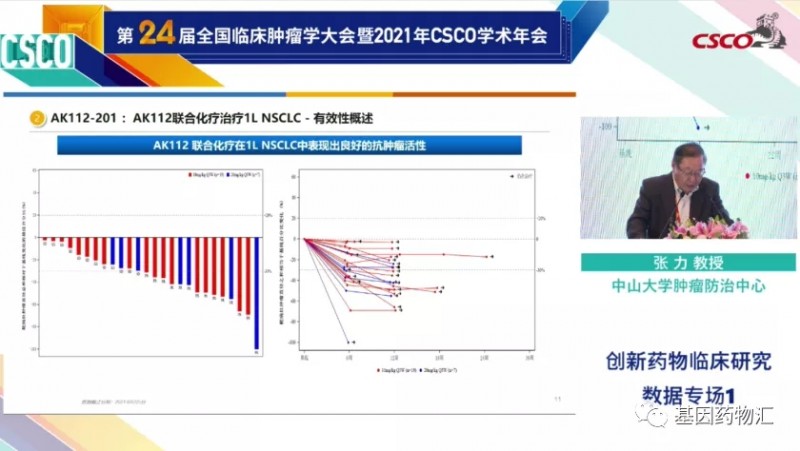
在目前为止已经接受过评估的26例患者当中,14例患者达到了临床缓解,整体缓解率高达53.8%;所有患者的疾病都得到了不同程度的控制,疾病控制率高达100%!
图中左侧柱形图:已经完成了至少1次评估,列入本次统计当中的26例患者,病灶均有不同程度的缩小;图中右侧蛛网图:折线末尾有黑色箭头标记的患者,均仍在接受治疗。
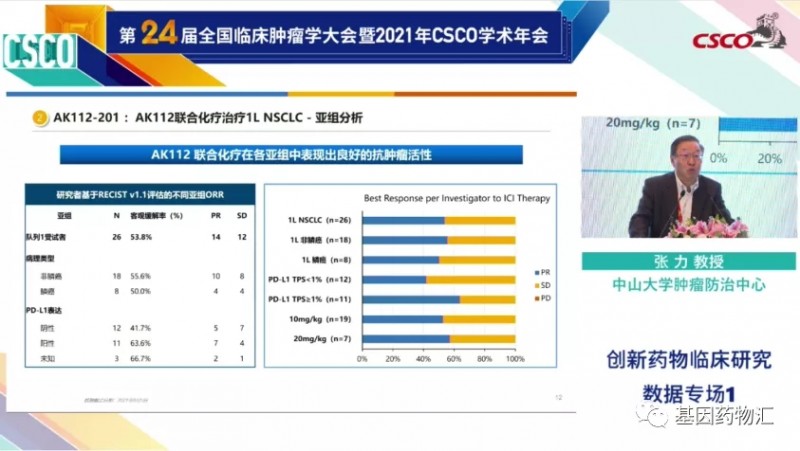
02)亚组分析:多类型患者均可获益
亚组分析结果显示,PD-L1表达阳性的患者中,整体缓解率为70%;尤其是在PD-L1表达阳性的腺癌患者当中整体缓解率最高,为83.3%,此外还有一例病灶缩小比例达到27.3%的患者,非常接近临床缓解的标准。
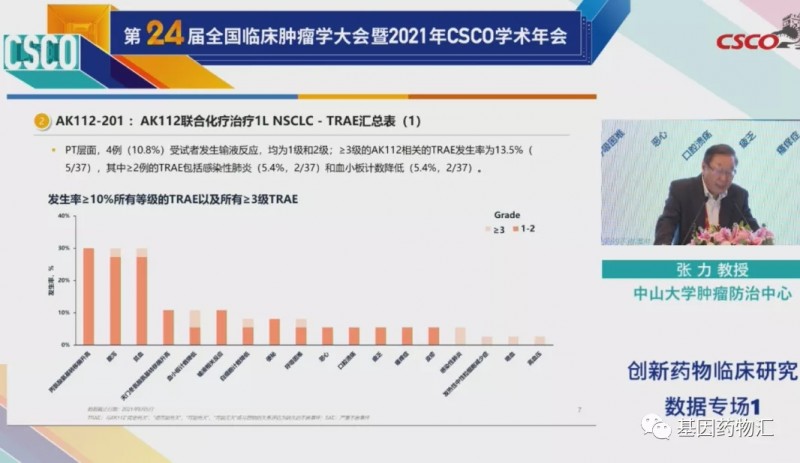
03)安全性:试验药物治疗相关不良事件13.5%
3级或以上的AK112治疗相关不良事件发生率为13.5%,其中最常见的是感染性肺炎(5.4%)和血小板计数降低(5.4%)。
02、EpCAM/CD3双抗:专"克"腹水
M701是一款注射用重组抗EpCAM/CD3人鼠嵌合双特异性抗体。人源化的Fc片段IgG1让M701的免疫原性降低,更不容易导致其与人体发生的副作用。而自主知识产权的CD3序列,CD3亲和力弱化,发生细胞因子风暴不良事件的概率也同时下降。
近期,研究者公开了M701的Ⅰ期试验中期数据。缓解率方面,在16例可评估的患者当中,腹水的临床缓解率为62.5%,控制率为100%;包括了3例完全缓解、7例部分缓解和6例疾病稳定。患者的中位总生存期为152天,其中卵巢癌患者的中位总生存期为148天,胃癌患者为209天。
目前这款药物的后续试验正在招募患者,腹水患者可以联系基因药物汇-临床新药招募中心了解招募详情,或将病历资料及联系方式发送至招募中心邮箱(doctorjona0404@gmail.com)进行申请。
进击的"三抗",正在布局
为了获得更好的治疗效果、达到更多的治疗目标,一部分癌症精准治疗方案走上了“越来越复杂”的道路。靶向+免疫+化疗、双免疫+化疗、双免疫+靶向,越来越多的组合投入了临床应用以及临床试验当中。
其中,PD-L1/VEGF-A/TGF-β“三抗”等药物的发展比较快,有兴趣尝试或了解详情的患者,可以联系我们。