第二代ROS1/NTRK双靶点抑制剂,Talectrectinib(DS-6051b)数据公布,AB-106临床试验招募中
近两年,靶向治疗带给我们的惊喜不断,其中,不限癌种广谱抗癌药的突破性进展更是给晚期患者带来了生命之光,因为目前获批上市的不限癌种靶向药,款款堪称抗癌“特药”,有效率超高,比如首款获批的NTRK抑制剂拉罗替尼,在实体瘤中的客观缓解率高达75%,第二款获批的NTRK抑制剂恩曲替尼客观缓解率为57.4%,这些不分年龄,不分癌种,不限分期,有效率超高的药物开启了肿瘤治疗的新篇章。
近期,又一款广谱抗癌药Taletrectinib(DS-6051b / AB-106)登上了国际癌症顶级期刊《clinical cancer research》,在癌友圈中引起了轰动。
初识ROS1/NTRK双靶点抑制剂Taletrectinib
Talectrectinib代号为DS-6051b/AB-106,是一款新型、有效、选择性高的下一代ROS1和NTRK双靶点小分子抑制剂,可穿越血脑屏障。
它长这个样子:
单看化学结构式并没有什么特别,然而这款新药在临床中却有非常显著的优势:
1、双靶点:对ROS1及NTRK1-3具有高效抑制作用;
2、安全性好,应答率高,有效持续时间长,带给病人更长的无疾病进展生存期;
3、对克唑替尼治疗失败的ROS1阳性非小细胞肺癌患者(主要耐药位点ROS1 G2032R同样具有高效抑制作用)及脑转移患者也有效;
4、不限癌种,有ROS1或NTRK融合突变就可适用,是新一代广谱抗癌药,有潜力与国际领先的上市明星产品Larotrectinib (拉罗替尼,LOXO-101)、Entrectinib (恩曲替尼, RXDX-101)及在研产品Repotrectinib (TPX-0005)相媲美。
美国晚期实体瘤患者I期首次人体研究数据出炉
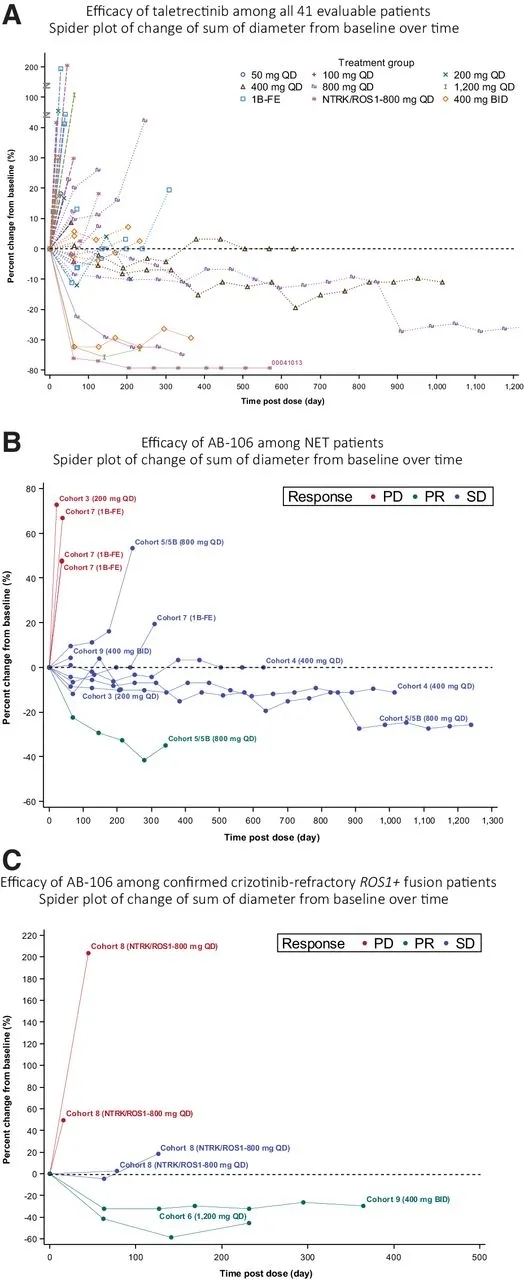
本次在《临床癌症研究》上发表的是taletrectinib在美国开展的治疗晚期实体瘤患者的1期临床数据,这也是taletrectinib在美国开展的首个人体试验。
招募对象:此次试验共有46例患者入组,包括成人神经内分泌肿瘤患者、患有肿瘤引起疼痛的晚期实体瘤患者、以及携带ROS1/NTRK基因重排的肿瘤患者。
试验设计:入组的患者每日服用不同剂量 taletrectinib,研究的主要目标是评估taletrectinib的安全性和耐受性。
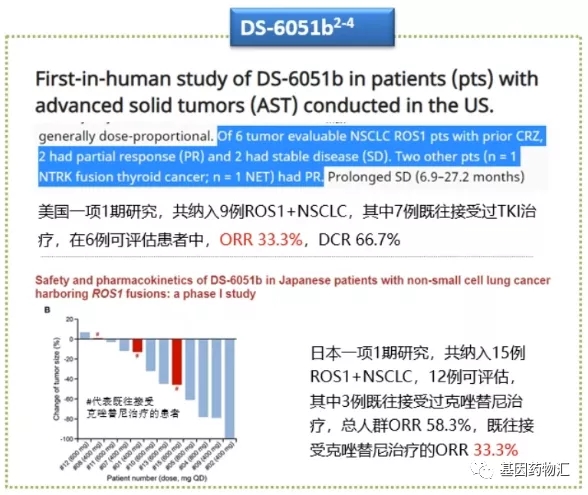
研究结果:taletrectinib在每日800mg的最佳剂量下具有可控制的毒性;而在克唑替尼耐药的ROS1+NSCLC患者中疗效显著,在6例可评估的克唑替尼耐药后难治性的ROS1+NSCLC患者中,客观缓解率(ORR)还能达到33.3%。
非小细胞肺癌:
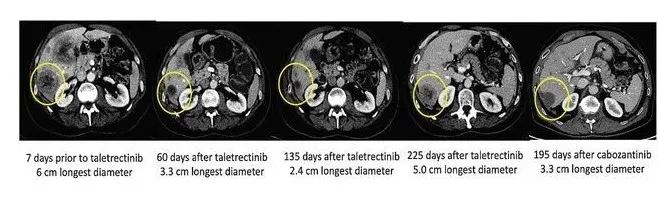
其中,有一名患有ROS1 + 的晚期非小细胞肺癌患者,在接受克唑替尼和色瑞替尼治疗后出现耐药并发生肝转移,基因检测后发现存在CD74-ROS1融合,每天接受一次1,200 mg taletrectinib的治疗后,患者达到部分缓解。
甲状腺癌:
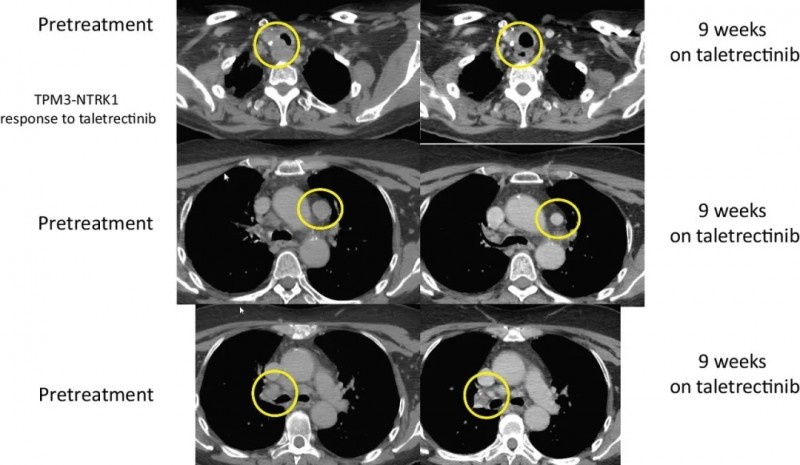
另一位患者是晚期甲状腺癌,手术后接受了化学放疗,放射性I-131,索拉非尼,以及PD-1的临床试验,后经过Foundation One CDx检测到存在TPM3-NTRK1 融合,参加了taletrectinib的临床试验,截止到文献发表,这名幸运的患者持续缓解时间已经长达33.4个月,将近3年。
神经内分泌癌:
此外,在数据截止时,两名神经内分泌患者仍在接受治疗,一名患者已接受taletrectinib治疗,每日一次400 mg,持续47.2个月,将近四年!另一名患者接受800 mg,每天一次,持续41.4个月!
安全性:
最常见的治疗相关不良事件是恶心(47.8%)、腹泻(43.5%)和呕吐(32.6%)。
Taletrectinib:针对脑转移患者同样有效
根据临床前研究的结果,AB-106对于ROS1 G2032R和L2026M突变敏感,同时具有较好的入脑性,适合治疗克唑替尼耐药后的患者。
目前为止,AB-106已经在Ⅰ期研究中展现出了较好的治疗潜力。在2018年ASCO大会上,研究者公开了Ⅰ期安全性、耐受性和剂量限制性毒性研究的结果。研究中共纳入46例患者,其中7例患者为ROS1融合阳性的非小细胞肺癌患者,6例患者拥有可评估的实体病灶。其结果显示,2例患者达到部分缓解,2例患者疾病稳定,整体来说,整体缓解率达到33.3%。研究将AB-106的最大耐受剂量确定为800 mg qd。
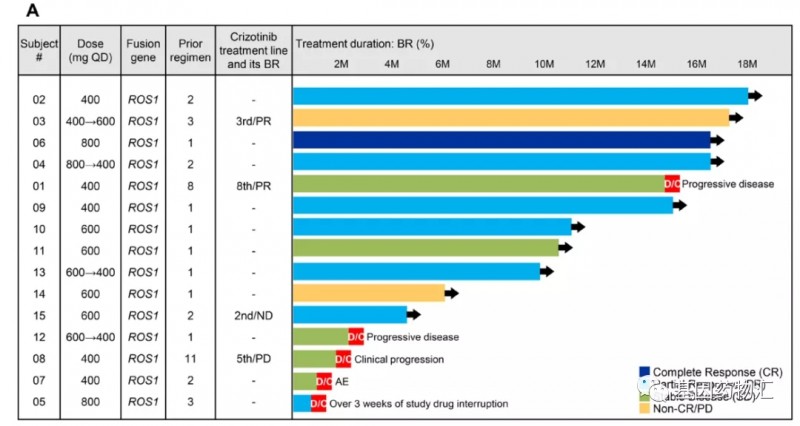
在2018年5月的Oncotarget上公开了日本研究的结果,共纳入15例ROS1阳性肺腺癌患者,其中4例患者为克唑替尼耐药患者;存在可评估病灶患者共12例,3例为克唑替尼耐药患者。12例患者接受药物剂量为600 mg qd,3例患者剂量为800 mg qd。
试验结果显示,在可评估的3例克唑替尼耐药患者中1例达到部分缓解,2例患者疾病稳定,整体缓解率33.3%;9例非克唑替尼耐药患者中,1例达到完全缓解,5例达到部分缓解,整体缓解率66.7%,疾病控制率100%。
研究中共纳入了5例脑转移患者,其中1例患者的颅内病灶达到完全缓解。
AB-106国内临床招募正式开始
目前,taletrectinib已经在日本和美国完成了1期临床试验,用于治疗含有ROS1或NTRK融合基因实体瘤患者。好消息是,2020年3月,该药在中国获得批准开展两项新的临床研究,针对携带ROS1融合基因的NSCLC,以及携带NTRK融合基因的不分瘤种的实体瘤患者的二期临床试验,这意味着,国内的患者也有机会免费接受国际抗癌新药的治疗。
试验题目:
AB-106治疗携带ROS1融合基因的局部进展或全身转移的晚期非小细胞肺癌(NSCLC)的一项Ⅱ期、多中心、单臂、开放的研究
试验类型:单臂试验
试验分期:Ⅱ期
首次公开时间:2020-05-15
纳入标准(部分):
1、年龄≥18岁,男性或女性;
2、ECOG评分0~1分,预期生存期>6个月;
3、局部进展或全身转移性晚期非小细胞肺癌,Ⅲb期或Ⅲc期或Ⅳ期患者,ROS1突变阳性;
4、接受克唑替尼治疗失败或未经克唑替尼治疗均可,患者需提供已经存档的或新近取得的肿瘤组织标本;
5、合并脑转移的患者中枢神经系统症状稳定等;
6、详细纳入及排除标准可咨询全球肿瘤医生网医学部。
申请流程:
需要申请临床试验的患者需将基因检测报告、病理报告提交至全球肿瘤医生网医学部进行初步评估,我们的专家将为您全面分析解读检测报告、推荐新药及用药方案,并匹配适合入组的临床试验项目。
注:请将基因检测报告、诊断报告电子版或清晰照片发送至doctor.huang@globecancer.com,邮件中留下联系方式,医学部收到报告分析完毕后一个工作日内电话联系。
需要提醒大家的是,即使是标准治疗方案失败,也可以尝试进行基因检测,一旦存在ROS1,NTRK1、NTRK2或者NTRK3基因融合,就可以尝试这些特效的广谱抗癌药。做过基因检测的病友,可以将报告发送至全球肿瘤医生网医学部申请,我们的专家将为您全面分析检测报告,匹配能够入组的临床试验,以及有无新药可以使用。
目前已经上市的多款广谱抗癌药:拉罗替尼,恩曲替尼,LOXO-292等仍在国内的招募仍在进行,由国内肿瘤领域权威的几家医院率先开展。以前这些美国研发上市的抗癌新药对于国内的患者来说遥不可及,近两年随着国家的重视,加快了各类抗癌药物研发上市的审批速度,让更多国外的新药好药,也能造福国内的癌症患者。希望这款药物能尽快在国内完成临床试验,顺利上市,造福患者。
参考资料:
https://anhearttherapeutics.com/en/category/news/
https://clincancerres.aacrjournals.org/content/26/18/4785