2020年治疗胃癌的药物有哪些,胃癌靶向药物,胃癌免疫治疗(PD-1/PD-L1)药物
中国每年近50万人死于胃癌,占全球总数的一半以上!中国发病率和死亡率远高于全球平均水平,发病率仅次于肺癌,死亡率位列第三。在大多数情况下,手术仍然是无进展生存性治疗的主要手段。随着靶向治疗的兴起,胃癌发生、发展分子机制研究的不断深入,胃癌的分子靶向和免疫治疗治疗逐渐崭露头角。
比如,对于HER-2阳性的胃癌患者,赫赛汀可以延长生存;抗血管生成药物雷莫卢单抗可以延长一线化疗失败的晚期胃癌患者的生存期;阿帕替尼能够延长二线治疗失败的胃癌患者的生存获益等,全球肿瘤医生网医学部为大家盘点了目前胃癌FDA批准的靶向及免疫药物以及的研究进展,希望给病友们增加战胜癌症的信心。
胃癌已上市的靶向和免疫药物
目前针对胃癌的靶点主要包括TP53,EGFR,HER-2,VEGF,VEGFR,MET,FGFR2,mTOR等。
但在过去十年间,胃癌分子靶向治疗的探索主要集中在两个途径,肿瘤细胞的EGFR通路和血管内皮细胞的VEGFR通路,研究者针对这两种通路开发了一系列的药物,并开展临床试验验证其在胃癌中的疗效。目前FDA获批的靶向及免疫疗法只有三种。
| 研发公司 | 药物靶点 | 药物名称 | 上市时间 | 中国是否上市 | 医保报销 |
| 罗氏 | HER2 | 曲妥珠单抗(Trastuzumab) | 1998 | 是 | 是 |
| 礼来 | VEGFR2 | 雷莫芦单抗(Ramucirumab) | 2014 | 否 | 否 |
| 默沙东 | PD-1 | 帕博利珠单抗(Pembrolizumab) | 2017 | 是 | 否 |
HER2靶向药
曲妥珠单抗(Herceptin 赫赛汀、Herzuma、Ogivri)
2012年10月,曲妥珠单抗批准可用于HER2阳性转移性胃癌的一线治疗(胃腺癌或胃食管连接处的腺癌)。
在此需要提醒大家的是,晚期胃癌HER2治疗已获得全球共识,NCCN指南推荐胃癌患者检测HER2表达, 如果检测结果显示HER2+,那么患者一线推荐使用曲妥珠单抗联合化疗,而如何检测HER2是关键!
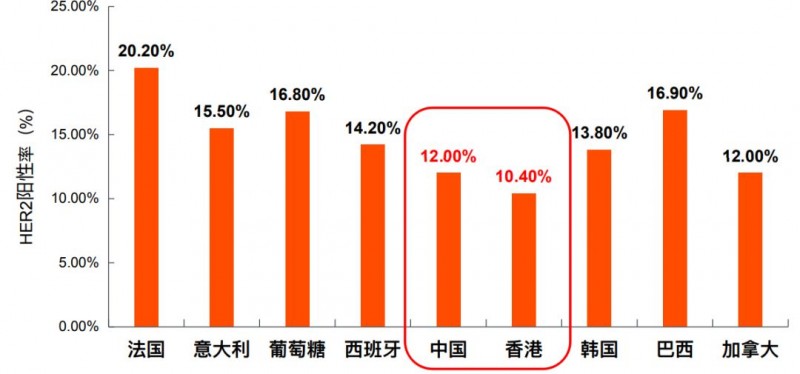
长期以来,IHC和FISH是检测HER2的金标准,临床上一项大型、非干预性、国际性流行病学研究(HER-EAGLE),共纳入4949例胃腺癌或胃食管结合部癌患者,旨在评估不同国家真实世界中的HER2阳性率 :结果显示,我国胃癌患者的HER2阳性率低于国外水平。传统的FISH/IHC遗漏将近50%的HER2/ERBB2 改变!大家一定要慎重选择检测机构,如做过检测的病友可以联系全球肿瘤医生网医学部进行解读,评估可用的治疗方案。
VEGF靶向药
雷莫芦单抗(Cyramza)
雷莫芦单抗(ramucirumab,Cyramza®)是一种抗血管生成的靶向药物。
2014年4月21日,FDA批准雷莫芦单抗用于接受过氟嘧啶或含铂化疗后疾病进展的晚期胃或胃食管结合部腺癌患者的治疗。成为第一个化疗后进展晚期胃癌患者的治疗药物。
甲磺酸阿帕替尼(国内获批)
除了雷莫芦单抗,还有一款在国内上市的抗血管生成药物甲磺酸阿帕替尼,是我国自主研发新药,其主要作用机制是竞争性结合该受体胞内酪氨酸ATP结合位点,高度选择性地抑制VEGFR-2酪氨酸激酶活性,阻断VEGF通路信号转导,从而有效抑制肿瘤血管生成。
中国国家药监局于 2014 年 10 月 17 日正式批准其用于晚期胃癌或胃食管结合部腺癌患者三线及三线以上治疗。
免疫治疗PD-1药物
派姆单抗(keytruda)
2017年9月,FDA批准派姆单抗用于已经接受过至少2次治疗(包括化疗)的晚期胃癌患者,用于治疗复发性局部晚期或转移性胃或胃食管连接(GEJ)腺癌的患者,其肿瘤表达PD-L1 [综合阳性评分(CPS)≥1],由FDA批准的测试确定。在包括含氟嘧啶和铂的化学疗法,或者HER2 / neu靶向疗法两线或多线治疗后进展。另外,基因检测结果MSI-H的胃癌患者也适用。
纳武单抗(Opdivo,国内获批)
2020年3月,中国国家药品监督管理局正式批准欧狄沃(纳武利尤单抗注射液)用于治疗既往接受过两种或两种以上全身性治疗方案的晚期或复发性胃或胃食管交界腺癌患者。(PD-L1阳性)
这是中国首个也是目前唯一一个获批用于晚期胃癌的免疫治疗药物,也是迄今唯一经过Ⅲ期临床试验证实能为中国晚期胃癌患者带来生存获益的PD-1抑制剂。
ATTRACTION-2的研究结果证实,opdivo用于胃癌三线或三线以上治疗安全性良好,且这部分患者一旦获益,其中有61.3%患者的生存期可延长2年以上。
胃癌研究进展盘点
一,无进展生存率51%!DS-8201成为晚期胃癌治疗药物的一匹黑马
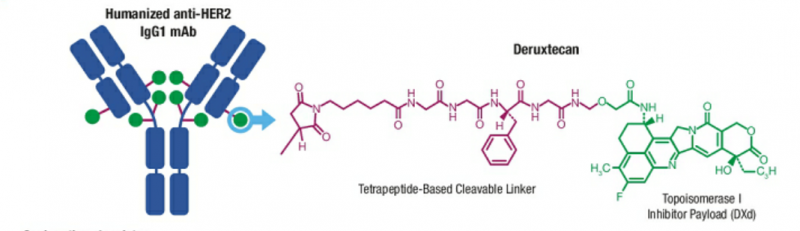
DS8201(trastuzumab deruxtecan,T-DXd) ,是一种HER2抗体+伊立替康类化疗药物的偶联药物,属于ADC型药物类型(抗体偶联药物)。它有两部分组成:第一部分是针对HER2靶点的抗体,可以精准的识别并且结合HER2高表达甚至低表达的肿瘤细胞;第二部分是剧毒的化疗药伊立替康。这种设计会使抗体带着化疗药去找肿瘤细胞,然后精准地给肿瘤细胞下毒,毒死它们。
这种药物设计结合了靶向药的精准和化疗药的高效,既避免了全身使用化疗药的毒副作用,也比单独使用靶向药具有更强的杀伤能力,一举两得。
在代号为DESTINY-Gastric01的随机,II期,多中心,开放标签研究中,评估了DS-8201在HER2阳性晚期胃或胃食管交界处(GEJ)腺癌患者中的有效性。
纳入187例接受过至少两次治疗的HER2阳性胃或胃食管交界处腺癌患者,所有患者随机分组,分别接受DS-8201(125人)或化疗(62人),其中日本患者占79.7%,韩国患者占20.3%。
研究结果显示:
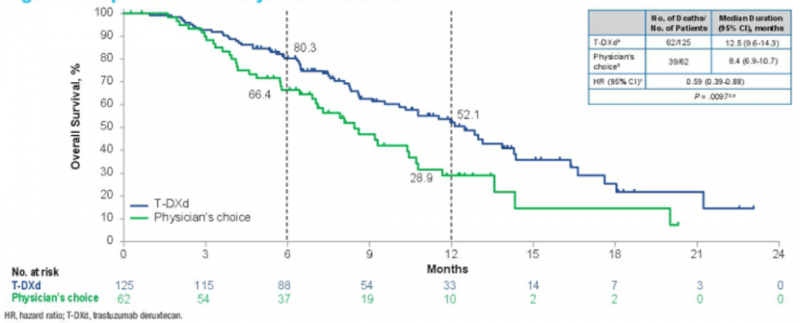
客观缓解率(ORR):DS-8201组的为51.3%(61/119),包括11例完全缓解(CR)和50例部分缓解(PR),而化疗方案组仅为14.3%(8/56);
疾病控制率(DCR):分别为85.7%和62.5%(P=0.0005);
中位缓解持续时间(DoR):分别为11.3个月和3.9个月
中位无进展生存期(PFS):分别为5.6个月和3.5个月。
在 HER2、晚期胃或胃食管交界癌患者中,DS-8201的客观缓解率明显高于常规化疗,总生存期较常规化疗更长。
预计FDA将基于DESTINY-Gastric01的惊艳数据,批准DS-8201作为胃癌晚期治疗的新药上市。
二,未来可期!ZW25联合替雷丽珠单抗进军晚期胃癌一线治疗
ZW25是一种基于Zymeworks的Azymetric TM 平台的双特异性抗体,其可以同时结合HER2的两个非重叠表位,称为双互补位结合,可以双重阻断HER2信号,增加HER2蛋白从细胞表面的结合和去除,具有更强的抗HER2驱动肿瘤生长的作用。
这样一个新型双特异性抗体,跨癌肿有效,副作用轻微,令学术界十分激动。此前,一项多中心1期研究的数据显示,单一药物ZW25可诱导抗肿瘤活性,并且对HER2阳性经过各种治疗失败的患者具有良好的耐受性。
ZW25在多种表达HER2的肿瘤类型中具有活性和耐受性;
持久的抗肿瘤活性,中位无进展生存>六个月;
经过标准治疗失败的患者总控制率达到82%。
在2020年ASCO大会上,ZW25公布了联合或不联合替雷利珠单抗作为晚期HER2阳性乳腺癌或胃/胃食管连接腺癌患者的一线治疗方案的1B / 2期临床试验设计。我们期待这项研究能早日获得阳性的临床数据。
三,AMG199首次人体1期研究正式开始
AMG199是一种靶向MUC17/CD3的双特异性抗体。该药物由两个单链可变片段组成,一个针对肿瘤相关抗原(TAA)人粘蛋白17(MUC17),一个针对人CD3(T淋巴细胞上发现的一种T细胞表面抗原),具有潜在的抗肿瘤活性。给药后,AMG199可与T细胞上的CD3和肿瘤细胞上表达的MUC17结合,促使T细胞和肿瘤细胞交联,并诱导针对表达MUC17的肿瘤细胞的强效细胞毒性T淋巴细胞(CTL)反应。
在本次ASCO大会上,公布了一项首次在人体的1期开放标签剂量递增研究(NCT04117958),评估AMG199治疗MUC17阳性胃/胃食管交界癌症患者的剂量限制性毒性及无进展生存率。
这是首个研究将MUC17作为潜在抗肿瘤靶标的临床试验,该研究于2020年1月开始招募患者,目前正在进行中。
四,65岁以上晚期胃癌患者或可获益于安德西昔单抗治疗
Andecaliximab是一种MMP9抑制剂; MMP9是在许多实体瘤和所有胃癌中过表达的蛋白质。它的作用是重塑细胞外基质; 它与增加的血管生成和增加的髓样抑制细胞和[调节性T细胞]的募集相关。[MMP9过度表达]使免疫监视变得更加困难,使癌症更容易分解基质并扩散。因此,MMP9是一个很好的靶标。
GAMMA-1GAMMA-1是一项关于andecaliximab联合FOLFOX一线治疗胃癌患者的III期研究。结果显示:在HER2阴性胃癌患者的一线治疗中,与单独的化疗相比,未发现MMP9抑制剂安德西昔单抗(Andecaliximab)加入FOLFOX6可提高总生存期(OS)和无进展生存期(PFS)。但敏感性分析显示该药物可能对65岁以上老年患者有益。
研究人员认为,在老年人群中,胃癌的生物学有点不同; 也许细胞外基质是不同的,这可能会导致老年人群的特异性敏感性。
五,过继性MTCA-CTL免疫治疗
对胃癌来说,免疫治疗中人群的选择是非常重要的,但目前都没有明确的最终结论。细胞免疫治疗通过往体内回输一些具有免疫功能的细胞,来帮助免疫系统的重建,一定程度上会帮助我们的免疫系统去杀肿瘤,但如果肿瘤体积太大,细胞免疫治疗起到的治疗作用就很有限。
目前,国内的免疫治疗技术已经更新至第五代,即MTCA-CTL免疫疗法。
MTCA-CTL免疫疗法在保证非 MHC限制性 杀伤性NK-T细胞扩缮的同时,定向扩增MHC限制性的CD8+特异性CTL细胞,使其在细胞培养产品中的 比率可达到60-70% 这两种杀伤细胞的共同作用,使杀伤癌细胞的效率更高。
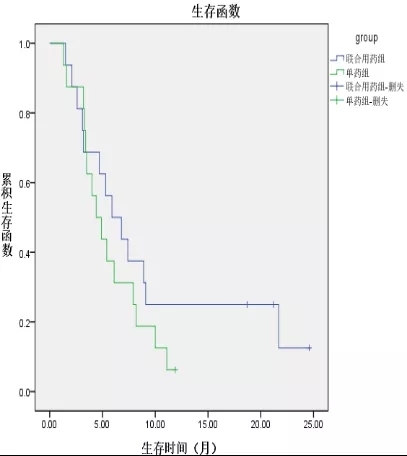
中国医科院肿瘤医院发布国内新一代细胞免疫疗法MTCA-CTL联合化疗治疗胃癌II 期临床研究数据,与化疗组相比,联合治疗组治疗不可切除胃癌(来自中国医科院肿瘤医院GCP中心)中位无进展生存期延长135天!中位生存期延长120天!
PD-1抗体、PD-L1抗体目前是非常新的热点,确实在研究中可以看到很好的结果,但并非适合所有胃癌患者,不能盲目追求。
Claudin18.2 CAR-T
近两年,我们国家的实体肿瘤取得了备受世界瞩目的成绩,研发出了国际上首个靶向Claudin18.2的实体瘤CAR-T疗法。
Claudin18.2(CLDN18.2)是一种胃特异性膜蛋白,被认为是胃癌和其他癌症类型的潜在治疗靶点。基于此,中国研究人员开发了国际上首个针对 Claudin18.2 的 CAR-T 细胞。
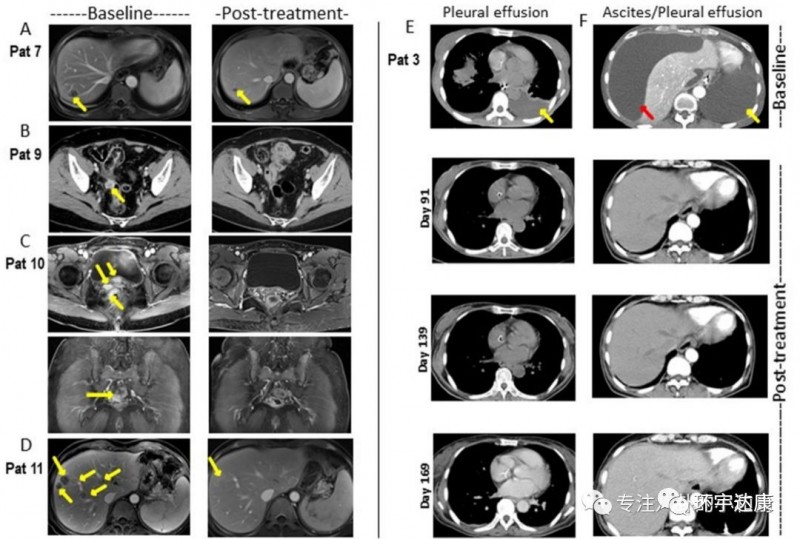
2019 ASCO年会上,CAR-Claudin18.2 T 细胞治疗胃癌/胰腺癌的临床数据更新显示,靶向claudin18.2 CAR T细胞治疗12例转移性腺癌(胃癌7例,胰腺癌5例),未发生严重不良事件、治疗相关死亡或严重神经毒性。
11例评估对象中:
1例(胃腺癌)完全缓解;
3例(胃腺癌2例胰腺腺癌1例)部分缓解;
5例病情稳定;
2例病情进展;
总客观缓解率为33.3%。
并且,CAR-Claudin18.2 T 细胞治疗胃癌的临床前研究成果显示,靶向Claudin18.2的CAR-T细胞在小鼠模型中可以完全清除胃肿瘤,且没有发生脱靶毒性。
好消息是,这项试验已经率先由国内胃肠道肿瘤享负盛名的北京大学肿瘤医院胃肠肿瘤科开展,评估自体人源化抗claudin18.2嵌合抗原受体T细胞在晚期实体瘤中的安全性及功效。
入组标准(部分)
1.年龄18至75岁,男性或女性;
2.患有病理证实的实体瘤(即晚期胃癌,食管胃交界癌和胰腺癌)并且经标准治疗失败的受试者;
3.Claudin 18.2 IHC染色阳性;
4.预计寿命>12周;
除此之外,还有一些在研的新型免疫治疗药物在胃癌的治疗上取得了很好的疗效,例如ICOS激动剂JTX-2011,IConIC 1/2期临床研究中八例胃癌患者有两例获得了明显的肿瘤退缩,疾病控制分别大于8.5个月及11个月,并且在治疗过程中都出现了明显的外周血免疫细胞亚群的变化,未来也期待ICOS激动剂在胃癌领域有进一步的突破。
相信上面这些在研药物给了晚期胃癌患者新的希望,同时也能看出,随着新型临床研究如雨伞篮子研究的推进,对检测提出了更高要求,需要全面了解患者的基因图谱 ,已经做了检测的可以登录全球肿瘤医生网医学部全面的解读报告获得用药方案及临床试验推荐。相信胃癌患者的明天会越来越好。