继去年12月19日,美国食品和药物管理局(FDA)批准K药用于治疗Merkel细胞癌(一种罕见皮肤癌)之后。近日,默沙东公司又宣布,免疫肿瘤学明星(抗PD-1)Keytruda(简称K药)作为二线疗法,在治疗晚期转移性食管癌和胃食管连接部肿瘤患者的3期临床试验中达到主要终点。
结果显示:与化疗相比,在肿瘤PD-L1表达水平CPS评分≥10的食管癌患者中,K药显著提高患者的总生存期(OS)。这也使得Keytruda在同类产品中成为第一个能够证明能提高食管癌患者存活效益的产品。
关于KEYNOTE-181研究
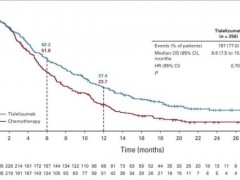
KEYNOTE-181是一项随机、开放标签的3期临床研究,纳入了628名晚期或转移性腺癌或鳞状细胞癌食管癌,或胃食管连接部Siewert I型腺癌患者(在一线标准疗法后疾病进展),患者以1:1的比例随机接受K药单药治疗或医师选择的化疗方案(多西他赛、紫杉醇或伊立替康)。K药组和化疗组的中位随访期分别为7.1个月 vs 6.9个月。
结果表明,在PD-L1表达阳性(CPS评分≥10)的患者中(n=222),K药组的中位OS为9.3个月,而化疗组的中位OS为6.7个月,Keytruda显著降低患者的死亡风险31%。K药组患者在12个月时的总生存率更有优势,约为43%,而化疗组的这一比例仅为20%。
鳞状食管癌患者(n=401),与化疗组中位OS(7.1个月)相比,K药组中位OS达到8.2个月,为患者带来了具有临床意义的生存改善,虽尚未显著达到研究预期设定的统计学意义但K药表现出了与此前研究中一致的,良好的安全耐受性。
我国为消化道肿瘤高发地区,大多数食管癌患者确诊时已处于较晚期,对于晚期食管癌的主要治疗方法——化疗与靶向治疗效果欠佳,疾病复发率和转移率较高,食管癌患者的总体预后较差(中位生存期 9-23个月左右,五年生存率仅15%-25%),因此迫切需要寻求新的治疗手段且疾病进展后缺乏标准治疗,食管癌的二线治疗状况急需改善,K药(Keytruda)能够显著改善PD-L1表达阳性的食管癌患者的总生存率,这是重要的科学进步,将为目前治疗选择有限的食管癌患者带来生存获益。
关于K药(Keytruda,派姆单抗)
通用名:帕博利珠单抗注射液
商品名:可瑞达/Keytruda
英文名:Pembrolizumab Injection
生产厂商:美国MSD默沙东药厂
用法与用量:2mg/kg(患者体重),静脉输注30min,每三周一次。
价格信息如下:
【100mg/4ml】的价格是17918元 (中国)
【100mg/4ml】的价格是17918元 (美国,折合人民币33000元)
【100mg/4ml】的价格是30000港币(美国,折合人民币26200元)
默沙东正在对超过9000名患者中开展对Keytruda的进一步研究,包括其在胃癌、肝细胞癌和食道癌等多种消化道肿瘤中的应用。在3期试验KEYNOTE-590中,Keytruda与化疗联合用药一线治疗食管癌的方案也正在接受检验。
从全球范围获批适应症数量而言,K药是目前用于治疗晚期瘤种最广泛的免疫药物。它已在80多个国家获批使用,覆盖了12个瘤种的16个以上适应症,具体如下:
以免疫检查点抑制剂为代表的免疫治疗将实体瘤治疗带入了激动人心的时代,我们相信这款重磅免疫疗法为食道癌患者带来巨大的生机。
参考来源:https://pharmaphorum.com/news/keytruda-cuts-risk-of-death-by-31-in-esophageal-cancer-trial/